Clear Sky Science · de
Synthese, spektroskopische Charakterisierung, antimikrobielle Wirkung, DNA-Interaktion, DFT- und molekulare Docking-Studien eines neuen Cu(II)-Schiff-Base-Komplexes
Warum ein vitamininspiriertes Metallmedikament wichtig ist
Viele der heutigen Antibiotika und Krebsmedikamente verlieren an Wirksamkeit – entweder weil Mikroben Resistenzen entwickeln oder weil Nebenwirkungen die maximal verträglichen Dosen begrenzen. Diese Studie untersucht einen einfallsreichen Ansatz: die Herstellung einer neuen kupferbasierten Verbindung aus Folsäure – dem bekannten Vitamin B9 – und die Prüfung, ob dieses maßgeschneiderte Molekül Bakterien angreifen, an DNA binden und das Wachstum von Brustkrebszellen verlangsamen kann. Indem ein Nährstoff, der von schnell teilenden Zellen bevorzugt aufgenommen wird, mit einem biologisch aktiven Metall kombiniert wird, zielen die Forschenden darauf ab, ein intelligenteres, vielseitigeres Therapeutikum zu schaffen.
Aus einem gebräuchlichen Vitamin ein maßgeschneidertes Werkzeug formen
Das Team begann mit Folsäure, einem Vitamin, das unsere Zellen für den Aufbau und die Reparatur von DNA benötigen und das Krebszellen häufig anreichern. Sie verknüpften Folsäure chemisch mit Salicylaldehyd, einer einfachen aromatischen Verbindung, und erzeugten so eine neue Schiff-Base-Ligandstruktur – im Wesentlichen einen maßgeschneiderten Haken zum Erfassen eines Metallions. Traf dieser Ligand auf Kupfer(II)-Ionen, bildete sich ein binukleares Komplex: zwei Kupferzentren, die durch das organische Gerüst verbunden sind. Die Forschenden stellten dieses Kupfer–Ligand-System sowohl in makroskopischer (Bulk-) als auch in nanometergroßer Form her und bestätigten seine Struktur sorgfältig mit einer Reihe gängiger Labortechniken, darunter Infrarot- und Sichtbarkeits-Spektroskopie, Kernspinresonanz, Massenspektrometrie, magnetische Messungen und thermische Analysen. Mit der Elektronenmikroskopie zeigten sie außerdem, dass die Nanoform gut definierte Partikel mit etwa 15–27 Nanometern Durchmesser bildet. 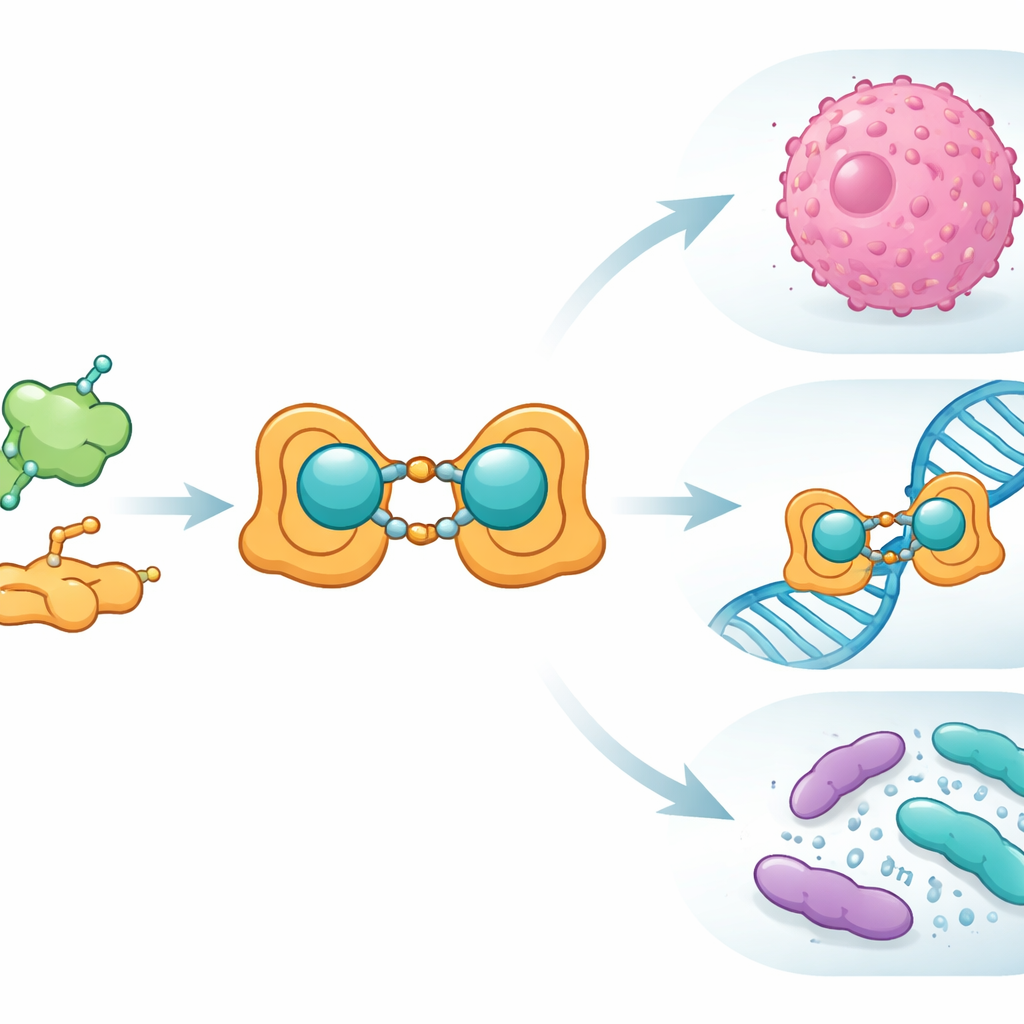
Wie sich die neue Verbindung verhält
Physikalische Messungen zeichneten ein stimmiges Bild von Form und Bindungsverhältnissen des Komplexes. Verschiebungen in den Infrarotsignalen zeigten, dass sowohl Stickstoff- als auch Sauerstoffatome der Schiff-Base-Liganden stark an Kupfer binden, während magnetische und Elektronenspin-Studien auf eine verzerrte tetraedrische Umgebung um die Metallzentren und auf starke Wechselwirkungen zwischen den beiden Kupferionen hinwiesen. Massenspektrometrie und Größenausschluss-Chromatographie deuteten darauf hin, dass der Komplex zu polymerähnlichen Ketten mit höherer Masse aggregieren kann, stabilisiert durch Wechselwirkungen benachbarter Einheiten. Zur Ergänzung dieser Experimente führten die Forschenden moderne quantenchemische Rechnungen durch, die die vorgeschlagene Geometrie und elektronische Struktur stützten. Die Rechnungen zeigten außerdem, dass durch Kupferbindung die Energieabstände zwischen den Frontier-Orbitalen deutlich schrumpfen, was auf ein reaktiveres, ladungstransferfreundlicheres System mit verstärkter optischer und elektronischer Reaktionsfähigkeit hindeutet.
Prüfung an Bakterien, DNA und Krebszellen
Mit der bekannten Struktur untersuchten die Forschenden das Verhalten des neuen Kupferkomplexes in biologischen Kontexten. In antimikrobiellen Tests gegen häufige Bakterien- und Pilzstämme zeigte der freie Ligand praktisch keine Wirkung, während der nanoskalige Kupferkomplex klare Hemmhöfe gegen krankheitsrelevante Bakterien wie Escherichia coli und Staphylococcus aureus sowie gegen die Hefe Candida albicans erzeugte. Anschließend untersuchten sie die Wechselwirkung der Verbindungen mit DNA mittels dreier Methoden: Änderungen in der Ultraviolett-Absorption, Verdrängung eines fluoreszierenden Farbstoffs, der sich zwischen DNA-Basenpaare schiebt, und Messungen der Viskosität der Lösung. Über diese Experimente hinweg band der Kupferkomplex DNA stärker als der Ligand allein und verhielt sich ähnlich wie klassische Interkalatoren, indem er die Helix leicht verlängerte und entspannt. Molekulare Docking-Simulationen, die die Moleküle rechnerisch in Proteinstrukturen von Bakterien und Pilzen einpassen, zeigten günstige Bindungstaschen und negative Interaktionsenergien, wobei auch hier der Kupferkomplex besser abschnitt als seine metallfreie Gegenform.
Erfolg gegen Brustkrebszellen
Die Forschenden testeten die neuen Moleküle anschließend an menschlichen MCF-7-Brustkrebszellen. Mit einem standardisierten Zellviabilitätstest fanden sie heraus, dass der freie, aus Folsäure abgeleitete Ligand relativ schwach ist und hohe Konzentrationen benötigt, um das Zellwachstum um die Hälfte zu reduzieren. Im Gegensatz dazu erreichte der nanoskalige Kupferkomplex dieselbe Wachstumshemmung bei deutlich niedrigeren Dosen und näherte sich damit der Wirksamkeit des Referenzchemotherapeutikums Cisplatin an, wenngleich er insgesamt weniger stark war. Das Folsäurefragment könnte helfen, den Komplex zu Krebszellen zu lenken, die Folatrezeptoren überexprimieren, während die Kupferzentren reaktive Spezies erzeugen und DNA sowie Schlüsselenzyme stören können. Theoretische Analysen der Ladungsverteilung und des elektrostatischen Potenzials unterstützten dieses Bild, indem sie bestimmte Stickstoff- und Sauerstoffatome als bevorzugte Stellen für Elektronenspende an Kupfer und an biologische Zielstrukturen identifizierten. 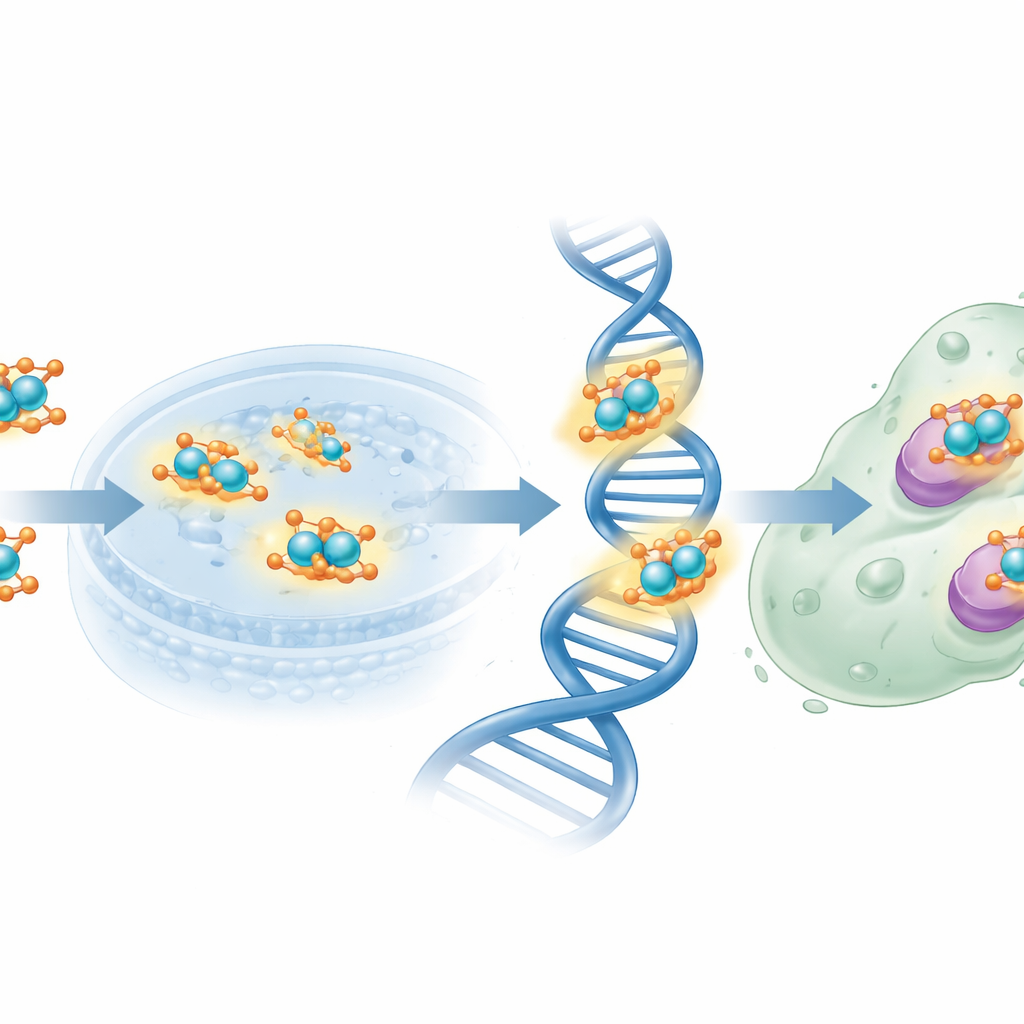
Was das für zukünftige Medikamente bedeuten könnte
Anschaulich zeigt diese Studie, dass die clevere Kombination eines Vitamin-“Adresslabels” mit einem aktiven Metallzentrum ein sonst schwaches organisches Molekül in ein vielseitiges Mittel gegen Mikroben und Krebszellen verwandeln kann. Die folsäurebasierte Schiff-Base ist für sich genommen nur mäßig aktiv, wird jedoch in Kombination mit Kupfer und in Form eines binukleären Nano-Komplexes effektiver beim Einschleusen in DNA, beim Stören bakterieller Mechanismen und beim Verlangsamen des Wachstums von Brustkrebszellen. Obwohl noch viel Arbeit nötig ist, bevor ein solcher Komplex in die Klinik gelangen könnte – insbesondere ausführliche Sicherheits- und Selektivitätsstudien –, unterstreichen die Ergebnisse eine vielversprechende Designstrategie: Nährstoffe zu nutzen, die natürlicherweise schnell wachsende Zellen ansteuern, als Gerüst für Metallkomplexe, die Krankheiten auf Ebene der DNA und essentieller Proteine angreifen können.
Zitation: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Schlüsselwörter: Kupferkomplexe, Folsäure, Schiff-Base, DNA-Bindung, Antikrebsmittel