Clear Sky Science · nl
Synthese, spectroscopisch onderzoek, karakterisering, antimicrobieel functioneren, DNA-interactie, DFT- en moleculair-dockingstudies van een nieuw Cu(II)-Schiffbasisch complex
Waarom een door een vitamine geïnspireerd metaalmedicijn ertoe doet
Veel van de huidige antibiotica en kankergeneesmiddelen verliezen hun effectiviteit, doordat microben resistent worden of doordat bijwerkingen de toegestane dosering beperken. Deze studie onderzoekt een inventieve aanpak: het bouwen van een nieuw koperhoudend verbinding uit folinezuur—de bekende vitamine B9—en het testen of dit op maat gemaakte molecuul bacteriën kan aanvallen, zich aan DNA kan hechten en de groei van borstkankercellen kan vertragen. Door een voedingsstof die van nature snel delende cellen opspoort te combineren met een biologisch actief metaal, streven de onderzoekers ernaar een slimmer en veelzijdiger therapeutisch middel te ontwikkelen.
Een veelvoorkomende vitamine omzetten in een aangepast instrument
Het team begon met folinezuur, een vitamine die onze cellen gebruiken voor DNA-opbouw en -herstel en die kankercellen vaak hamsteren. Ze koppelden folinezuur chemisch aan salicylaldehyde, een eenvoudige aromatische verbinding, om een nieuwe "Schiff-base" ligand te vormen—in wezen een op maat gemaakte haak om een metaalion vast te pakken. Wanneer dit ligand in contact kwam met koper(II)-ionen, ontstond een binucleair complex: twee kopercentra verbonden door het organische geraamte. De wetenschappers bereidden dit koper–ligand systeem zowel in bulk- als in nanometerschaal en bevestigden de structuur zorgvuldig met een reeks standaard laboratoriumtechnieken, waaronder infrarood- en zichtbaarlichtspektroscopie, kernspinresonantie, massaspectrometrie, magnetische metingen en thermische analyse. Ze gebruikten ook elektronenmicroscopie om aan te tonen dat de nano‑versie goed gedefinieerde deeltjes vormt van circa 15–27 nanometer. 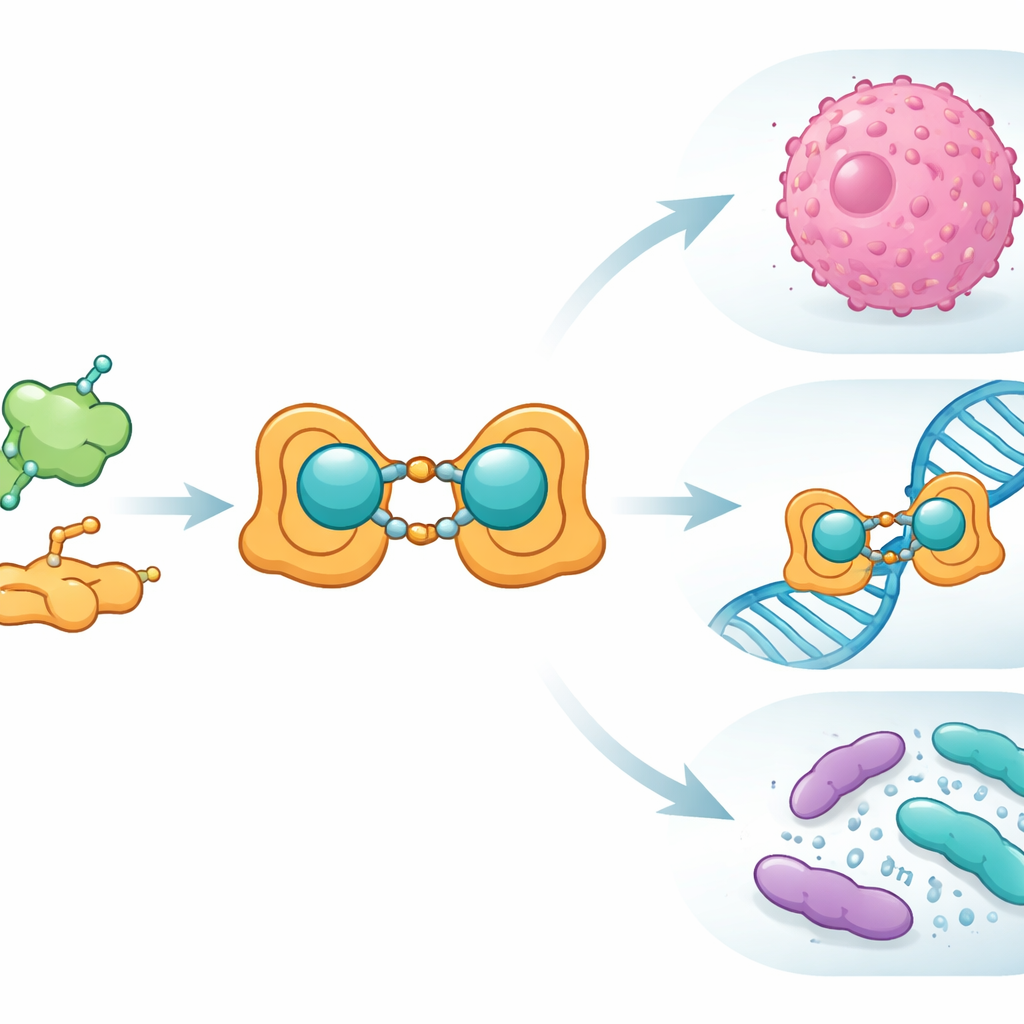
Hoe de nieuwe verbinding zich gedraagt
Fysische metingen gaven een consistent beeld van de vorm en de bindingen in het complex. Verschuivingen in de infraroodsignalen toonden dat zowel stikstof- als zuurstofatomen van het Schiff-base ligand sterk aan koper binden, terwijl magnetische en elektronspinstudies wezen op een vervormde tetraëdrische omgeving rond de metaalcentra en sterke interactie tussen de twee kopereenheden. Massaspectrometrie en gelaatschromatografie suggereerden dat het complex kan samenklonteren tot hogere-massa-polymeerachtige ketens, gestabiliseerd door wisselwerkingen tussen aangrenzende eenheden. Ter ondersteuning van deze experimenten voerden de onderzoekers moderne kwantumchemische berekeningen uit, die de voorgestelde geometrie en elektronische structuur bevestigden. De berekeningen toonden ook dat zodra koper is gebonden, de energiekloof tussen de grensorbitale van de verbinding sterk verkleint, wat duidt op een reactiever systeem met verbeterde ladingsoverdracht en grotere optische en elektronische responsiviteit.
Bacteriën, DNA en kankercellen aan de tand gevoeld
Met de structuur vastgesteld onderzocht het team hoe het nieuwe kopercomplex zich in biologische omstandigheden gedraagt. In antimicrobiële tests tegen veelvoorkomende bacteriële en schimmelstammen leverde het vrije ligand op zichzelf vrijwel geen activiteit, maar het nanoschaal kopercomplex veroorzaakte duidelijke remzones voor ziekteverwekkende bacteriën zoals Escherichia coli en Staphylococcus aureus, en voor de gist Candida albicans. Vervolgens onderzochten ze de interactie met DNA met drie methoden: veranderingen in ultravioletlichtabsorptie, verdringing van een fluorescente kleurstof die zich tussen DNA-basen nestelt, en metingen van de viscositeit van oplossingen. In al deze experimenten bond het kopercomplex sterker aan DNA dan het ligand alleen en gedroeg het zich veelal als klassieke intercalatoren die tussen basen schuiven, waardoor de helix licht verlengd en ontwonden wordt. Moleculaire-docking-simulaties, waarin de moleculen computationeel in eiwitstructuren van bacteriën en schimmels werden geplaatst, toonden gunstige bindingspockets en negatieve interactie-energieën, opnieuw met het kopercomplex dat betere prestaties leverde dan zijn metalenvrije tegenhanger.
Belofte tegen borstkankercellen
De onderzoekers stelden daarna menselijke MCF-7 borstkankercellen bloot aan de nieuwe verbindingen. Met een standaard test voor celviabiliteit vonden ze dat het vrije, uit folaat afgeleide ligand relatief zwak was en hoge concentraties nodig had om de celgroei met de helft te verminderen. Daarentegen bereikte het nanoschaal kopercomplex hetzelfde remmingsniveau bij veel lagere doseringen, in de buurt van de werkzaamheid van het referentiechemotherapie-middel cisplatine, hoewel het in het totaal nog minder krachtig bleef. Het folinezuurfragment kan helpen het complex naar kankercellen te sturen die folaatreceptoren overexpressen, terwijl de kopercentra reactieve speciën kunnen genereren en DNA en sleutelenzymen kunnen verstoren. Theoretische analyses van ladingsverdeling en elektrostatische potentiaal ondersteunden dit beeld door specifieke stikstof- en zuurstofatomen te identificeren als voorkeursplaatsen voor elektrondonatie aan koper en aan biologische doelwitten. 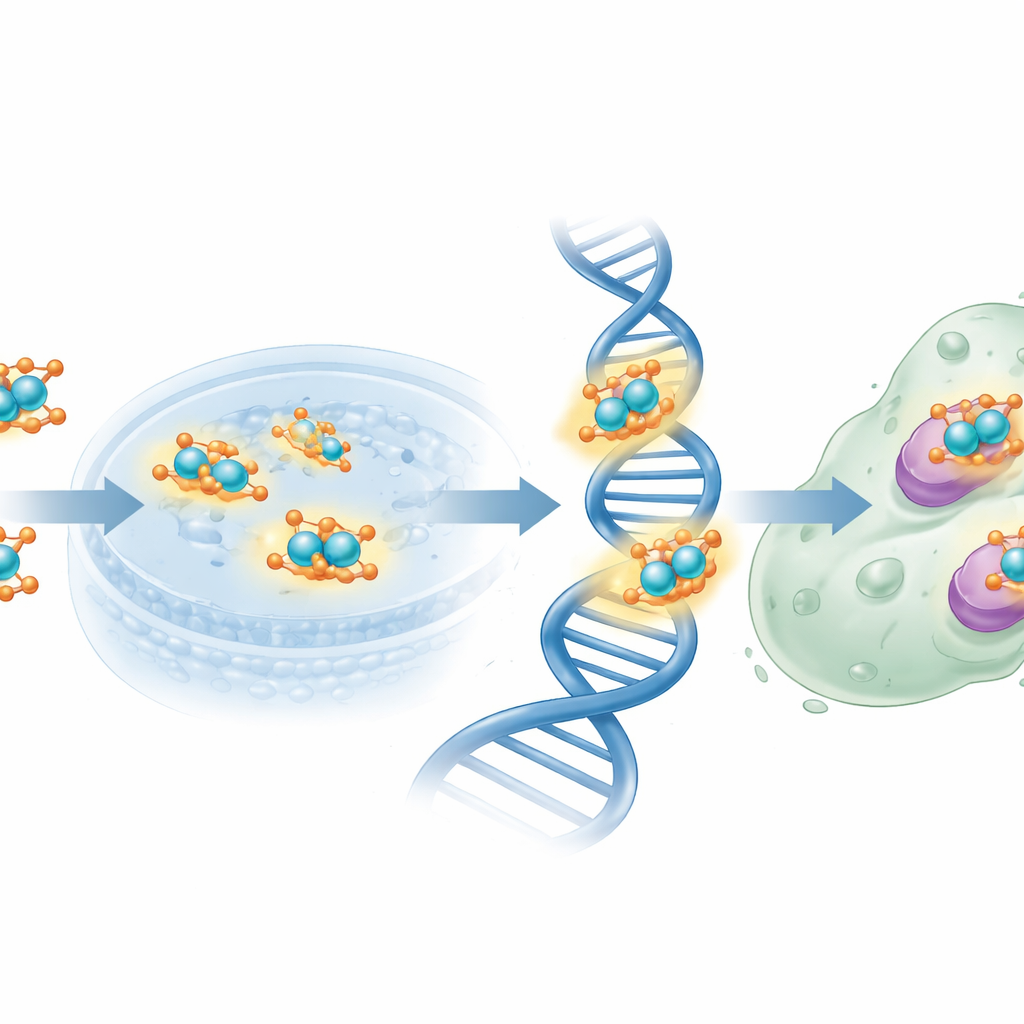
Wat dit kan betekenen voor toekomstige geneesmiddelen
Concreet laat deze studie zien dat het slim combineren van een vitamine-"adreslabel" met een actief metaalcentrum een anders zwak organisch molecuul kan transformeren tot een veelzijdig wapen tegen microben en kankercellen. De folinezuurgebaseerde Schiff-base is op zichzelf matig actief, maar wanneer die wordt gekoppeld aan koper en gevormd tot een binucleair, nanoschaalcomplex, wordt hij beter in het binnendringen van DNA, het verstoren van bacteriële processen en het vertragen van de groei van borstkankercellen. Hoewel er nog veel werk nodig is voordat zo’n verbinding klinisch haalbaar is—met name gedetailleerde veiligheid- en selectiviteitsstudies—benadrukken de resultaten een veelbelovende ontwerprichting: gebruik voedingsstoffen die van nature snelgroeiende cellen aantrekken als draagstructuren voor metaalcomplexen die ziekte op het niveau van DNA en essentiële eiwitten kunnen bestrijden.
Bronvermelding: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Trefwoorden: kopercomplexen, folinezuur, Schiff-base, DNA-binding, antikankermiddelen