Clear Sky Science · es
Síntesis, espectroscopía, caracterización, actividad antimicrobiana, interacción con ADN, estudios DFT y de acoplamiento molecular de un nuevo complejo de Cu(II)-Schiff
Por qué importa un fármaco metálico inspirado en una vitamina
Muchos de los antibióticos y fármacos contra el cáncer actuales están perdiendo eficacia, ya sea porque los microbios desarrollan resistencia o porque los efectos secundarios limitan la dosis tolerable por los pacientes. Este estudio explora un enfoque ingenioso: construir un nuevo compuesto a base de cobre a partir del ácido fólico —la conocida vitamina B9— y probar si esta molécula diseñada puede atacar bacterias, unirse al ADN y frenar el crecimiento de células de cáncer de mama. Al combinar un nutriente que busca naturalmente células de rápida proliferación con un metal biológicamente activo, los investigadores pretenden crear una herramienta terapéutica más inteligente y versátil.
Convertir una vitamina común en una herramienta a medida
El equipo partió del ácido fólico, una vitamina que nuestras células usan para sintetizar y reparar ADN y que las células cancerosas a menudo acumulan. Ligaron químicamente el ácido fólico con salicilaldehído, un compuesto aromático simple, para formar una nueva ligando tipo «base de Schiff», esencialmente un gancho diseñado para captar un ión metálico. Cuando este ligando se encontró con iones Cu(II), formó un complejo binuclear: dos centros de cobre unidos por el armazón orgánico. Los científicos prepararon este sistema cobre–ligando tanto en forma convencional (a granel) como en forma nanométrica y confirmaron cuidadosamente su estructura usando una batería de técnicas estándar de laboratorio, incluidas espectroscopía en el infrarrojo y en el visible, resonancia magnética nuclear, espectrometría de masas, medidas magnéticas y análisis térmico. También emplearon microscopía electrónica para mostrar que la versión nano forma partículas bien definidas de alrededor de 15–27 nanómetros de tamaño. 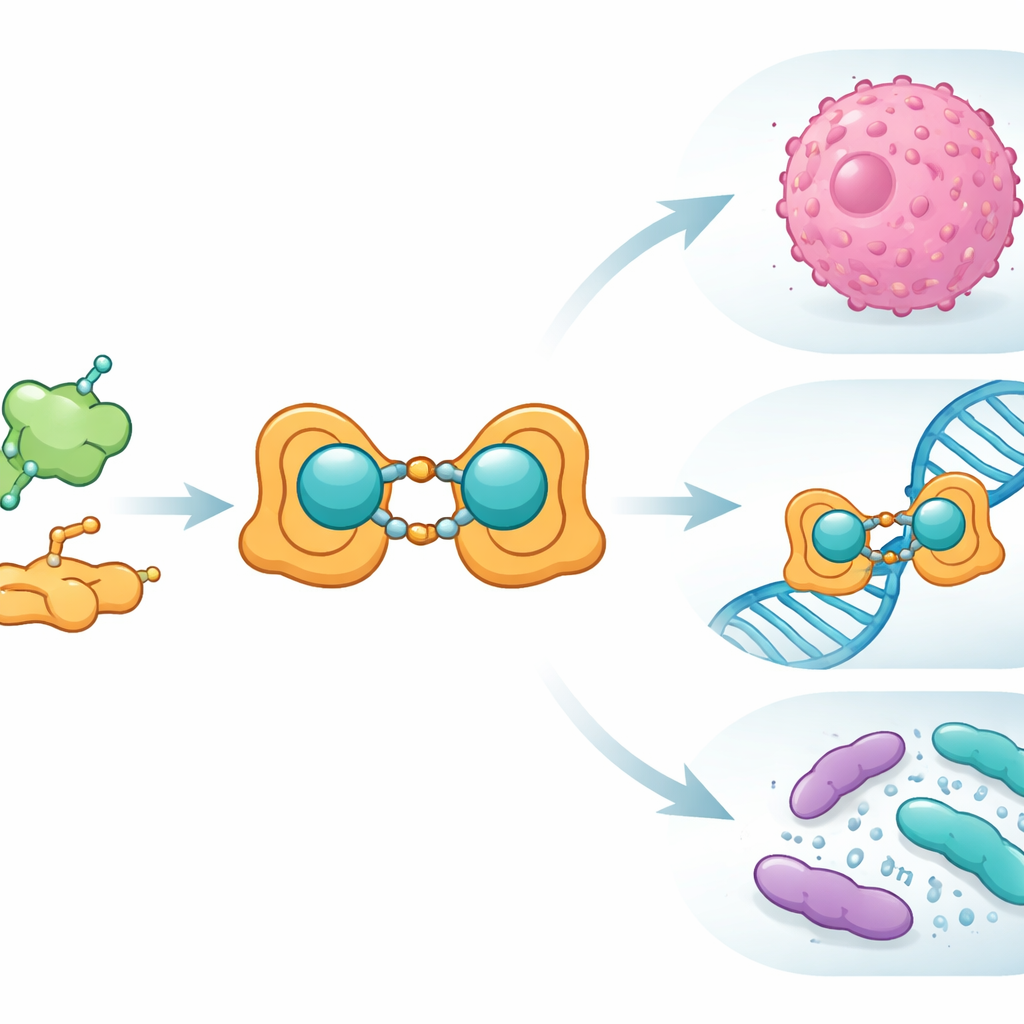
Cómo se comporta el nuevo compuesto
Las mediciones físicas dibujaron una imagen coherente de la geometría y los enlaces del compuesto. Desplazamientos en las señales infrarrojas revelaron que tanto los átomos de nitrógeno como de oxígeno del ligando tipo Schiff se enlazan fuertemente al cobre, mientras que los estudios magnéticos y de espín electrónico indicaron un entorno tetraédrico distorsionado alrededor de los centros metálicos y una interacción fuerte entre los dos iones de cobre. La espectrometría de masas y la cromatografía de exclusión por tamaño sugirieron que el complejo puede ensamblarse en cadenas poliméricas de mayor masa, estabilizadas por interacciones entre unidades vecinas. Para complementar estos experimentos, los investigadores recurrieron a cálculos moderno- químicos cuánticos, que respaldaron la geometría y la estructura electrónica propuestas. Los cálculos también mostraron que, una vez ligado el cobre, la brecha de energía entre los orbitales frontera del compuesto se reduce notablemente, lo que implica un sistema más reactivo, favorable al tránsito de carga y con mayor respuesta óptica y electrónica.
Poniendo a prueba bacterias, ADN y células cancerosas
Con la estructura caracterizada, el equipo examinó cómo se comporta el nuevo complejo de cobre en entornos biológicos. En pruebas antimicrobianas contra cepas bacterianas y fúngicas comunes, el ligando libre prácticamente no mostró actividad, pero el complejo de cobre en tamaño nano produjo claras zonas de inhibición del crecimiento para bacterias de interés clínico como Escherichia coli y Staphylococcus aureus, y para la levadura Candida albicans. A continuación investigaron cómo los compuestos interactúan con el ADN empleando tres métodos: cambios en la absorción en el ultravioleta, desplazamiento de una sonda fluorescente que se intercala entre las bases del ADN y mediciones de la viscosidad de la solución. En estos experimentos, el complejo de cobre se unió al ADN con mayor afinidad que el ligando solo y se comportó de forma similar a agentes clásicos que se intercalan entre pares de bases, alargando y desenrollando sutilmente la hélice. Las simulaciones de acoplamiento molecular, que «encajan» computacionalmente las moléculas en estructuras proteicas de bacterias y hongos, mostraron bolsillos de unión favorables y energías de interacción negativas, nuevamente con el complejo de cobre superando a su contraparte sin metal.
Potencial frente a células de cáncer de mama
Los investigadores retaron después a células humanas MCF-7 de cáncer de mama con las nuevas moléculas. Mediante una prueba estándar de viabilidad celular, hallaron que el ligando derivado del folato libre era relativamente débil, requiriendo concentraciones altas para reducir el crecimiento celular a la mitad. En contraste, el complejo de cobre en escala nanométrica logró el mismo nivel de inhibición del crecimiento a dosis mucho más bajas, acercándose a la potencia del fármaco quimioterápico de referencia cisplatino, aunque seguía siendo en conjunto menos potente. El fragmento de ácido fólico podría ayudar a dirigir el complejo hacia células cancerosas que sobreexpresan receptores del folato, mientras que los centros de cobre pueden generar especies reactivas y perturbar el ADN y enzimas clave. Los análisis teóricos de distribución de carga y potencial electrostático respaldaron este panorama al identificar átomos específicos de nitrógeno y oxígeno como sitios primarios para donar electrones al cobre y a dianas biológicas. 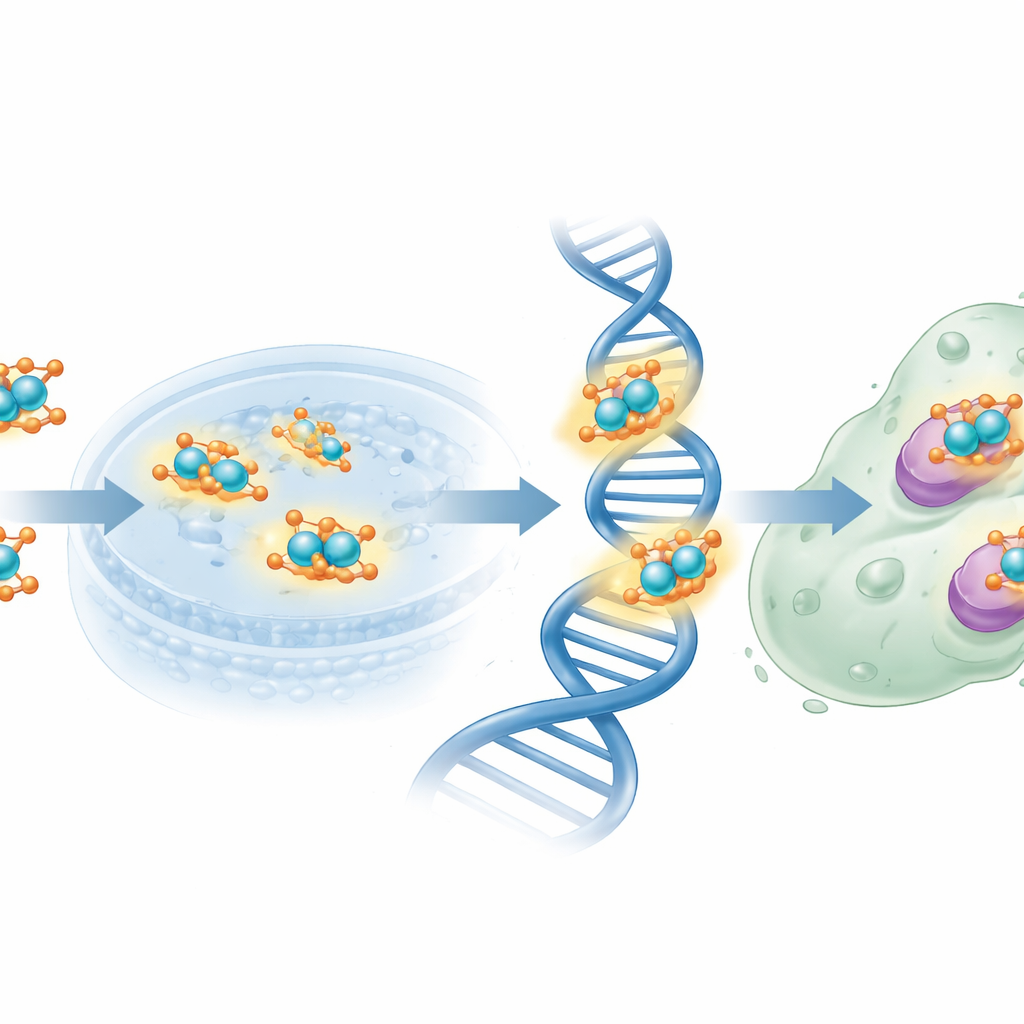
Qué podría significar esto para futuros medicamentos
En términos accesibles, este estudio muestra que combinar inteligentemente una «etiqueta de dirección» basada en una vitamina con un centro metálico activo puede transformar una molécula orgánica moderada en un arma multifacética contra microbios y células cancerosas. La base de Schiff derivada del ácido fólico por sí sola es modestamente activa, pero cuando se asocia con cobre y se configura como un complejo binuclear en escala nanométrica, mejora su capacidad para intercalarse en el ADN, alterar la maquinaria bacteriana y frenar el crecimiento de células de cáncer de mama. Aunque queda mucho trabajo antes de que un compuesto así pueda llegar a la clínica —especialmente estudios detallados de seguridad y selectividad— los resultados subrayan una estrategia de diseño prometedora: usar nutrientes que se dirigen de forma natural a células de rápido crecimiento como andamiajes para complejos metálicos capaces de atacar la enfermedad a nivel del ADN y proteínas esenciales.
Cita: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Palabras clave: complejos de cobre, ácido fólico, base de Schiff, unión al ADN, agentes anticancerígenos