Clear Sky Science · pl
Synteza, spektroskopia, charakterystyka, aktywność przeciwmikrobowa, interakcja z DNA, obliczenia DFT i badania dokowania molekularnego nowego kompleksu Cu(II)-Schiffa
Dlaczego lek metalowy inspirowany witaminą ma znaczenie
Wiele współczesnych antybiotyków i leków przeciwnowotworowych traci skuteczność — albo z powodu narastającej oporności mikroorganizmów, albo z powodu działań niepożądanych ograniczających dawki u pacjentów. W tej pracy badano pomysłowe podejście: zbudowanie nowego związku na bazie miedzi z wykorzystaniem kwasu foliowego — znanej witaminy B9 — i sprawdzenie, czy zmodyfikowana cząsteczka może zwalczać bakterie, wiązać się z DNA i hamować wzrost komórek raka piersi. Łącząc składnik odżywczy, który naturalnie tropi szybko dzielące się komórki, z aktywnym biologicznie metalem, autorzy dążą do stworzenia bardziej precyzyjnego i wszechstronnego narzędzia terapeutycznego.
Przekształcenie powszechnej witaminy w narzędzie na zamówienie
Zespół rozpoczął od kwasu foliowego, witaminy wykorzystywanej przez komórki do syntezy i naprawy DNA, którą często akumulują komórki nowotworowe. Chemicznie powiązano kwas foliowy z salicylaldehydem, prostym związkiem aromatycznym, tworząc nowy ligand typu „zasada Schiffa” — w praktyce zaprojektowany zaczep do chwytania jonów metalu. Gdy ligand zetknął się z jonami Cu(II), utworzył kompleks binuklearny: dwa centra miedzi połączone organiczną ramą. Naukowcy przygotowali ten układ zarówno w formie masowej, jak i w postaci nanometrycznej i starannie potwierdzili jego strukturę przy użyciu szeregu standardowych technik: spektroskopii w podczerwieni i widzialnej, magnetycznego rezonansu jądrowego, spektrometrii mas, pomiarów magnetycznych oraz analizy termicznej. Użyto też mikroskopii elektronowej, która wykazała, że wersja nano tworzy dobrze zdefiniowane cząstki o rozmiarach około 15–27 nanometrów. 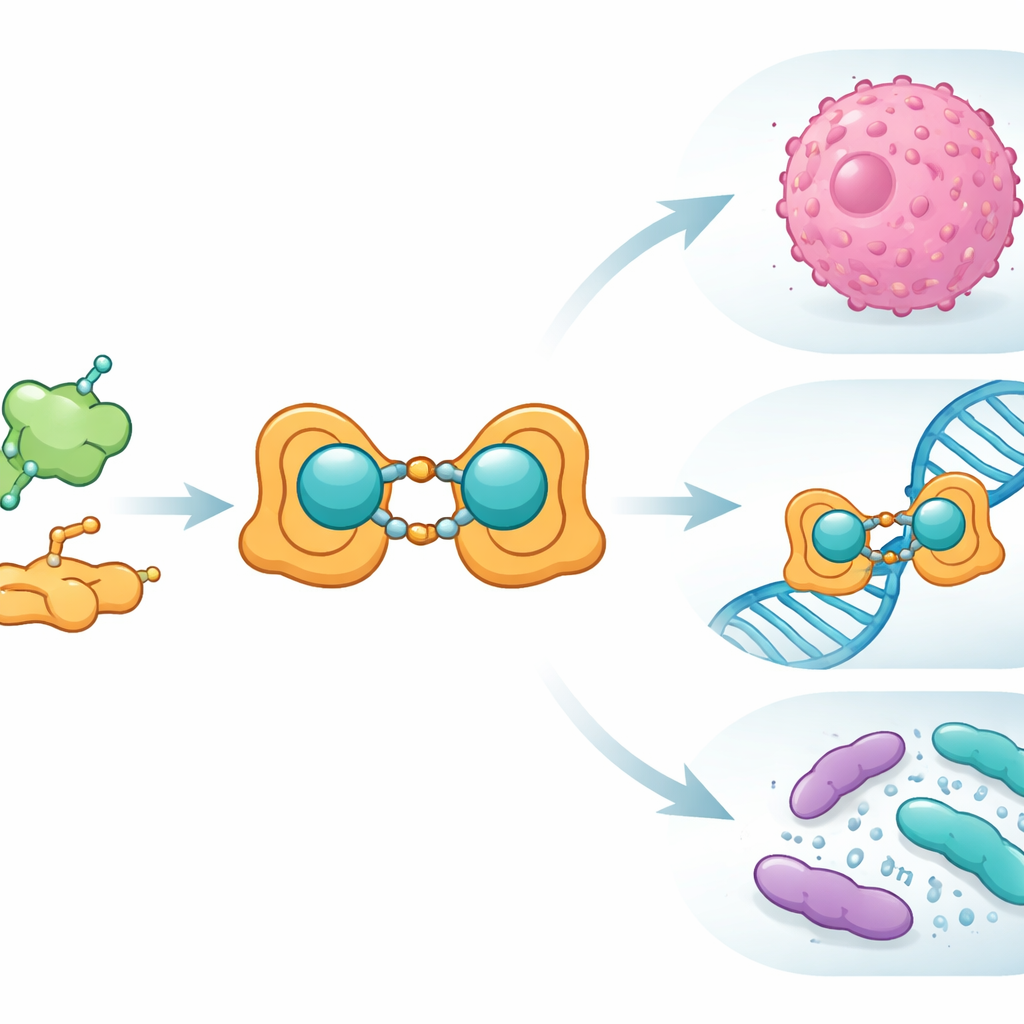
Jak zachowuje się nowy związek
Pomiarom fizycznym odpowiadał spójny obraz kształtu i wiązań związku. Przesunięcia sygnałów w widmie podczerwieni ujawniły, że zarówno atomy azotu, jak i tlenu liganda typu Schiffa silnie koordynują miedź, podczas gdy badania magnetyczne i spinowe elektronów wskazały na zdeformowane tetraedryczne otoczenie wokół centrów metalu oraz silną interakcję między dwoma jonami miedzi. Spektrometria mas i chromatografia wykluczająca sugerowały, że kompleks może się organizować w wyższej masy łańcuchy przypominające polimery, stabilizowane przez wzajemne oddziaływania między jednostkami. Aby uzupełnić te doświadczenia, autorzy sięgnęli po współczesne obliczenia kwantowo-chemiczne, które wspierały zaproponowaną geometrię i strukturę elektronową. Obliczenia wykazały również, że po związaniu miedzi zmniejsza się znacznie przerwa energetyczna między orbitami brzegowymi związku, co sugeruje bardziej reaktywny system sprzyjający transferowi ładunku oraz zwiększoną odpowiedź optyczną i elektroniczną.
Testy na bakteriach, DNA i komórkach nowotworowych
Mając strukturę, zespół sprawdził zachowanie nowego kompleksu w warunkach biologicznych. W testach przeciwbakteryjnych i przeciwgrzybiczych ligand wolny praktycznie nie wykazywał działania, natomiast nano-rozmiarowy kompleks miedzi wywoływał widoczne strefy zahamowania wzrostu dla patogennych bakterii, takich jak Escherichia coli i Staphylococcus aureus, oraz dla drożdży Candida albicans. Następnie badano interakcje z DNA trzema metodami: zmiany w absorpcji UV, wypieranie fluorescencyjnego barwnika wcinającego się między pary zasad oraz pomiary lepkości roztworu. We wszystkich tych eksperymentach kompleks miedzi wiązał się z DNA silniej niż sam ligand i zachowywał się podobnie do klasycznych czynników wsuwających się między pary zasad (interkalatorów), nieznacznie wydłużając i rozkręcając helisę. Symulacje dokowania molekularnego, które komputerowo „dopasowują” cząsteczki do struktur białkowych pochodzących od bakterii i grzybów, wykazały korzystne kieszenie wiążące i ujemne energie interakcji, także z przewagą kompleksu miedzi nad jego pozbawionym metalu odpowiednikiem.
Obiecujące wyniki wobec komórek raka piersi
Następnie badacze wystawili ludzkie komórki raka piersi linii MCF-7 na działanie nowych związków. W standardowym teście żywotności komórek stwierdzono, że wolny ligand pochodzący z folianu był stosunkowo słaby i wymagał wysokich stężeń, aby zmniejszyć wzrost komórek o połowę. Natomiast kompleks miedzi w postaci nano osiągał ten sam poziom zahamowania wzrostu przy znacznie niższych dawkach, zbliżając się do mocy działania referencyjnego leku chemioterapeutycznego, cisplatyny, choć wciąż pozostawał od niej słabszy. Fragment kwasu foliowego może ułatwiać kierowanie kompleksu ku komórkom nadekspresującym receptory folianowe, podczas gdy centra miedzi mogą generować reaktywne rodzaje tlenu i zakłócać DNA oraz kluczowe enzymy. Analizy teoretyczne rozkładu ładunku i potencjału elektrostatycznego wspierały ten obraz, identyfikując konkretne atomy azotu i tlenu jako główne miejsca oddawania elektronów do miedzi i celów biologicznych. 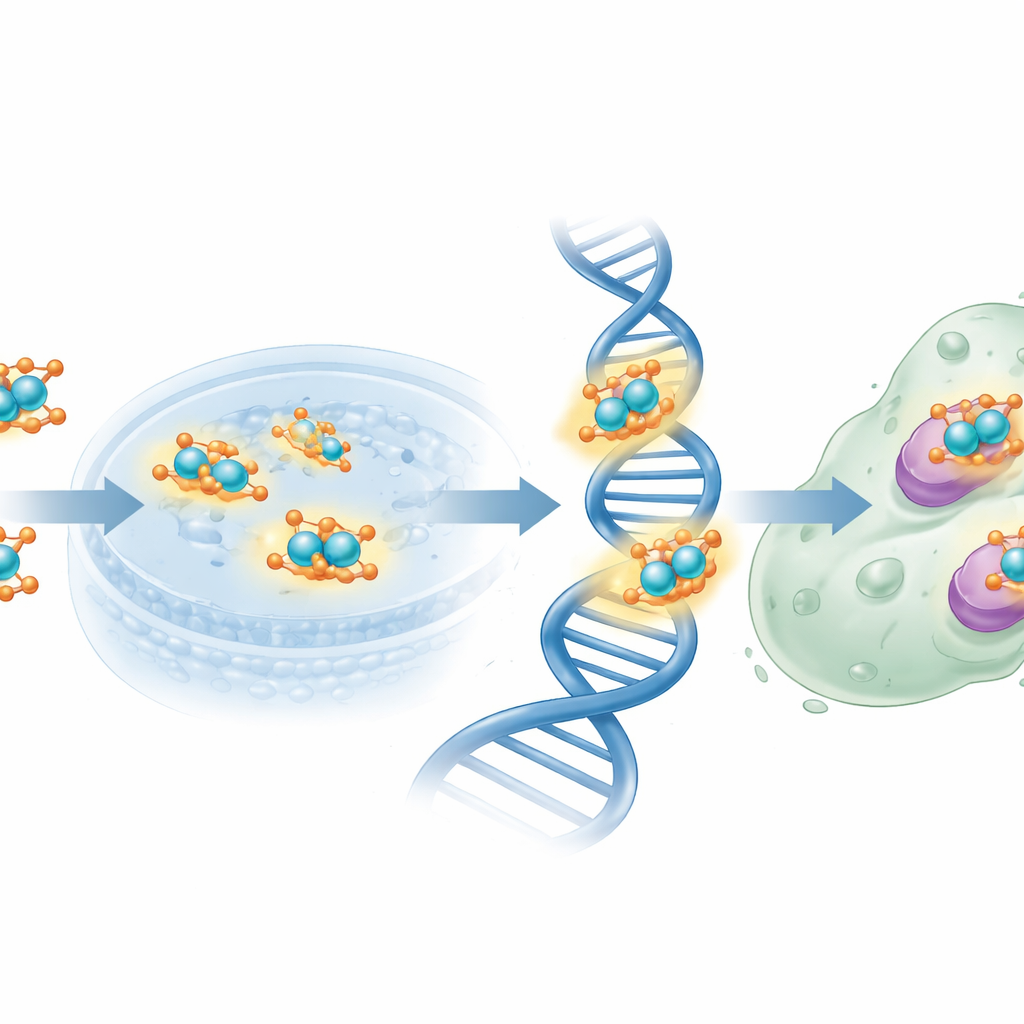
Co to może znaczyć dla przyszłych leków
Mówiąc przystępnie, badanie pokazuje, że sprytne połączenie „adresu” w postaci witaminy z aktywnym centrum metalu może przekształcić stosunkowo łagodną cząsteczkę organiczną w wielofunkcyjną broń przeciwko mikrobom i komórkom nowotworowym. Sam ligand oparty na kwasie foliowym ma umiarkowaną aktywność, ale w połączeniu z miedzią i uformowany w kompleks binuklearny o nanometrycznych rozmiarach staje się lepszy w wnikaniu w DNA, zaburzaniu mechanizmów bakteryjnych i spowalnianiu wzrostu komórek raka piersi. Choć przed ewentualnym wprowadzeniem takiego związku do praktyki klinicznej czeka jeszcze wiele pracy — zwłaszcza szczegółowe badania bezpieczeństwa i selektywności — wyniki podkreślają obiecującą strategię projektową: wykorzystać składniki odżywcze, które naturalnie trafiają do szybko rosnących komórek, jako rusztowania dla kompleksów metalicznych atakujących chorobę na poziomie DNA i niezbędnych białek.
Cytowanie: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Słowa kluczowe: kompleksy miedzi, kwas foliowy, zasada Schiffa, wiążenie DNA, środki przeciwnowotworowe