Clear Sky Science · fr
Synthèse, spectroscopie, caractérisation, activité antimicrobienne, interaction avec l’ADN, études DFT et de docking moléculaire d’un nouveau complexe Cu(II)-Schiff base
Pourquoi un médicament métallique inspiré d’une vitamine a de l’importance
Beaucoup des antibiotiques et des médicaments anticancéreux actuels perdent de leur efficacité, soit parce que les microbes deviennent résistants, soit parce que les effets secondaires limitent les doses tolérables par les patients. Cette étude explore une approche inventive : concevoir un nouveau composé à base de cuivre à partir de l’acide folique — la vitamine familière B9 — et tester si cette molécule sur mesure peut attaquer des bactéries, se lier à l’ADN et ralentir la croissance de cellules du cancer du sein. En combinant un nutriment qui cible naturellement les cellules à division rapide avec un métal biologiquement actif, les chercheurs visent à créer un outil thérapeutique plus intelligent et polyvalent.
Transformer une vitamine courante en un outil personnalisé
L’équipe a commencé par l’acide folique, une vitamine utilisée par nos cellules pour la synthèse et la réparation de l’ADN et que les cellules cancéreuses accumulent souvent. Ils ont lié chimiquement l’acide folique au salicylaldéhyde, un composé aromatique simple, pour former un nouveau ligand de type « base de Schiff » — essentiellement un crochet conçu pour saisir un ion métallique. Quand ce ligand a rencontré des ions Cu(II), il a formé un complexe binucléaire : deux centres de cuivre reliés par l’armature organique. Les scientifiques ont préparé ce système cuivre–ligand en formes macroscopique et nanométrique et ont confirmé sa structure à l’aide d’un ensemble de techniques de laboratoire standard, incluant la spectroscopie infrarouge et visible, la résonance magnétique nucléaire, la spectrométrie de masse, des mesures magnétiques et l’analyse thermique. Ils ont également utilisé la microscopie électronique pour montrer que la version nano forme des particules bien définies d’environ 15–27 nanomètres. 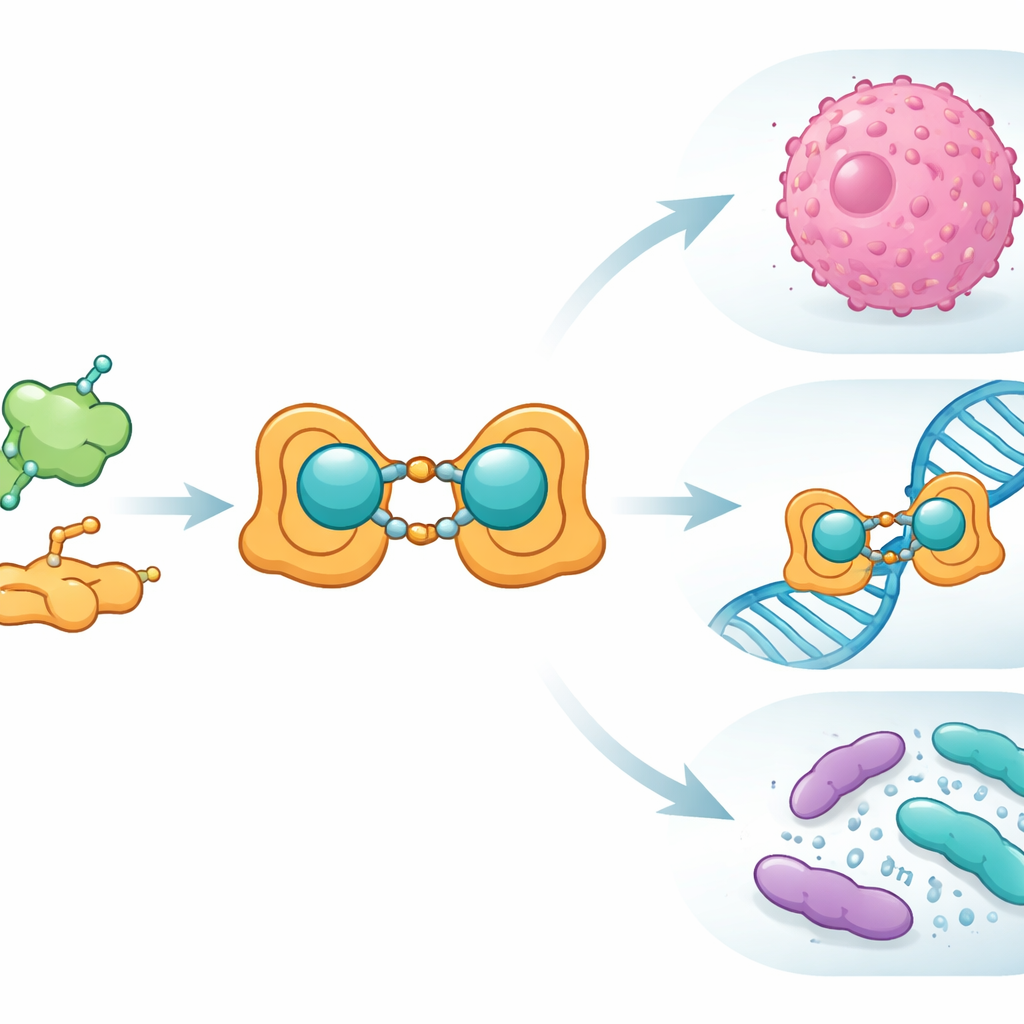
Comportement du nouveau composé
Les mesures physiques ont dressé un tableau cohérent de la géométrie et des liaisons du composé. Des décalages dans les signaux infrarouges ont révélé que les atomes d’azote et d’oxygène de la base de Schiff se lient fortement au cuivre, tandis que des études magnétiques et de spin électronique ont indiqué un environnement déformé autour des centres métalliques et une interaction forte entre les deux ions cuivre. La spectrométrie de masse et la chromatographie d’exclusion de taille ont suggéré que le complexe peut s’assembler en chaînes de masse plus élevée de type polymérique, stabilisées par des interactions entre unités voisines. Pour compléter ces expériences, les chercheurs ont eu recours à des calculs quantico-chimiques modernes, qui ont soutenu la géométrie et la structure électronique proposées. Les calculs ont aussi montré qu’une fois le cuivre lié, l’écart d’énergie entre les orbitales frontalières du composé diminue sensiblement, ce qui implique un système plus réactif, favorable aux transferts de charge et présentant une réponse optique et électronique amplifiée.
Mettre à l’épreuve bactéries, ADN et cellules cancéreuses
Avec la structure établie, l’équipe a examiné le comportement du nouveau complexe de cuivre en milieu biologique. Lors de tests antimicrobiens contre des souches bactériennes et fongiques courantes, le ligand libre n’a pratiquement rien produit, mais le complexe de cuivre nanométrique a généré des zones nettes d’inhibition de croissance pour des bactéries pathogènes telles que Escherichia coli et Staphylococcus aureus, ainsi que pour la levure Candida albicans. Ensuite, ils ont étudié l’interaction des composés avec l’ADN en utilisant trois méthodes : les variations d’absorption dans l’ultraviolet, le déplacement d’un colorant fluorescent qui s’insère entre les paires de bases, et des mesures de viscosité en solution. Dans ces expériences, le complexe de cuivre se liait à l’ADN plus fortement que le ligand seul et se comportait comme des agents classiques qui s’intercalent entre les paires de bases, allongeant et déroulant subtilement l’hélice. Des simulations de docking moléculaire, qui « ajustent » computationnellement les molécules dans des structures protéiques issues de bactéries et de champignons, ont montré des poches de liaison favorables et des énergies d’interaction négatives, le complexe de cuivre surpassant à nouveau son homologue sans métal.
Des promesses contre les cellules du cancer du sein
Les chercheurs ont ensuite confronté des cellules humaines MCF-7 du cancer du sein aux nouvelles molécules. À l’aide d’un test standard de viabilité cellulaire, ils ont constaté que le ligand dérivé du folate libre était relativement faible, nécessitant des concentrations élevées pour réduire de moitié la croissance cellulaire. En revanche, le complexe de cuivre à l’échelle nanométrique obtenait le même niveau d’inhibition de la croissance à des doses beaucoup plus faibles, approchant la puissance du médicament de référence cisplatine, bien qu’il reste globalement moins puissant. Le fragment d’acide folique pourrait aider à orienter le complexe vers les cellules cancéreuses surexprimant les récepteurs du folate, tandis que les centres cuivre peuvent générer des espèces réactives et perturber l’ADN et des enzymes clés. Des analyses théoriques de la distribution de charge et du potentiel électrostatique ont corroboré ce tableau en identifiant des atomes d’azote et d’oxygène spécifiques comme sites privilégiés de donation d’électrons vers le cuivre et vers des cibles biologiques. 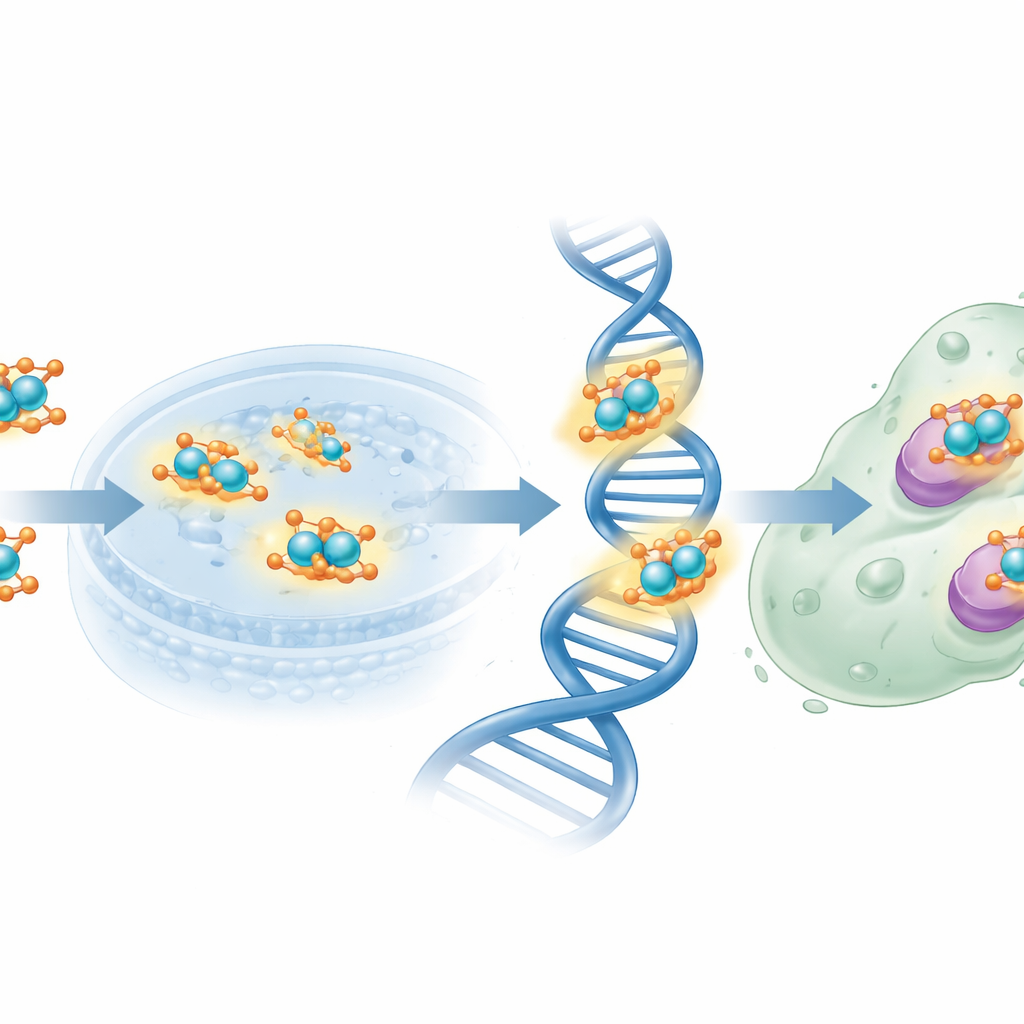
Ce que cela pourrait signifier pour les médicaments futurs
En termes accessibles, cette étude montre que combiner astucieusement une « adresse » vitaminée avec un centre métallique actif peut transformer une molécule organique par ailleurs modérée en une arme multifonction contre les microbes et les cellules cancéreuses. La base de Schiff dérivée de l’acide folique est en elle-même modestement active, mais une fois associée au cuivre et structurée en complexe binucléaire de taille nanométrique, elle devient mieux à même de s’insérer dans l’ADN, de perturber les mécanismes bactériens et de ralentir la croissance des cellules du cancer du sein. Bien qu’il reste beaucoup de travail avant qu’un tel composé puisse atteindre la clinique — notamment des études détaillées de sécurité et de sélectivité — les résultats mettent en lumière une stratégie de conception prometteuse : utiliser des nutriments qui ciblent naturellement les cellules à croissance rapide comme échafaudages pour des complexes métalliques capables d’attaquer la maladie au niveau de l’ADN et des protéines essentielles.
Citation: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Mots-clés: complexes de cuivre, acide folique, base de Schiff, liaison à l’ADN, agents anticancéreux