Clear Sky Science · ru
Синтез, спектроскопия, характеристика, антимикробная активность, взаимодействие с ДНК, методы DFT и молекулярного докинга нового комплекса Cu(II)-шИффовой основы
Почему важен металлопрепарат, вдохновлённый витамином
Многие современные антибиотики и противораковые препараты теряют эффективность: микроорганизмы вырабатывают устойчивость, а побочные эффекты ограничивают переносимость у пациентов. В этом исследовании рассматривается оригинальный подход: создание нового медьсодержащего соединения на основе фолиевой кислоты — известного витамина B9 — и проверка того, сможет ли этот адаптированный молекулярный «инструмент» атаковать бактерии, связываться с ДНК и замедлять рост раковых клеток молочной железы. Объединяя питательное вещество, которое естественно нацеливается на быстро делящиеся клетки, с биологически активным металлом, исследователи стремятся получить более умное и универсальное терапевтическое средство.
Преобразование привычного витамина в специализированный инструмент
Команда начала с фолиевой кислоты — витамина, который клетки используют для синтеза и восстановления ДНК и который часто аккумулируется в раковых клетках. Они химически связали фолиевую кислоту с салицилальдегидом, простым ароматическим соединением, чтобы получить новую лигандную «шИффову основу» — по сути, специально разработанный «крючок» для захвата иона металла. При взаимодействии этого лиганда с ионами Cu(II) образовывался бинуклеарный комплекс: две медные центры, соединённые органической матрицей. Учёные приготовили эту систему медь–лиганд как в крупномасштабной (большой) форме, так и в наномасштабной, и тщательно подтвердили её структуру с помощью набора стандартных лабораторных методов, включая инфракрасную и видимую спектроскопию, ядерный магнитный резонанс, масс-спектрометрию, магнитные измерения и термический анализ. Также использовали электронную микроскопию, показавшую, что нано-версия образует чётко определённые частицы размером примерно 15–27 нанометров. 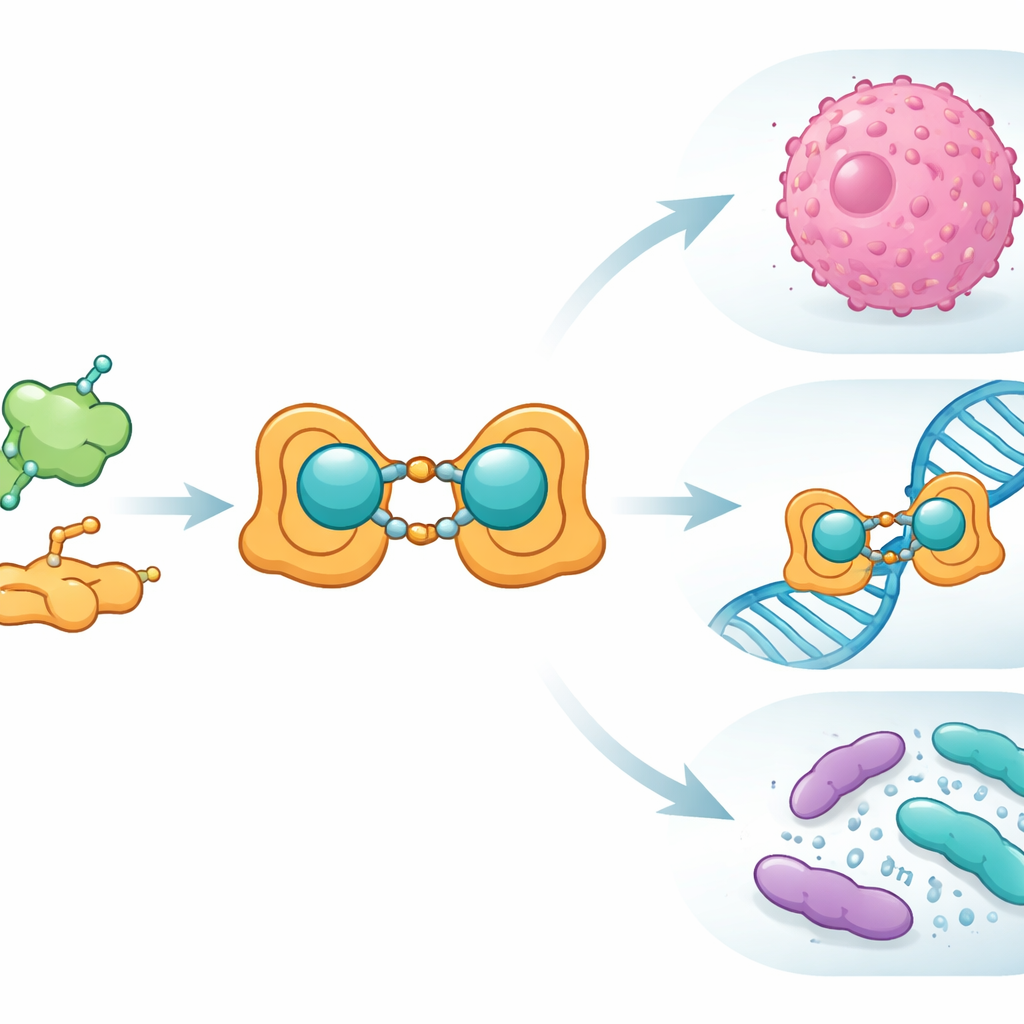
Как ведёт себя новый комплекс
Физические измерения дали согласованную картину формы и связей соединения. Сдвиги в инфракрасных сигналах указывали на сильное связывание как атомов азота, так и кислорода лиганда со медью, тогда как магнитные и электронно-спиновые исследования показывали искажённую тетраэдрическую среду вокруг металлических центров и сильное взаимодействие между двумя ионами меди. Данные масс-спектрометрии и хроматографии по размеру предполагали, что комплекс может собираться в цепочки с более высокой молекулярной массой, стабилизируемые взаимодействиями между соседними звеньями. В дополнение к экспериментам исследователи обратились к современным квантово-химическим расчётам, которые поддержали предложенную геометрию и электронную структуру. Расчёты также показали, что после связывания меди энергетический зазор между фронтирными орбиталями заметно уменьшается, что подразумевает более реакционноспособную систему, благоприятную для переноса заряда и обладающую усиленной оптической и электронной откликаемостью.
Проверка на бактериях, ДНК и раковых клетках
Имея структуру, команда изучила поведение нового медного комплекса в биологических условиях. В антимикробных тестах против распространённых бактериальных и грибковых штаммов свободный лиганд по сути не проявлял активности, тогда как нано-размерный медный комплекс образовывал чёткие зоны подавления роста для болезнетворных бактерий, таких как Escherichia coli и Staphylococcus aureus, а также для дрожжей Candida albicans. Далее они изучали взаимодействие соединений с ДНК тремя методами: изменения в УФ-поглощении, вытеснение флуоресцентного красителя, вклинивающегося между основаниями ДНК, и измерения вязкости раствора. Во всех этих экспериментах медный комплекс связывался с ДНК сильнее, чем сам лиганд, и вел себя подобно классическим интеркалирующим агентам, частично удлиняя и разворачивая спираль. Молекулярный докинг, моделирующий «встраивание» молекул в белковые структуры бактерий и грибов, показал благоприятные карманы связывания и отрицательные энергии взаимодействия, причём медный комплекс снова превосходил неметаллический аналог.
Перспективы против клеток рака молочной железы
Затем исследователи подвергли испытанию на линии человеческих раковых клеток молочной железы MCF-7 новые молекулы. По стандартному тесту жизнеспособности клеток выяснилось, что свободный производный от фолата лиганд относительно слаб, требуя высоких концентраций для снижения роста на 50 %. В отличие от него наноразмерный медный комплекс достиг того же уровня ингибирования при значительно меньших дозах, приближаясь по эффективности к эталонному химиотерапевтическому препарату цисплатину, хотя в целом оставался менее мощным. Фрагмент фолиевой кислоты может способствовать направлению комплекса к раковым клеткам, которые сверхэкспрессируют фолатные рецепторы, тогда как медные центры способны генерировать реактивные виды и нарушать ДНК и ключевые ферменты. Теоретический анализ распределения заряда и электростатического потенциала поддержал эту картину, выявив конкретные атомы азота и кислорода как основные сайты для отдачи электронов меди и биологическим мишеням. 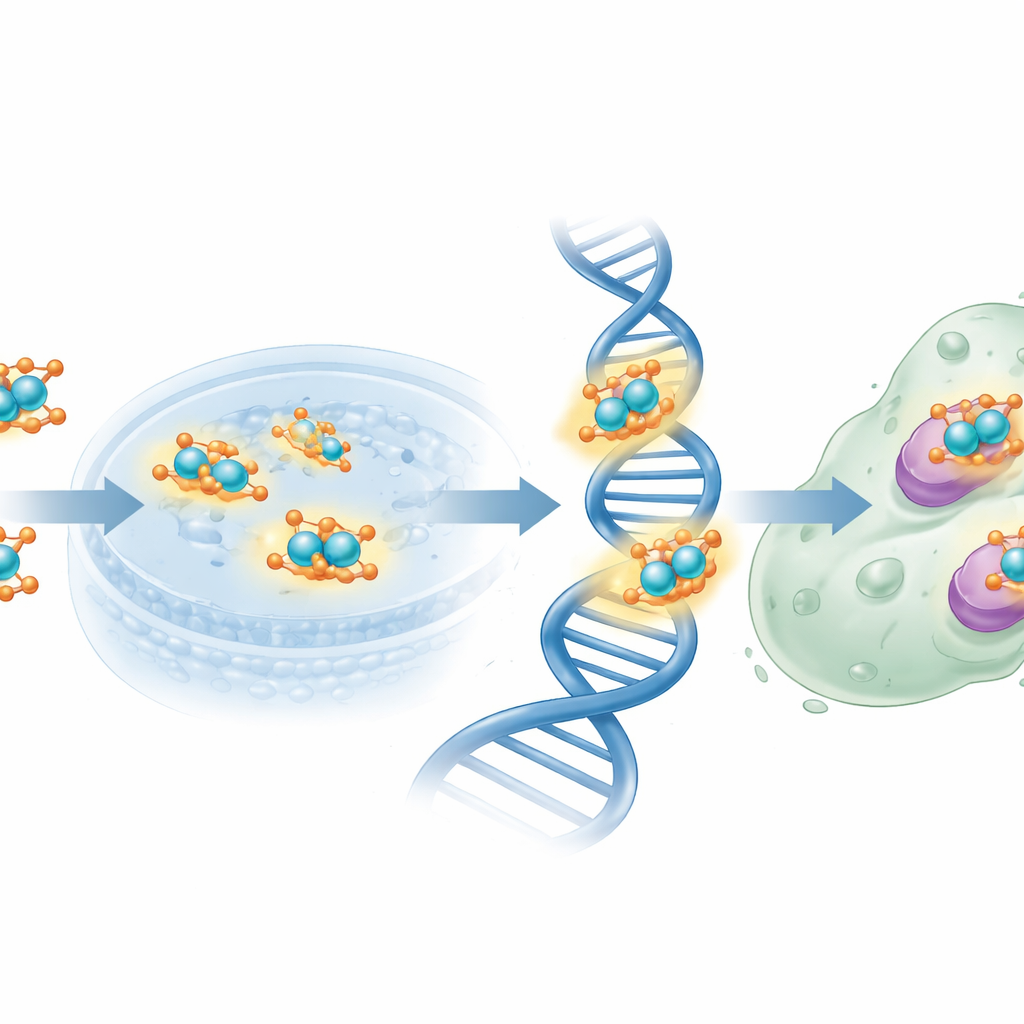
Что это может означать для будущих лекарств
Проще говоря, исследование демонстрирует, что продуманное сочетание «адресной метки» в виде витамина и активного металлического центра может превратить в целом слабоактивную органическую молекулу в многофункциональное средство против микроорганизмов и раковых клеток. Сама по себе фолиево-кислотная шИффова основа проявляет умеренную активность, но в комбинации с медью и в форме бинуклеарного нанокомплекса она лучше внедряется в ДНК, нарушает бактериальные механизмы и замедляет рост клеток рака молочной железы. Хотя до возможного клинического применения остаётся много работы — прежде всего детальные исследования безопасности и селективности — результаты подчеркивают перспективную стратегию проектирования: использовать питательные вещества, естественно нацеливающиеся на быстро растущие клетки, как каркас для металлических комплексов, атакующих болезнь на уровне ДНК и важных белков.
Цитирование: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Ключевые слова: медные комплексы, фолиевая кислота, шИффова основа, связывание с ДНК, противораковые агенты