Clear Sky Science · pt
Síntese, estudos espectroscópicos, caracterização, antimicrobiano, interação com DNA, DFT e docking molecular de um novo complexo de Cu(II)-base de Schiff
Por que um fármaco inspirado em uma vitamina importa
Muitos dos antibióticos e fármacos contra o câncer usados hoje estão perdendo eficácia, seja pela resistência microbiana ou por efeitos colaterais que limitam a dose tolerável pelos pacientes. Este estudo explora uma abordagem inventiva: construir um novo composto à base de cobre a partir do ácido fólico — a conhecida vitamina B9 — e testar se essa molécula projetada pode atacar bactérias, ligar‑se ao DNA e frear o crescimento de células de câncer de mama. Ao combinar um nutriente que naturalmente se direciona a células de rápida divisão com um metal biologicamente ativo, os pesquisadores buscam criar uma ferramenta terapêutica mais inteligente e versátil.
Transformando uma vitamina comum em uma ferramenta sob medida
A equipe partiu do ácido fólico, uma vitamina que nossas células usam na síntese e reparo do DNA e que células cancerosas frequentemente acumulam. Eles ligaram quimicamente o ácido fólico à salicilaldeído, um composto aromático simples, para formar uma nova ligante do tipo "base de Schiff" — essencialmente um gancho projetado para capturar um íon metálico. Quando esse ligante encontrou íons Cu(II), formou um complexo binuclear: dois centros de cobre ligados pela estrutura orgânica. Os cientistas prepararam esse sistema cobre–ligante tanto em forma convencional (bulk) quanto em escala nanométrica e confirmaram cuidadosamente sua estrutura usando um conjunto de técnicas laboratoriais padrão, incluindo espectroscopia no infravermelho e no visível, ressonância magnética nuclear, espectrometria de massa, medidas magnéticas e análise térmica. Também utilizaram microscopia eletrônica para mostrar que a versão nano forma partículas bem definidas na faixa de 15–27 nanômetros. 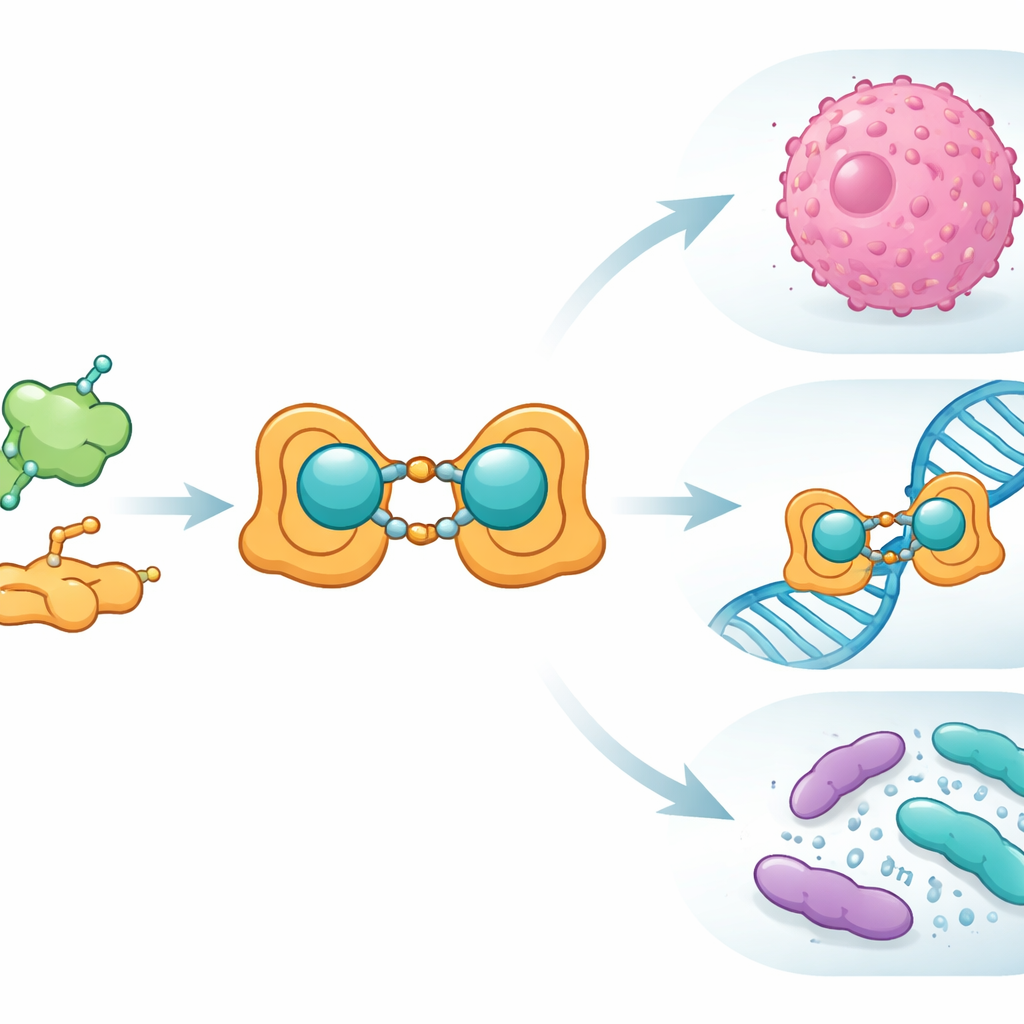
Como o novo composto se comporta
As medições físicas traçaram um quadro consistente da geometria e das ligações do composto. Deslocamentos nos sinais do infravermelho revelaram que tanto os átomos de nitrogênio quanto os de oxigênio do ligante base de Schiff se ligam fortemente ao cobre, enquanto estudos magnéticos e de spin eletrônico indicaram um ambiente distorcido ao redor dos centros metálicos e forte interação entre os dois íons de cobre. A espectrometria de massa e a cromatografia por exclusão de tamanho sugeriram que o complexo pode se montar em cadeias poliméricas de massa mais elevada, estabilizadas por interações entre unidades vizinhas. Para complementar esses experimentos, os pesquisadores recorreram a cálculos quântico‑químicos modernos, que apoiaram a geometria e a estrutura eletrônica propostas. Os cálculos também mostraram que, uma vez que o cobre está ligado, a lacuna de energia entre os orbitais de fronteira do composto se reduz marcadamente, implicando um sistema mais reativo e favorável à transferência de carga, com resposta óptica e eletrônica aumentada.
Testando contra bactérias, DNA e células cancerosas
Com a estrutura em mãos, a equipe examinou como o novo complexo de cobre se comporta em contextos biológicos. Em testes antimicrobianos contra cepas bacterianas e fúngicas comuns, o ligante livre praticamente não apresentou efeito, mas o complexo de cobre em escala nanométrica produziu claros halos de inibição para bactérias associadas a doenças, como Escherichia coli e Staphylococcus aureus, e para a levedura Candida albicans. Em seguida, investigaram a interação dos compostos com DNA por meio de três métodos: mudanças na absorção no ultravioleta, deslocamento de um corante fluorescente que se intercala entre pares de bases do DNA e medições de viscosidade da solução. Em todos esses experimentos, o complexo de cobre ligou‑se ao DNA mais fortemente que o ligante isolado e comportou‑se de forma semelhante a agentes clássicos que se enredam entre pares de bases, alongando e desenrolando sutilmente a hélice. Simulações de docking molecular, que “encaixam” computacionalmente as moléculas em estruturas proteicas de bactérias e fungos, mostraram bolsões de ligação favoráveis e energias de interação negativas, novamente com o complexo de cobre superando seu equivalente sem metal.
Potencial contra células de câncer de mama
Os pesquisadores então desafiaram células humanas de câncer de mama MCF‑7 com as novas moléculas. Usando um teste padrão de viabilidade celular, verificaram que o ligante derivado do folato isolado era relativamente fraco, exigindo concentrações elevadas para reduzir à metade o crescimento celular. Em contraste, o complexo de cobre em escala nanométrica alcançou o mesmo nível de inibição do crescimento em doses muito menores, aproximando‑se da potência do medicamento de referência cisplatina, embora ainda menos potente no conjunto. O fragmento de ácido fólico pode ajudar a direcionar o complexo a células cancerosas que superexpressam receptores de folato, enquanto os centros de cobre podem gerar espécies reativas e perturbar o DNA e enzimas essenciais. Análises teóricas da distribuição de carga e do potencial eletrostático sustentaram esse cenário ao identificar átomos específicos de nitrogênio e oxigênio como locais preferenciais para doação de elétrons ao cobre e a alvos biológicos. 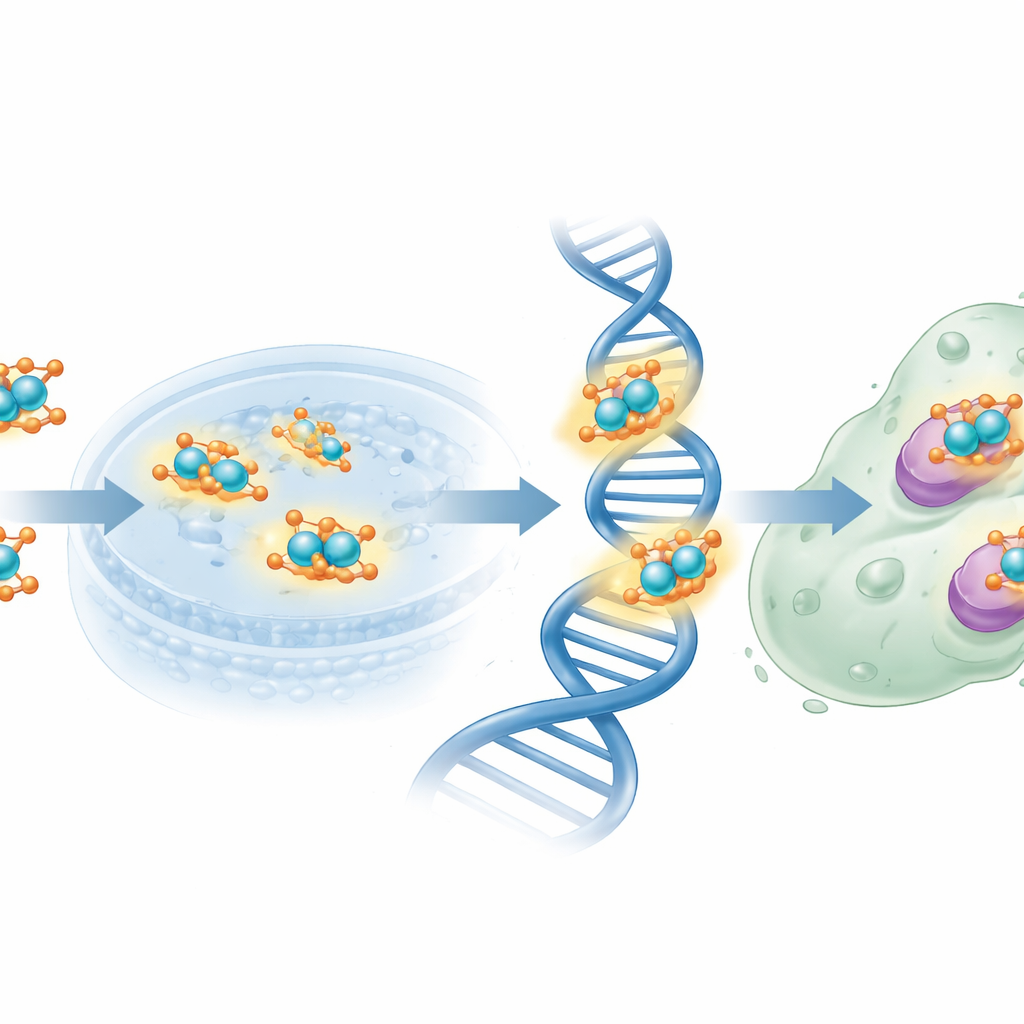
O que isso pode significar para medicamentos futuros
Em termos acessíveis, este estudo mostra que combinar de forma inteligente um “endereço” dérivado de uma vitamina com um centro metálico ativo pode transformar uma molécula orgânica relativamente branda em uma arma multifacetada contra microrganismos e células cancerosas. A base de Schiff derivada do ácido fólico sozinha é moderadamente ativa, mas quando associada ao cobre e estruturada como um complexo binuclear em escala nanométrica, torna‑se mais apta a inserir‑se no DNA, desorganizar o maquinário bacteriano e retardar o crescimento de células de câncer de mama. Embora ainda falte muito trabalho antes que tal composto possa chegar à clínica — especialmente estudos detalhados de segurança e seletividade — os resultados destacam uma estratégia de desenho promissora: usar nutrientes que naturalmente se dirigem a células de rápido crescimento como andaimes para complexos metálicos capazes de atacar doenças ao nível do DNA e de proteínas essenciais.
Citação: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
Palavras-chave: complexos de cobre, ácido fólico, base de Schiff, ligação com DNA, agentes anticâncer