Clear Sky Science · zh
GABARAPL1 对于 eIF2α 磷酸化依赖的丙酮酸盐应激反应中 HRI 激活至关重要(对亚砷酸钠的响应)
这对处于应激状态的细胞意味着什么
我们的细胞每天都受到来自环境的各种应激冲击,其中就包括像砷这样的有毒金属。为了生存,细胞必须迅速放慢日常活动,转入损伤控制模式。这项研究揭示了一个意想不到的参与者——一种名为 GABARAPL1 的蛋白,它帮助细胞感知砷诱导的应激并决定是否暂停蛋白质合成以保护其遗传信息。理解这一隐蔽的保护机制,可能有助于阐明细胞如何应对污染、为什么部分细胞对毒素更具抵抗力,以及应激控制通路在疾病中如何出错。
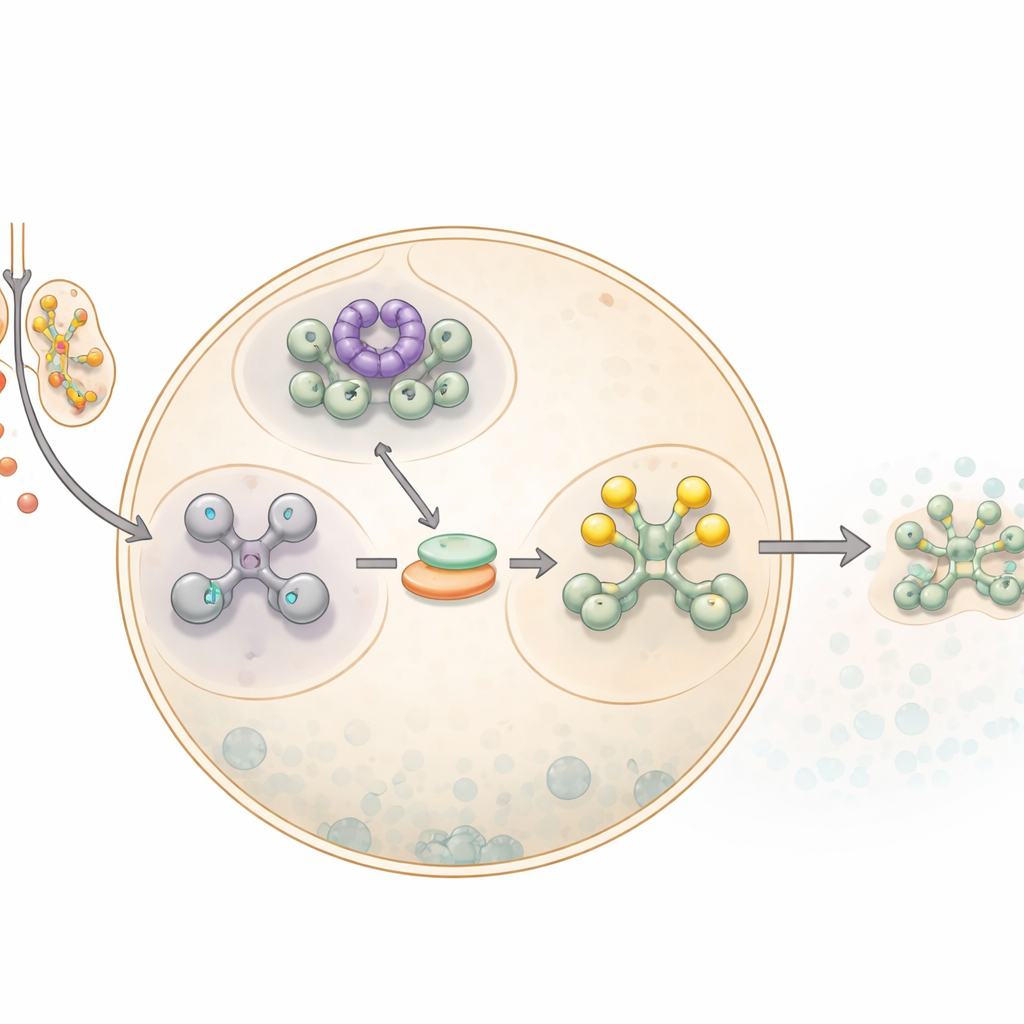
细胞如何按下“暂停”键
当细胞遇到亚砷酸钠(一种砷的形式)时,会启动被称为整合应激反应的广泛报警网络。该反应的关键步骤之一是关闭大多数蛋白质合成。细胞通过修饰一个核心翻译因子 eIF2α 来实现这一点——eIF2α 通常在将信使 RNA 翻译为蛋白质的起始阶段发挥作用。一旦 eIF2α 被化学标记(即磷酸化),细胞就会减慢整体蛋白质合成,并将未被使用的信使 RNA 输送到称为应激颗粒的高密度液滴中。这些颗粒作为临时储存位点,保护 RNA 直至危险解除,并为细胞重新编程其蛋白质产出争取时间。
一个循环利用蛋白的意外角色
GABARAPL1 属于一类以自噬最为人所知的蛋白家族,自噬是细胞内部的回收系统,用于分解不需要的成分。研究者在人体肺癌细胞中通过基因编辑或沉默去除 GABARAPL1,然后将细胞暴露于亚砷酸盐并观察结果。在正常细胞中,亚砷酸盐会迅速诱导应激颗粒形成并导致强烈的 eIF2α 磷酸化,这与强烈的应激反应一致。形成鲜明对比的是,缺失 GABARAPL1 的细胞形成的应激颗粒明显更少,eIF2α 的磷酸化也较弱,尽管亚砷酸盐确实进入了细胞并激活了其他信号通路。
定位报警链中断的环节
为弄清报警链在何处失败,团队将注意力集中在 HRI(一种位于 eIF2α 上游且能被砷相关的氧化应激特异性激活的激酶)上。他们发现 HRI 的早期激活步骤——涉及蛋白本身的自我修饰——在缺乏 GABARAPL1 的细胞中仍然发生。然而,一个更晚且关键的步骤受到了损害:HRI 与伴侣蛋白 HSP90 之间高效配合的形成受阻,HSP90 有助于 HRI 达到完全活性状态。利用一种可以检测两种蛋白何时非常接近的成像方法,研究者观察到在亚砷酸盐应激下,正常细胞中 HSP90 与 HRI 会随时间重新结合,但在缺少 GABARAPL1 时这一结合未能正常发生。这表明 GABARAPL1 起到了某种支架作用,在关键时刻将 HSP90 和 HRI 聚集到一起。
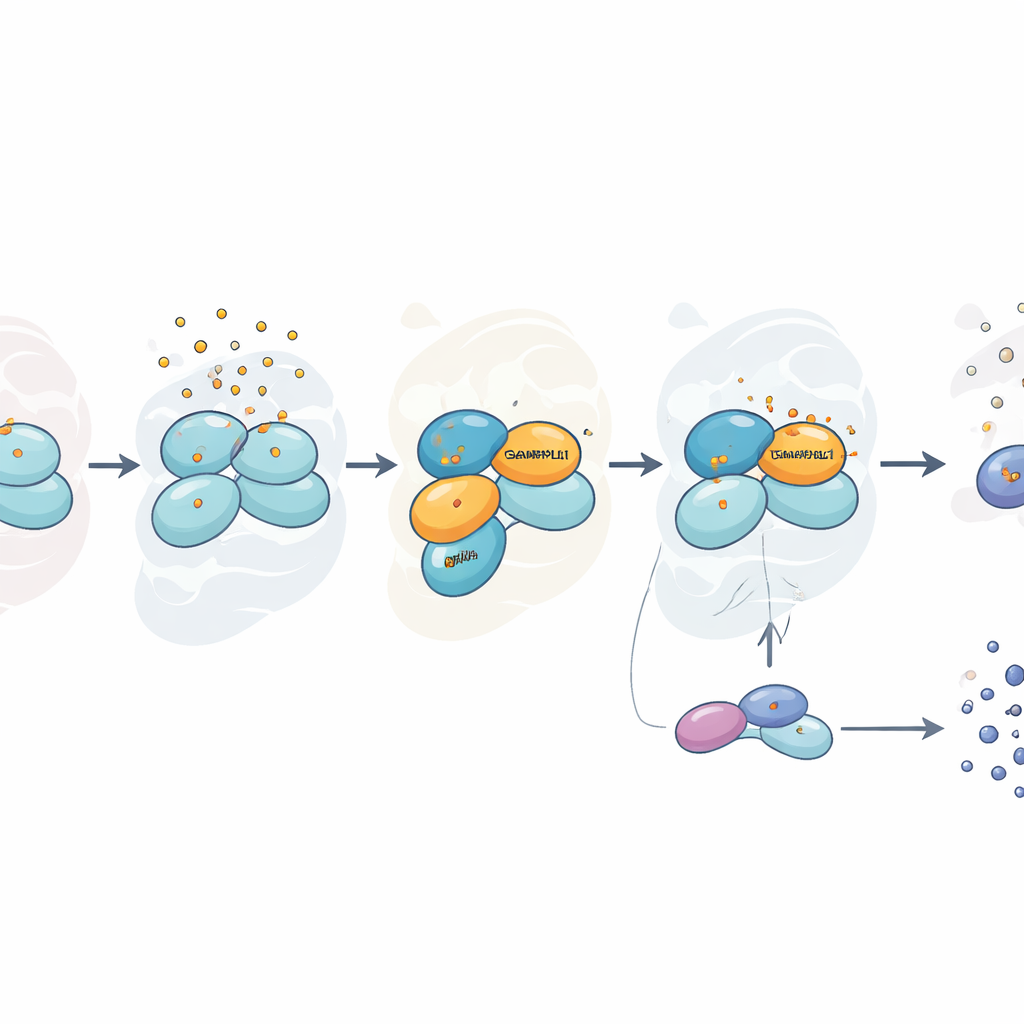
应激具有选择性,而非普遍性
有趣的是,对 GABARAPL1 的依赖性是针对亚砷酸盐特异的。当研究者用山梨醇(影响细胞水分平衡)或过氧化氢(另一种氧化损伤来源)对应激细胞时,即便没有 GABARAPL1,eIF2α 的磷酸化和应激颗粒的形成也能正常进行。然而在亚砷酸盐处理下,缺失 GABARAPL1 的细胞不仅表现出较弱的应激反应,在活力测试中似乎对毒素更有抵抗力,这可能是因为它们抑制了代谢活性,从而避免了与强烈报警反应相关的一部分损伤。同科的另一个相关蛋白 LC3B 仅表现出部分效应,这提示多个家族成员可能协同作用,但 GABARAPL1 扮演着主导角色。
这对细胞保护意味着什么
综合来看,这项研究提出 GABARAPL1 是砷应激通路中一个此前未被识别的辅助因子。通过作为 HSP90 的辅因子,它支持 HRI 的完全激活,进而促使 eIF2α 的修饰、减慢蛋白质合成并推动保护性应激颗粒的形成。缺少 GABARAPL1 时,这一连锁反应被削弱,使细胞对亚砷酸盐的响应变弱,并改变它们在生存与损伤之间的权衡。这些见解加深了我们对细胞如何解读特定环境威胁的理解,可能为未来关于毒性暴露、癌细胞耐受性以及针对细胞应激反应的治疗研究提供线索。
引用: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
关键词: 细胞应激反应, 砷毒性, 应激颗粒, 蛋白质质量控制, 自噬相关蛋白