Clear Sky Science · de
GABARAPL1 ist wichtig für die Aktivierung von HRI während der eIF2α-Phosphorylierung-abhängigen Stressantwort auf Natriumarsenit
Warum das für unsere Zellen unter Stress wichtig ist
Unsere Zellen sind täglich Umwelteinflüssen ausgesetzt, darunter toxischen Metallen wie Arsen. Um zu überleben, müssen sie normale Aktivitäten rasch herunterfahren und in einen Schadensbegrenzungsmodus wechseln. Diese Studie deckt einen unerwarteten Akteur auf, ein Protein namens GABARAPL1, das Zellen dabei hilft, arseninduzierten Stress zu erkennen und zu entscheiden, ob die Proteinsynthese pausiert und genetische Nachrichten geschützt werden sollen. Das Verständnis dieses verborgenen Schutzmechanismus kann Aufschluss darüber geben, wie Zellen mit Umweltverschmutzung umgehen, warum einige Zellen widerstandsfähiger gegen Toxine sind und wie Stresskontrollwege bei Krankheiten fehlreguliert werden können.
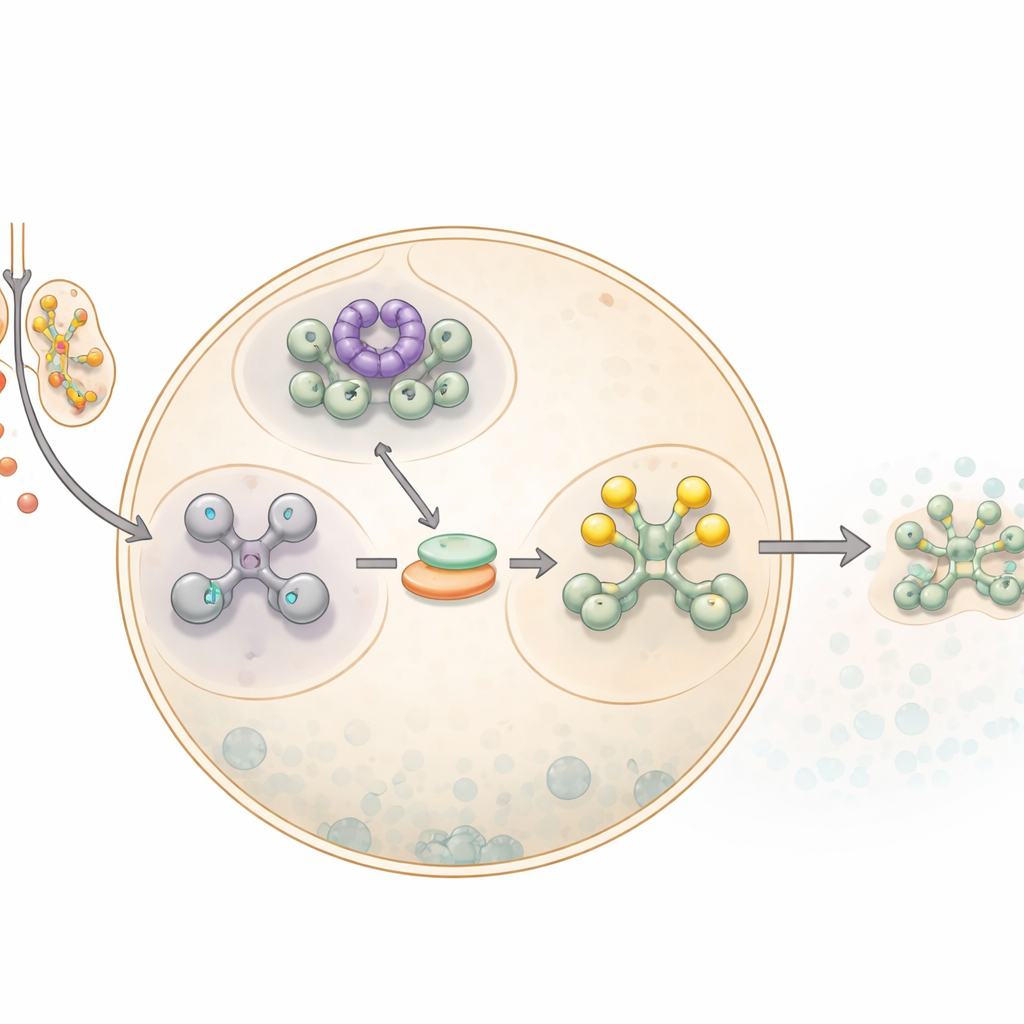
Wie Zellen den Pausenknopf drücken
Wenn Zellen Natriumarsenit, eine Form von Arsen, ausgesetzt werden, aktivieren sie ein umfassendes Alarmsystem, das als integrierte Stressantwort bekannt ist. Ein entscheidender Schritt dabei ist das Herunterfahren der meisten Proteinsynthese. Dies geschieht durch Modifikation eines zentralen Translationsfaktors, eIF2α, der normalerweise beim Starten der Proteinfertigung von Boten-RNAs hilft. Sobald eIF2α chemisch markiert, also phosphoryliert ist, verlangsamt die Zelle die allgemeine Proteinsynthese und leitet ungenutzte Boten-RNAs in dichte Tropfen um, die als Stressgranula bezeichnet werden. Diese Granula fungieren als vorübergehende Speicherorte, schützen RNAs, bis die Gefahr vorüber ist, und geben der Zelle Zeit, neu zu programmieren, welche Proteine sie herstellt.
Eine überraschende Rolle für ein Recycling-Protein
GABARAPL1 gehört zu einer Proteinfamilie, die vor allem für die Autophagie bekannt ist, das interne Recyclingsystem der Zelle, das unerwünschte Bestandteile abbaut. Die Forscher arbeiteten mit menschlichen Lungenkrebszellen und entfernten GABARAPL1 mittels Geneditierung oder Stilllegung. Anschließend setzten sie die Zellen Arsenit aus und beobachteten die Folgen. In normalen Zellen löste Arsenit schnell die Bildung von Stressgranula und eine starke eIF2α-Phosphorylierung aus, was einer robusten Stressantwort entspricht. Im auffälligen Gegensatz dazu bildeten Zellen ohne GABARAPL1 deutlich weniger Stressgranula und zeigten nur eine schwache Phosphorylierung von eIF2α, obwohl Arsenit offenbar in die Zellen eindrang und andere Signalwege aktivierte.
Das Defizit in der Alarmkette lokalisieren
Um zu verstehen, wo die Alarmkette versagte, konzentrierte sich das Team auf HRI, eine Kinase, die stromaufwärts von eIF2α sitzt und speziell durch arsenitbedingten oxidativen Stress aktiviert wird. Sie fanden heraus, dass frühe Aktivierungsschritte von HRI, die eine Selbstmodifikation des Proteins umfassen, in Zellen ohne GABARAPL1 weiterhin stattfanden. Ein späterer, entscheidender Schritt war jedoch beeinträchtigt: die effiziente Partnerschaft zwischen HRI und einem Chaperon-Protein namens HSP90, das HRI hilft, seine voll aktive Form zu erreichen. Mit einer Bildgebungsmethode, die nachweist, wenn zwei Proteine sehr nahe beieinander sitzen, beobachteten die Forscher, dass sich HSP90 und HRI bei Arsenitstress über die Zeit in normalen Zellen wieder zusammenschlossen, in Zellen ohne GABARAPL1 dies jedoch nicht richtig geschah. Das deutet darauf hin, dass GABARAPL1 als eine Art Gerüst wirkt, das HSP90 und HRI zum richtigen Zeitpunkt zusammenbringt.
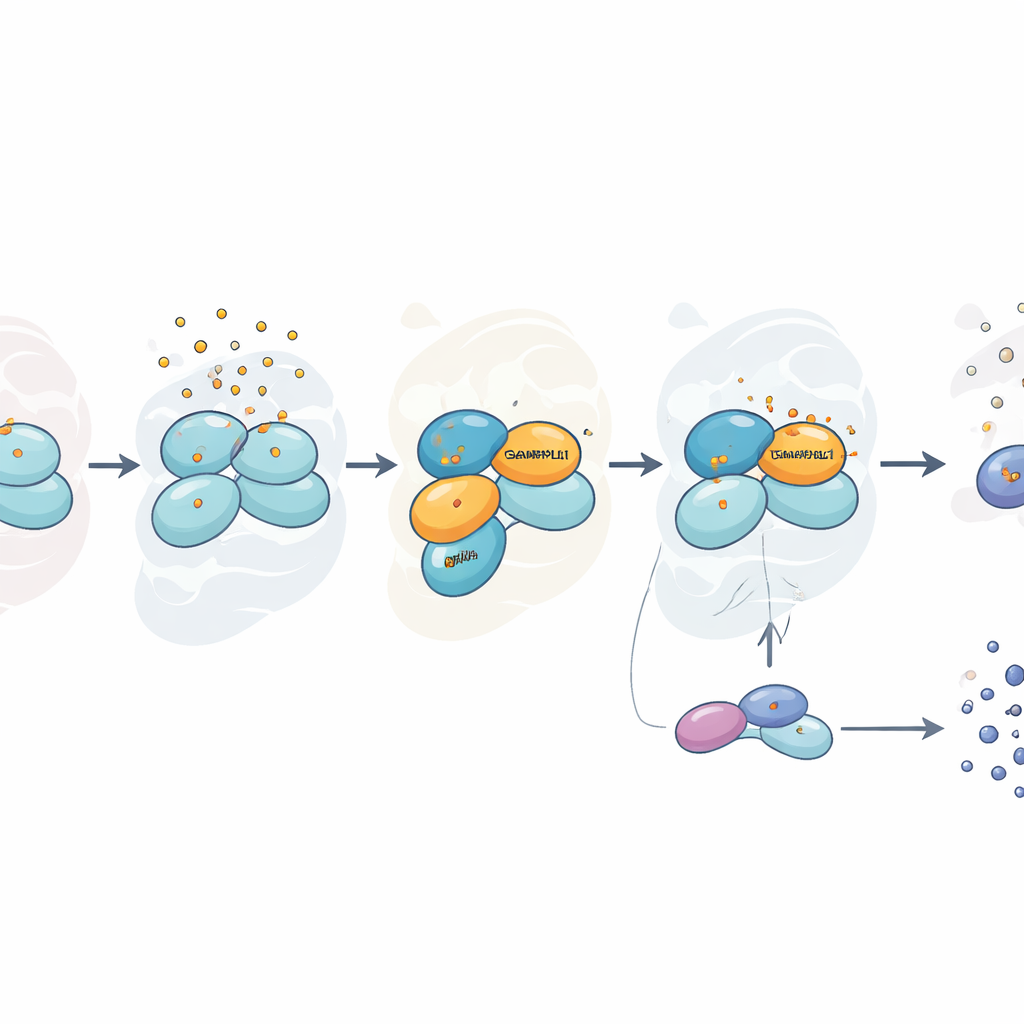
Stress, der selektiv ist, nicht universell
Interessanterweise war diese Abhängigkeit von GABARAPL1 spezifisch für Arsenit. Als die Forscher die Zellen mit Sorbitol, das das Wasserhaushalt der Zelle verändert, oder mit Wasserstoffperoxid, einer anderen Quelle oxidativen Schadens, stressten, verliefen eIF2α-Phosphorylierung und Bildung von Stressgranula auch ohne GABARAPL1 normal. Unter Arsenit zeigten Zellen ohne GABARAPL1 jedoch nicht nur eine schwächere Stressantwort, sondern erwiesen sich in Lebensfähigkeitstests auch als widerstandsfähiger gegenüber dem Toxin, wahrscheinlich weil sie ihre Stoffwechselaktivität dämpften und einigen Schäden vorbeugten, die mit einer intensiven Alarmreaktion einhergehen. Ein weiteres verwandtes Familienprotein, LC3B, zeigte nur eine partielle Wirkung, was darauf hindeutet, dass mehrere Familienmitglieder kooperieren können, GABARAPL1 jedoch eine führende Rolle spielt.
Was das für den Zellschutz bedeutet
Zusammengefasst schlagen die Autoren vor, dass GABARAPL1 ein bisher unerkanntes Hilfsprotein im Arsenit-Stressweg ist. Indem es als Kofaktor für HSP90 wirkt, unterstützt es die vollständige Aktivierung von HRI, das wiederum eIF2α modifiziert, die Proteinsynthese verlangsamt und die Bildung schützender Stressgranula antreibt. Ohne GABARAPL1 ist diese Ereigniskette geschwächt, wodurch Zellen weniger empfindlich auf Arsenit reagieren und sich das Gleichgewicht zwischen Überleben und Schaden verändert. Diese Erkenntnisse vertiefen unser Verständnis dafür, wie Zellen spezifische Umweltbedrohungen interpretieren, und können künftige Forschung zu toxischer Exposition, Resistenz von Krebszellen und Therapien, die zelluläre Stressantworten anvisieren, informieren.
Zitation: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Schlüsselwörter: zelluläre Stressantwort, Arsen-Vergiftung, Stressgranula, Proteinqualitätskontrolle, autophagiebezogene Proteine