Clear Sky Science · es
GABARAPL1 es importante para la activación de HRI durante la respuesta al estrés dependiente de la fosforilación de eIF2α frente al arseniato sódico
Por qué importa esto para nuestras células bajo estrés
Cada día, nuestras células son bombardeadas por estreses del entorno, incluidos metales tóxicos como el arsénico. Para sobrevivir, deben frenar rápidamente las actividades normales y cambiar a un modo de control de daños. Este estudio descubre a un actor inesperado, una proteína llamada GABARAPL1, que ayuda a las células a detectar el estrés inducido por arsénico y a decidir si pausar la producción de proteínas y proteger sus mensajes genéticos. Comprender este resguardo oculto puede arrojar luz sobre cómo las células afrontan la contaminación, por qué algunas células se vuelven más resistentes a las toxinas y cómo las vías de control del estrés pueden fallar en la enfermedad.
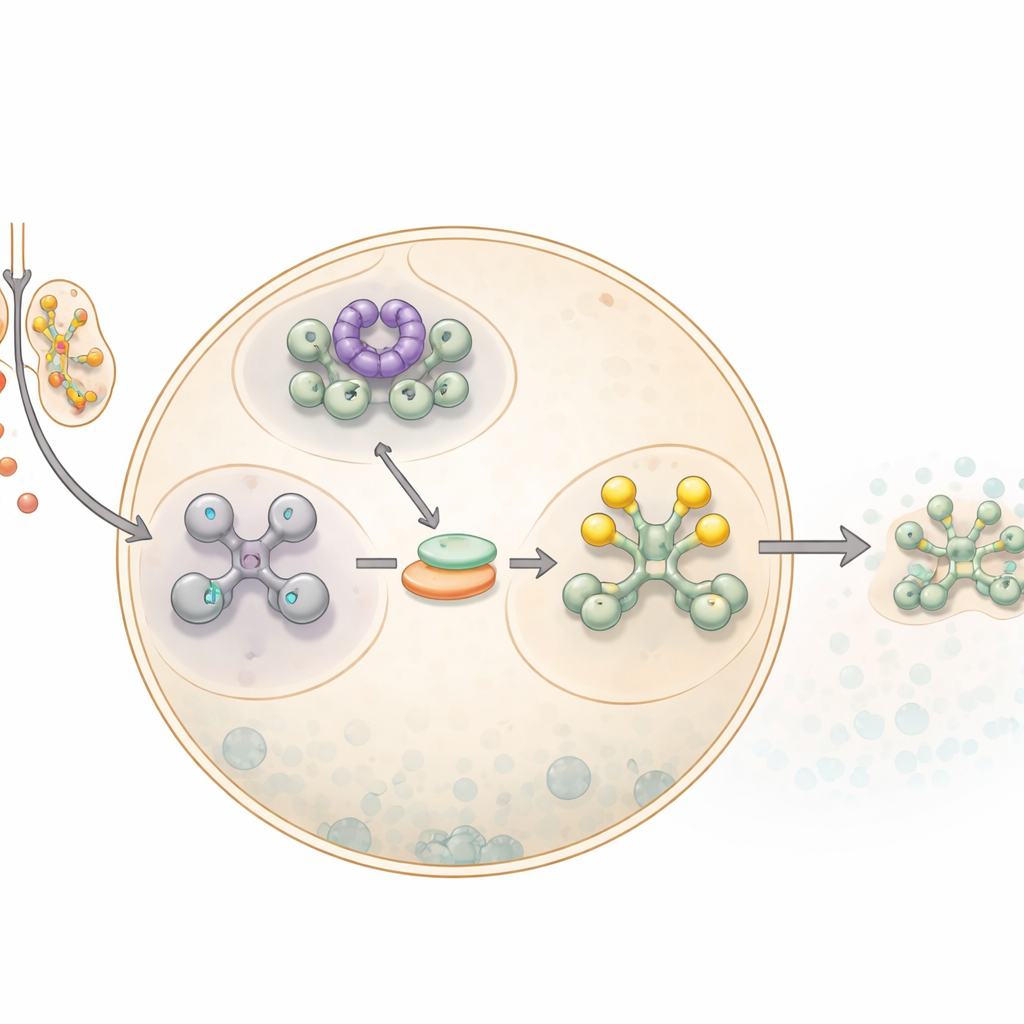
Cómo las células presionan el botón de pausa
Cuando las células se encuentran con arseniato sódico, una forma de arsénico, activan una red de alarma más amplia conocida como respuesta integrada al estrés. Un paso clave en esta respuesta es apagar la mayor parte de la producción de proteínas. Esto se logra modificando un factor central de la traducción, eIF2α, que normalmente ayuda a iniciar el proceso de construir proteínas a partir de ARN mensajero. Una vez que eIF2α es químicamente etiquetado, o fosforilado, la célula ralentiza la síntesis proteica general y desvía los ARNm no utilizados hacia gotículas densas llamadas gránulos de estrés. Estos gránulos actúan como sitios de almacenamiento temporales, protegiendo los ARNm hasta que el peligro ha pasado y dando tiempo a la célula para reprogramar qué proteínas produce.
Un papel sorprendente para una proteína de reciclaje
GABARAPL1 pertenece a una familia de proteínas conocida sobre todo por la autofagia, el sistema interno de reciclaje de la célula que descompone componentes no deseados. Los investigadores trabajaron con células humanas de cáncer de pulmón y eliminaron GABARAPL1 mediante edición génica o silenciamiento. A continuación, expusieron las células al arseniato y observaron lo que ocurría. En células normales, el arseniato desencadenó rápidamente la formación de gránulos de estrés y una fuerte fosforilación de eIF2α, coherente con una respuesta al estrés robusta. En marcado contraste, las células sin GABARAPL1 formaron muchos menos gránulos de estrés y mostraron solo una débil fosforilación de eIF2α, aunque el arseniato claramente entraba en las células y activaba otras vías de señalización.
Localizar el eslabón roto en la cadena de alarma
Para entender dónde falló la cadena de alarma, el equipo se centró en HRI, una quinasa que se sitúa aguas arriba de eIF2α y que se activa específicamente por el estrés oxidativo relacionado con el arseniato. Encontraron que los pasos tempranos de activación de HRI, que implican la auto-modificación de la proteína, todavía ocurrían en células sin GABARAPL1. Sin embargo, un paso posterior y crucial estaba deteriorado: la asociación eficiente entre HRI y una proteína chaperona llamada HSP90, que ayuda a HRI a alcanzar su forma totalmente activa. Usando un método de imagen que detecta cuando dos proteínas se encuentran muy próximas, los investigadores vieron que, bajo estrés por arseniato, HSP90 y HRI se reagruparon con el tiempo en células normales pero no lo hicieron correctamente cuando faltaba GABARAPL1. Esto apuntó a que GABARAPL1 actúa como una especie de andamiaje que reúne a HSP90 y HRI en el momento adecuado.
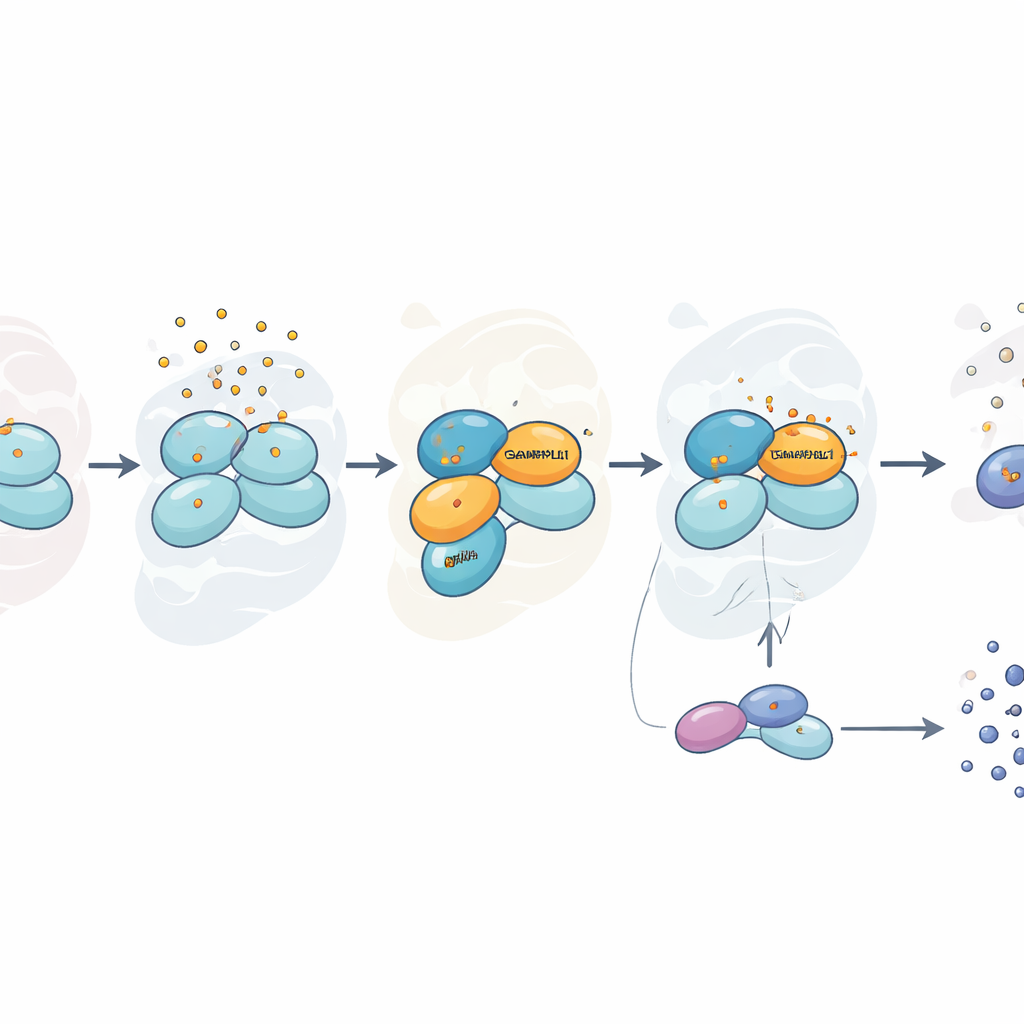
Estrés selectivo, no universal
Curiosamente, esta dependencia de GABARAPL1 fue específica del arseniato. Cuando los investigadores estresaron las células con sorbitol, que altera el equilibrio hídrico celular, o con peróxido de hidrógeno, otra fuente de daño oxidativo, la fosforilación de eIF2α y la formación de gránulos de estrés progresaron con normalidad incluso sin GABARAPL1. Bajo arseniato, sin embargo, las células carentes de GABARAPL1 no solo montaron una respuesta al estrés más débil, sino que además parecieron más resistentes a la toxina en pruebas de viabilidad, probablemente porque atenuaron su actividad metabólica y evitaron parte del daño asociado a una intensa reacción de alarma. Otra proteína relacionada de la misma familia, LC3B, mostró solo un efecto parcial, lo que sugiere que varios miembros de la familia pueden cooperar pero que GABARAPL1 desempeña un papel principal.
Qué significa esto para la protección celular
En conjunto, el estudio propone que GABARAPL1 es un colaborador hasta ahora no reconocido en la vía de estrés por arseniato. Al actuar como cofactor de HSP90, respalda la activación completa de HRI, que a su vez modifica eIF2α, ralentiza la producción de proteínas y promueve la formación de gránulos de estrés protectores. Sin GABARAPL1, esta cadena de eventos se debilita, dejando a las células menos receptivas al arseniato y alterando cómo equilibran la supervivencia frente al daño. Estos hallazgos profundizan nuestra comprensión de cómo las células interpretan amenazas ambientales específicas y pueden orientar futuras investigaciones sobre la exposición a tóxicos, la resistencia de células cancerosas y terapias que apunten a las respuestas celulares al estrés.
Cita: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Palabras clave: respuesta celular al estrés, toxicidad por arsénico, gránulos de estrés, control de calidad de proteínas, proteínas relacionadas con la autofagia