Clear Sky Science · sv
GABARAPL1 är viktigt för aktivering av HRI under eIF2α-fosforyleringsberoende stressrespons mot natriumarsenit
Varför detta spelar roll för våra celler under stress
Varje dag utsätts våra celler för miljöstress, bland annat toxiska metaller som arsenik. För att överleva måste de snabbt bromsa normala funktioner och gå över i skadelindringsläge. Denna studie avslöjar en oväntad aktör, ett protein kallat GABARAPL1, som hjälper celler att uppfatta arsenikinducerad stress och avgöra om de ska pausa proteinsyntesen och skydda sina genetiska budbärare. Att förstå denna dolda skyddsmekanism kan kasta ljus över hur celler hanterar föroreningar, varför vissa celler blir mer motståndskraftiga mot toxiner och hur stresskontrollvägar kan gå fel vid sjukdom.
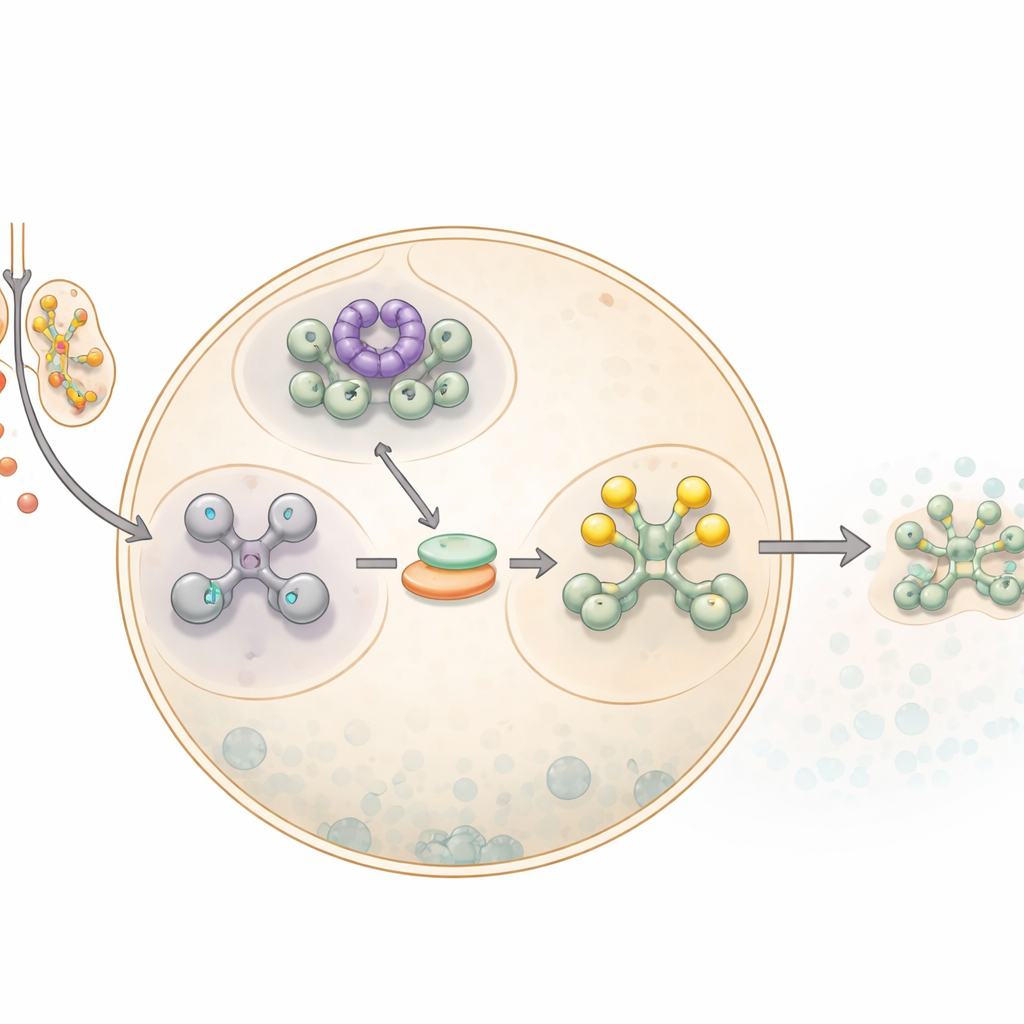
Hur cellerna trycker på pausknappen
När celler möter natriumarsenit, en form av arsenik, aktiverar de ett bredare larmsystem känt som den integrerade stressresponsen. Ett viktigt steg i denna respons är att stänga ned större delen av proteinsyntesen. Detta sker genom att ett kärntranslationselement, eIF2α, modifieras — normalt hjälper detta faktor till att starta omvandlingen av budbärar-RNA till proteiner. När eIF2α kemiskt märks, det vill säga fosforyleras, saktar cellen ner den generella proteinproduktionen och för oanvända budbärar-RNA in i täta droppar kallade stresskorn. Dessa korn fungerar som tillfälliga lagerplatser som skyddar RNA tills faran är över och ger cellen tid att omprogrammera vilka proteiner den tillverkar.
En överraskande roll för ett återvinningsprotein
GABARAPL1 tillhör en familj av proteiner som främst är kända för autofagi, cellens interna återvinningssystem som bryter ner oönskade komponenter. Forskarna jobbade med mänskliga lungcancerceller och avlägsnade GABARAPL1 med genredigering eller tystning. De utsatte sedan cellerna för arsenit och observerade vad som hände. I normala celler utlöste arsenit snabbt bildandet av stresskorn och stark fosforylering av eIF2α, i linje med en kraftfull stressrespons. I markant kontrast bildade celler utan GABARAPL1 avsevärt färre stresskorn och visade endast svag fosforylering av eIF2α, trots att arsenit klart trängde in i cellerna och aktiverade andra signalvägar.
Att peka ut den avbrutna länken i larmskedjan
För att förstå var larmskedjan brast fokuserade teamet på HRI, ett kinas som ligger uppströms om eIF2α och som specifikt aktiveras av arsenitrelaterad oxidativ stress. De fann att de tidiga aktiveringsstegen för HRI, som involverar självmärkning av proteinet, fortfarande skedde i celler utan GABARAPL1. Ett senare, avgörande steg var dock försvagat: det effektiva samarbetet mellan HRI och ett chaperonprotein kallat HSP90, som hjälper HRI att nå sin fullt aktiva form. Med en bildteknik som upptäcker när två proteiner sitter mycket nära varandra såg forskarna att HSP90 och HRI under arsenitstress återassocierade över tid i normala celler men inte gjorde det korrekt när GABARAPL1 saknades. Detta tyder på att GABARAPL1 fungerar som en slags stomme som för HSP90 och HRI samman vid rätt tidpunkt.
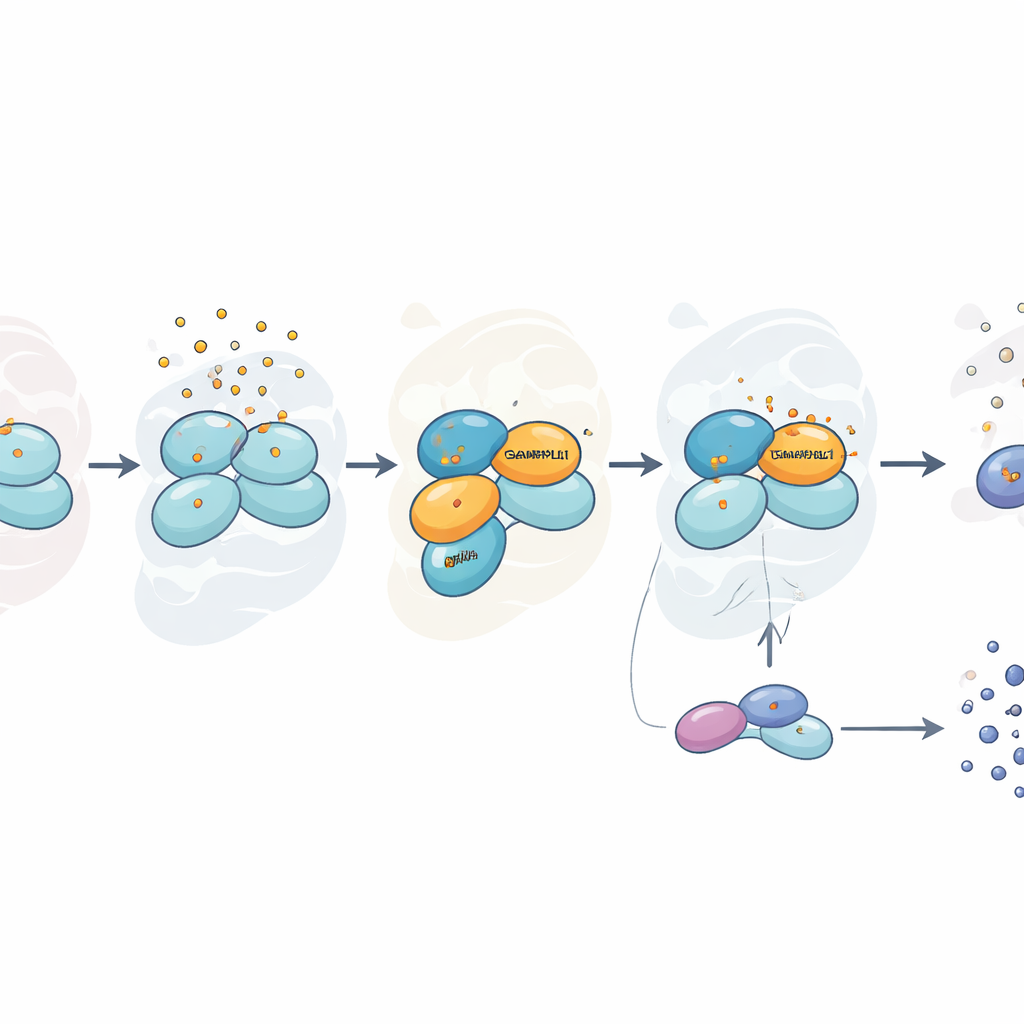
Stress som är selektiv, inte universell
Intressant nog var detta beroende av GABARAPL1 specifikt för arsenit. När forskarna stressade celler med sorbitol, som ändrar cellens vattenbalans, eller med väteperoxid, en annan källa till oxidativ skada, fortskred eIF2α-fosforylering och bildandet av stresskorn normalt även utan GABARAPL1. Under arsenit däremot visade celler utan GABARAPL1 inte bara en svagare stressrespons utan verkade också mer motståndskraftiga mot toxinet i livskrafttester, sannolikt eftersom de dämpade sin metaboliska aktivitet och undvek en del av skadorna som förknippas med en intensiv larmsituation. Ett annat närbesläktat protein i samma familj, LC3B, visade endast en partiell effekt, vilket antyder att flera familjemedlemmar kan samarbeta men att GABARAPL1 spelar en ledande roll.
Vad detta betyder för cellskydd
Tillsammans föreslår studien att GABARAPL1 är en tidigare oigenkänd hjälpare i arsenitstressvägen. Genom att fungera som en kofaktor för HSP90 stöder det HRI:s fulla aktivering, vilket i sin tur modifierar eIF2α, bromsar proteinproduktionen och driver bildningen av skyddande stresskorn. Utan GABARAPL1 försvagas denna händelsekedja, vilket gör att celler blir mindre responsiva mot arsenit och förändrar hur de väger överlevnad mot skada. Dessa insikter fördjupar vår förståelse av hur celler tolkar specifika miljöhot och kan informera framtida forskning om toxisk exponering, cancercellsresistens och terapier som riktar sig mot cellulära stressresponsvägar.
Citering: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Nyckelord: cellulär stressrespons, arsentoxisk, stresskorn, proteinkvalitetskontroll, autofagi-relaterade proteiner