Clear Sky Science · pt
GABARAPL1 é importante para a ativação de HRI durante a resposta ao estresse dependente da fosforilação de eIF2α em exposição ao arsenito de sódio
Por que isso importa para nossas células sob estresse
Cotidianamente, nossas células são bombardeadas por estresses ambientais, incluindo metais tóxicos como o arsênio. Para sobreviver, elas precisam desacelerar rapidamente suas atividades normais e mudar para um modo de controle de danos. Este estudo revela um ator inesperado, uma proteína chamada GABARAPL1, que ajuda as células a detectar o estresse induzido pelo arsênio e decidir se interrompem a produção proteica e protegem suas mensagens genéticas. Compreender esse mecanismo de proteção oculto pode esclarecer como as células lidam com a poluição, por que algumas ficam mais resistentes a toxinas e como as vias de controle do estresse podem falhar em doenças.
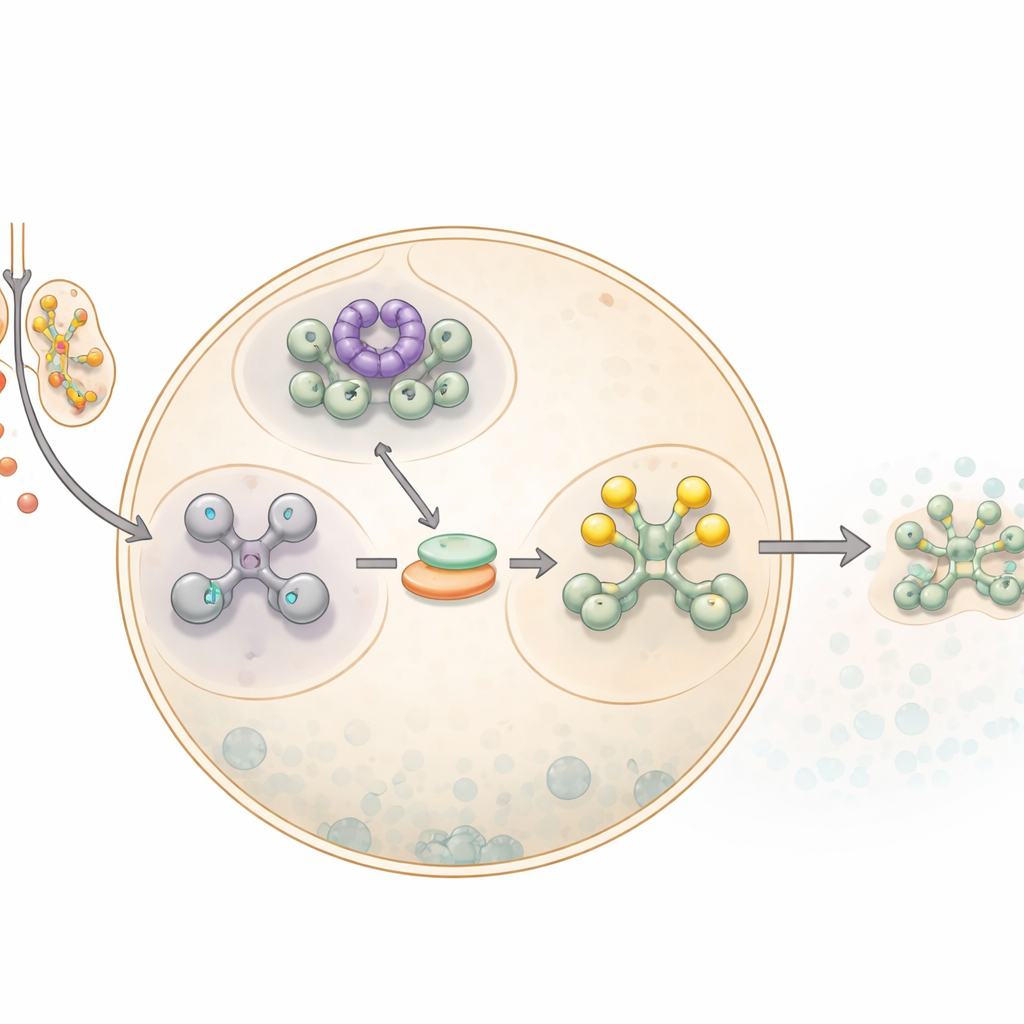
Como as células apertam o botão de pausa
Quando as células encontram arsenito de sódio, uma forma de arsênio, elas ativam uma rede de alarme mais ampla conhecida como resposta integrada ao estresse. Um passo chave nessa resposta é interromper a maior parte da produção proteica. Isso ocorre pela modificação de um fator central da tradução, eIF2α, que normalmente auxilia no início da síntese de proteínas a partir de RNAs mensageiros. Uma vez que eIF2α é quimicamente marcado, ou fosforilado, a célula reduz a produção geral de proteínas e direciona RNAs mensageiros não utilizados para gotículas densas chamadas grânulos de estresse. Esses grânulos atuam como locais de armazenamento temporário, protegendo os RNAs até que o perigo passe e dando tempo à célula para reprogramar quais proteínas produzir.
Um papel surpreendente para uma proteína de reciclagem
GABARAPL1 pertence a uma família de proteínas mais conhecida pela autofagia, o sistema interno de reciclagem celular que degrada componentes indesejados. Os pesquisadores trabalharam com células humanas de câncer de pulmão e removeram GABARAPL1 usando edição gênica ou silenciamento. Em seguida, expuseram as células ao arsenito e observaram o que acontecia. Em células normais, o arsenito rapidamente desencadeou a formação de grânulos de estresse e forte fosforilação de eIF2α, consistente com uma resposta robusta ao estresse. Em contraste marcante, células sem GABARAPL1 formaram muito menos grânulos de estresse e mostraram apenas fosforilação fraca de eIF2α, mesmo que o arsenito estivesse claramente entrando nas células e ativando outras vias de sinalização.
Localizando o elo quebrado na cadeia de alarme
Para entender onde a cadeia de alarme falhou, a equipe concentrou-se em HRI, uma quinase que atua acima de eIF2α e é especificamente ativada pelo estresse oxidativo associado ao arsenito. Eles descobriram que passos iniciais de ativação de HRI, envolvendo a automodificação da proteína, ainda ocorriam em células sem GABARAPL1. No entanto, um passo posterior e crucial estava prejudicado: a parceria eficiente entre HRI e uma proteína chaperona chamada HSP90, que ajuda HRI a atingir sua forma totalmente ativa. Usando um método de imageamento que detecta quando duas proteínas estão muito próximas, os pesquisadores observaram que, sob estresse por arsenito, HSP90 e HRI reassociavam-se ao longo do tempo em células normais, mas não o fizeram adequadamente quando GABARAPL1 estava ausente. Isso indicou que GABARAPL1 atua como uma espécie de andaime que reúne HSP90 e HRI no momento certo.
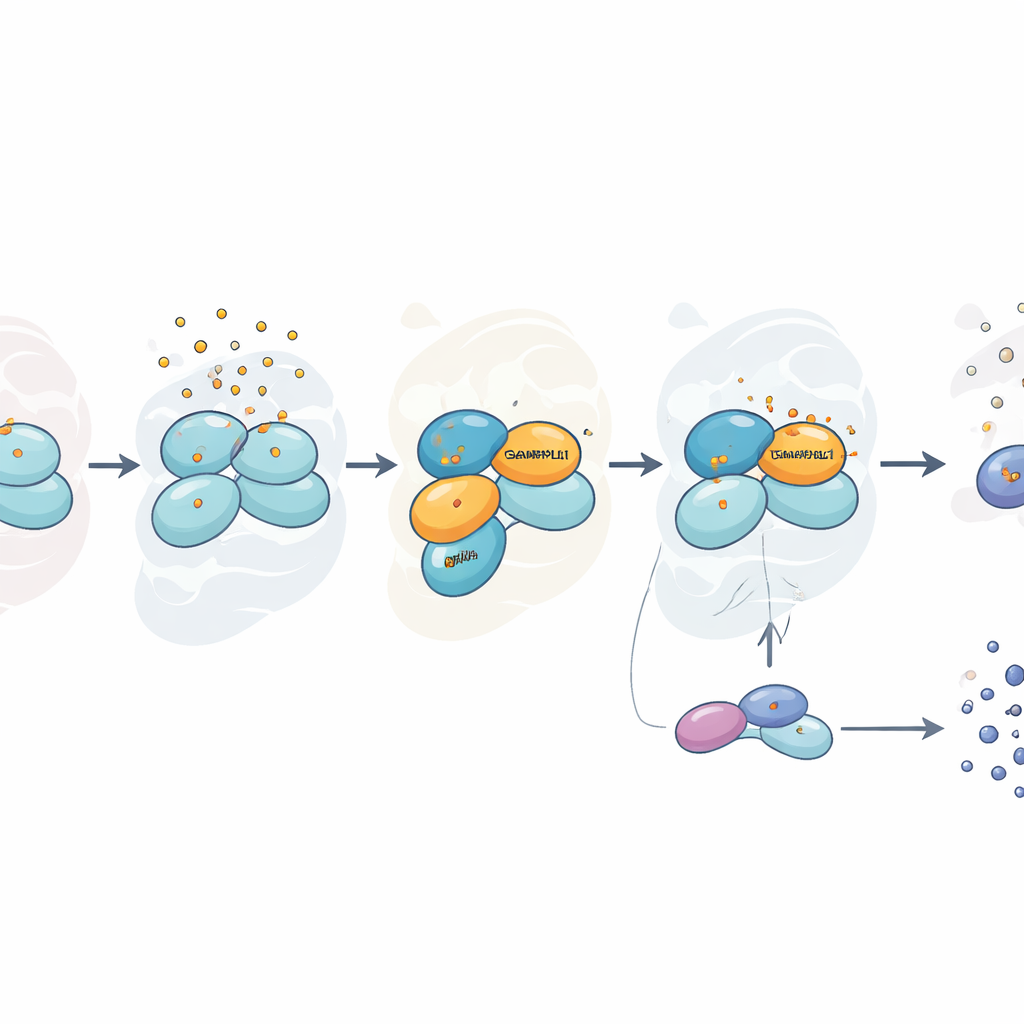
Estresse seletivo, não universal
Curiosamente, essa dependência de GABARAPL1 foi específica ao arsenito. Quando os pesquisadores estressaram as células com sorbitol, que altera o equilíbrio hídrico celular, ou com peróxido de hidrogênio, outra fonte de dano oxidativo, a fosforilação de eIF2α e a formação de grânulos de estresse prosseguiram normalmente mesmo sem GABARAPL1. Sob arsenito, entretanto, células sem GABARAPL1 não apenas apresentaram uma resposta ao estresse mais fraca, como também pareceram mais resistentes à toxina em testes de viabilidade, provavelmente porque reduziram sua atividade metabólica e evitaram parte dos danos associados a uma reação de alarme intensa. Outra proteína relacionada da mesma família, LC3B, mostrou apenas um efeito parcial, sugerindo que vários membros da família podem cooperar, mas que GABARAPL1 desempenha um papel predominante.
O que isso significa para a proteção celular
Em conjunto, o estudo propõe que GABARAPL1 é um cofator até agora não reconhecido na via de estresse induzida por arsenito. Ao atuar como cofator para HSP90, ele apoia a ativação completa de HRI, que por sua vez modifica eIF2α, desacelera a produção proteica e impulsiona a formação de grânulos de estresse protetores. Na ausência de GABARAPL1, essa cadeia de eventos fica enfraquecida, deixando as células menos responsivas ao arsenito e alterando como equilibram sobrevivência versus dano. Esses achados aprofundam nossa compreensão de como as células interpretam ameaças ambientais específicas e podem orientar futuras pesquisas sobre exposição a toxinas, resistência de células cancerosas e terapias que visem as respostas celulares ao estresse.
Citação: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Palavras-chave: resposta ao estresse celular, toxicidade por arsênio, grânulos de estresse, controle da qualidade de proteínas, proteínas relacionadas à autofagia