Clear Sky Science · nl
GABARAPL1 is belangrijk voor de activatie van HRI tijdens de eIF2α-fosforyleringsafhankelijke stressreactie op natriumarseniet
Waarom dit van belang is voor onze cellen onder stress
Dagelijks worden onze cellen bestookt door omgevingsstressoren, waaronder toxische metalen zoals arseen. Om te overleven moeten ze hun normale activiteiten snel vertragen en overschakelen op schadebeheersing. Deze studie onthult een onverwachte speler, een eiwit genaamd GABARAPL1, dat cellen helpt arsenicum-geïnduceerde stress te herkennen en te beslissen of ze de eiwitproductie pauzeren en hun genetische boodschappen beschermen. Inzicht in deze verborgen waarborg kan belichten hoe cellen omgaan met verontreiniging, waarom sommige cellen meer resistent worden tegen toxines, en hoe stressbeheersingsroutes kunnen ontsporen bij ziekte.
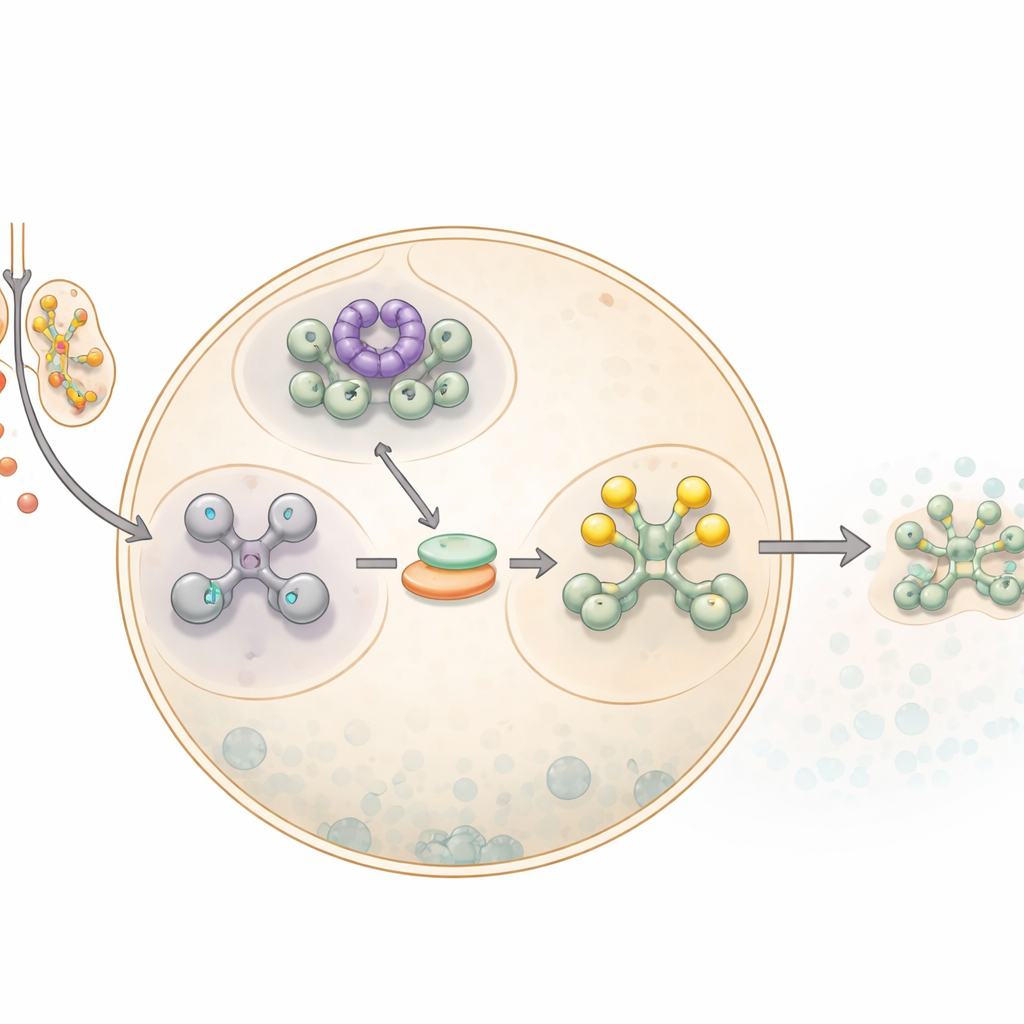
Hoe cellen op de pauzeknop drukken
Wanneer cellen in contact komen met natriumarseniet, een vorm van arseen, schakelen ze een breder alarmnetwerk in dat bekend staat als de geïntegreerde stressrespons. Een belangrijke stap in deze respons is het stilleggen van de meeste eiwitsynthese. Dat gebeurt door een kern-translationele factor, eIF2α, chemisch te wijzigen; normaal helpt die factor bij het starten van de bouw van eiwitten uit boodschapper-RNA’s. Zodra eIF2α gefosforyleerd is, vertraagt de cel de algemene eiwitproductie en worden ongebruikte boodschapper-RNA’s geleid naar dichte druppels die stressgranules worden genoemd. Deze granules fungeren als tijdelijke opslagplaatsen, beschermen RNA’s totdat het gevaar voorbij is en geven de cel tijd om te herprogrammeren welke eiwitten worden gemaakt.
Een verrassende rol voor een recyclingeiwit
GABARAPL1 behoort tot een familie eiwitten die vooral bekend is van autofagie, het interne recyclingsysteem van de cel dat ongewenste componenten afbreekt. De onderzoekers werkten met humane longkankercellen en verwijderden GABARAPL1 met genbewerking of door het te onderdrukken. Vervolgens stelden ze de cellen bloot aan arseniet en observeerden ze de effecten. In normale cellen veroorzaakte arseniet snel de vorming van stressgranules en sterke fosforylering van eIF2α, wat overeenkomt met een robuuste stressrespons. In opvallend contrast vormden cellen zonder GABARAPL1 veel minder stressgranules en vertoonden ze slechts zwakke fosforylering van eIF2α, hoewel arseniet duidelijk de cellen binnendrong en andere signaleringsroutes activeerde.
Het gebroken schakelpunt in de alarmketen aanwijzen
Om te begrijpen waar de alarmketen faalde, richtte het team zich op HRI, een kinase die stroomopwaarts van eIF2α zit en specifiek wordt geactiveerd door arseniet-gerelateerde oxidatieve stress. Ze ontdekten dat vroege activeringsstappen van HRI, die zelfmodificatie van het eiwit omvatten, nog steeds plaatsvonden in cellen zonder GABARAPL1. Echter, een latere, cruciale stap was verstoord: de efficiënte samenwerking tussen HRI en een chaperone-eiwit genaamd HSP90, dat HRI helpt zijn volledig actieve vorm te bereiken. Met een beeldvormingsmethode die detecteert wanneer twee eiwitten zeer dicht bij elkaar zitten, zagen de onderzoekers dat onder arsenietstress HSP90 en HRI in normale cellen na verloop van tijd weergeassocieerd raakten, maar dat dat niet goed gebeurde wanneer GABARAPL1 ontbrak. Dit wees erop dat GABARAPL1 fungeert als een soort steiger of scaffold die HSP90 en HRI op het juiste moment bij elkaar brengt.
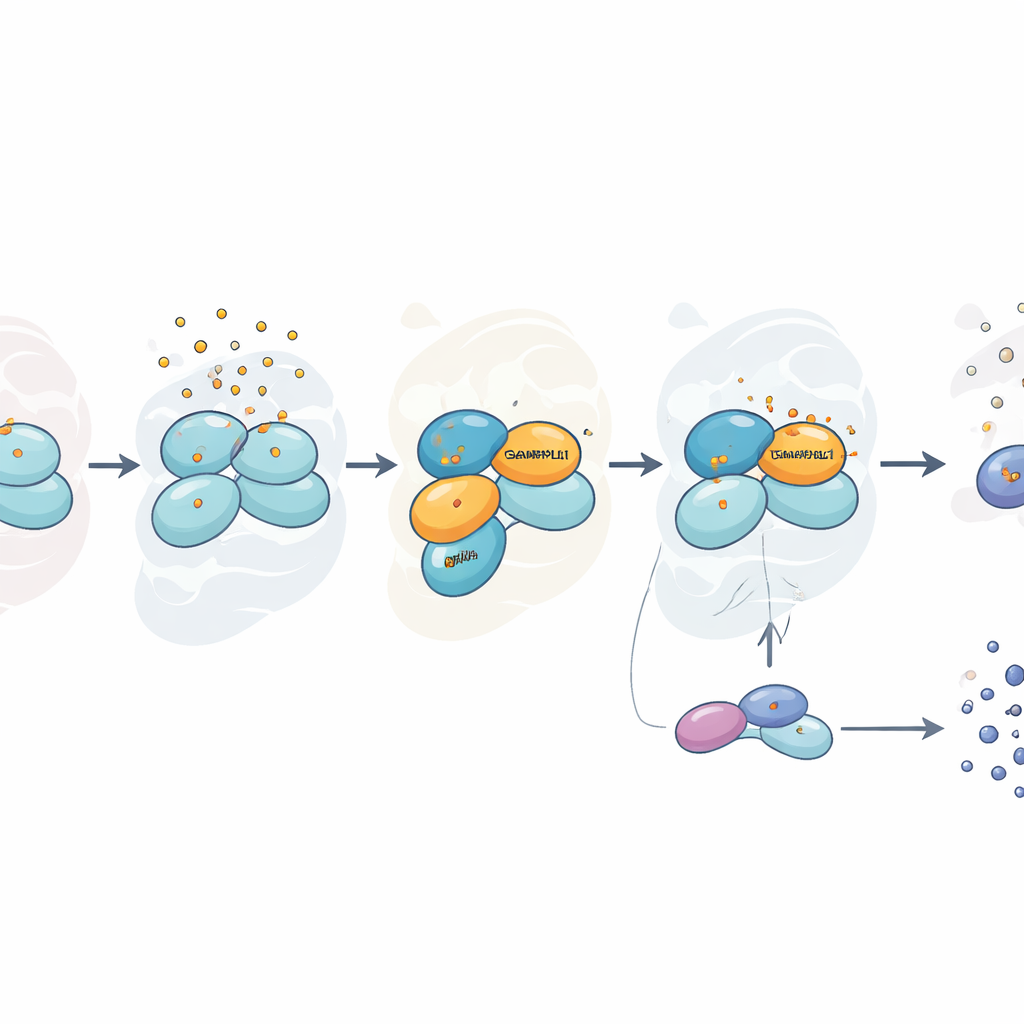
Stress die selectief is, niet universeel
Interessant genoeg was deze afhankelijkheid van GABARAPL1 specifiek voor arseniet. Wanneer de onderzoekers cellen stressen met sorbitol, dat de waterbalans van cellen verandert, of met waterstofperoxide, een andere bron van oxidatieve schade, verliepen eIF2α-fosforylering en de vorming van stressgranules normaal, zelfs zonder GABARAPL1. Onder arseniet echter leverden cellen zonder GABARAPL1 niet alleen een zwakkere stressrespons, maar leken ze in levensvatbaarheidstests ook resistenter tegen het toxine, waarschijnlijk omdat ze hun metabolische activiteit dempten en daarmee sommige schade vermeden die gepaard gaat met een sterke alarmreactie. Een ander verwant eiwit uit dezelfde familie, LC3B, toonde slechts een gedeeltelijk effect, wat doet vermoeden dat meerdere familieleden kunnen samenwerken maar dat GABARAPL1 een leidende rol speelt.
Wat dit betekent voor celbescherming
Samengevat stellen de auteurs dat GABARAPL1 een eerder onopgemerkte helper is in de arseniet-stresstraat. Door te fungeren als cofactor voor HSP90 ondersteunt het de volledige activatie van HRI, dat op zijn beurt eIF2α wijzigt, de eiwitproductie vertraagt en de vorming van beschermende stressgranules aanstuurt. Zonder GABARAPL1 is deze keten van gebeurtenissen verzwakt, waardoor cellen minder gevoelig reageren op arseniet en hun balans tussen overleving en schade verandert. Deze inzichten verdiepen ons begrip van hoe cellen specifieke bedreigingen uit de omgeving interpreteren en kunnen toekomstig onderzoek over toxische blootstelling, resistentie van kankercellen en therapieën die cellulaire stressresponsen targeten, informeren.
Bronvermelding: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Trefwoorden: cellulaire stressreactie, arsenictoxiciteit, stressgranules, eiwitkwaliteitscontrole, autofagie-gerelateerde eiwitten