Clear Sky Science · ja
GABARAPL1は、硫酸化依存的なeIF2αリン酸化ストレス応答におけるHRI活性化に重要である
細胞がストレス下で直面する重要性
私たちの細胞は毎日、ヒ素のような有害金属を含む環境ストレスにさらされています。生き延びるために、細胞は通常の活動を素早く低下させ、ダメージ制御モードに切り替える必要があります。本研究は、GABARAPL1という意外な役者が、ヒ素によるストレスを感知し、タンパク質合成を一時停止して遺伝情報を保護するかどうかを判断するのを助けることを明らかにしました。この隠れた防御機構の理解は、細胞が汚染にどう対処するか、なぜ一部の細胞が毒素に対して耐性を示すのか、そしてストレス制御経路が疾患でどのように誤動作するかを解明する手がかりを与える可能性があります。
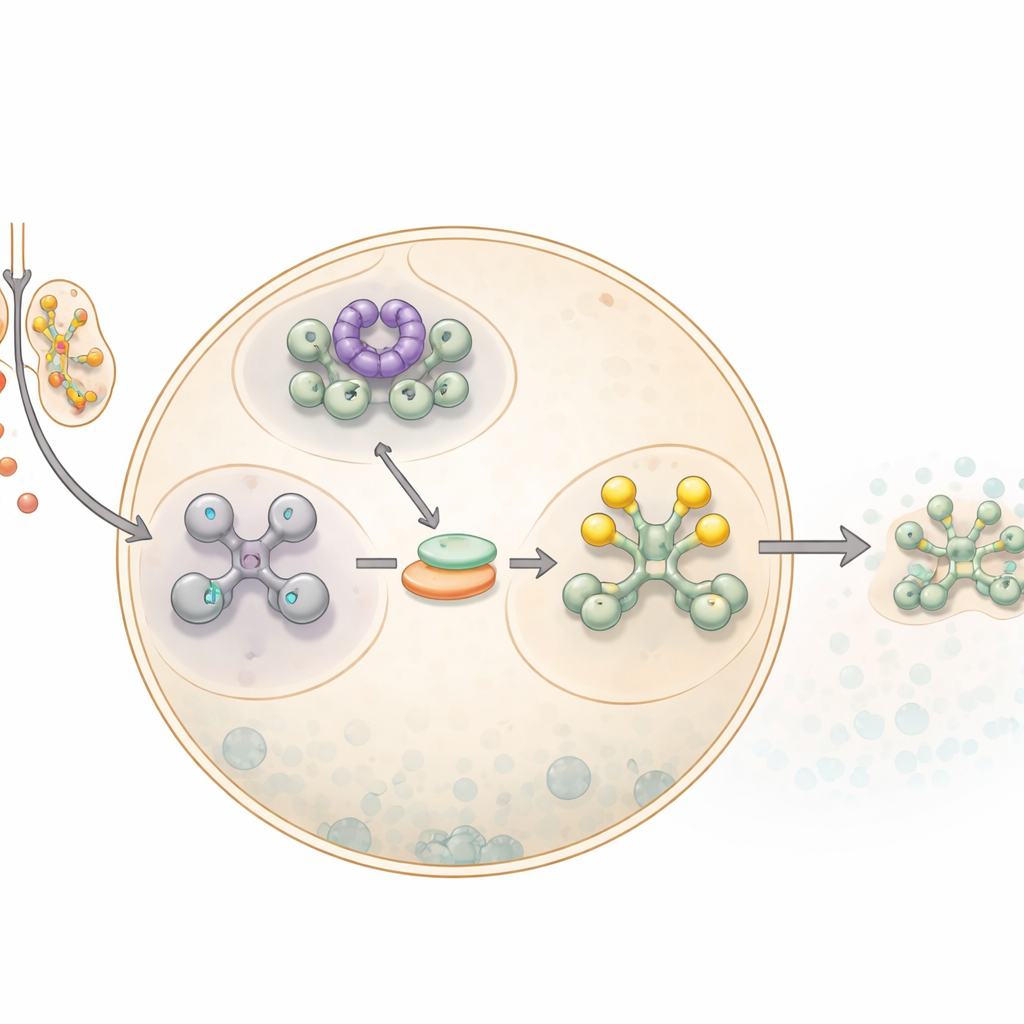
細胞が一時停止ボタンを押す仕組み
細胞が硫酸化ナトリウム(sodium arsenite)に遭遇すると、統合ストレス応答と呼ばれる広範なアラームネットワークが作動します。この応答の重要な段階は、ほとんどのタンパク質合成を停止することです。これは、通常メッセンジャーRNAからタンパク質の合成開始を助ける翻訳因子eIF2αを修飾することで行われます。一度eIF2αが化学的に標識(リン酸化)されると、細胞は一般的なタンパク質合成を鈍らせ、使われなくなったメッセンジャーRNAを密な液滴状のストレス顆粒に振り分けます。これらの顆粒は危険が去るまでRNAを一時保管し、細胞がどのタンパク質を作るかを再プログラムする時間を与える役割を果たします。
リサイクルタンパク質の意外な役割
GABARAPL1はオートファジーでよく知られるタンパク質ファミリーに属しており、細胞内の不要成分を分解する内部リサイクルシステムに関与します。研究者らはヒトの肺がん細胞を用い、遺伝子編集やサイレンシングでGABARAPL1を除去しました。次に細胞をアーセナイトにさらして経過を観察しました。正常な細胞では、アーセナイトは迅速にストレス顆粒の形成と強いeIF2αのリン酸化を引き起こし、強固なストレス応答が示されました。対照的に、GABARAPL1を欠く細胞ではストレス顆粒の形成が著しく少なく、eIF2αのリン酸化も弱かったのです。これはアーセナイトが細胞に取り込まれ、他のシグナル経路は確かに活性化されていたにもかかわらず起こりました。
アラーム連鎖のどこが途切れたかの特定
連鎖がどこで失敗したのかを理解するために、チームはeIF2αの上流に位置し、アーセナイトに関連した酸化ストレスによって特異的に活性化されるキナーゼであるHRIに注目しました。GABARAPL1欠損細胞でも、タンパク質の自己修飾を含むHRIの初期活性化ステップは起こることがわかりました。しかし、後の重要な段階が障害されていました。それは、HRIが完全に活性化されるのを助けるシャペロンタンパク質HSP90との効率的な協働です。二つのタンパク質が非常に近接したときに検出するイメージング法を用いると、アーセナイトストレス下でHSP90とHRIは正常細胞では時間とともに再結合したのに対し、GABARAPL1が欠如していると適切に再結合しませんでした。これにより、GABARAPL1はHSP90とHRIを適切なタイミングで結びつける足場のように働くことが示唆されました。
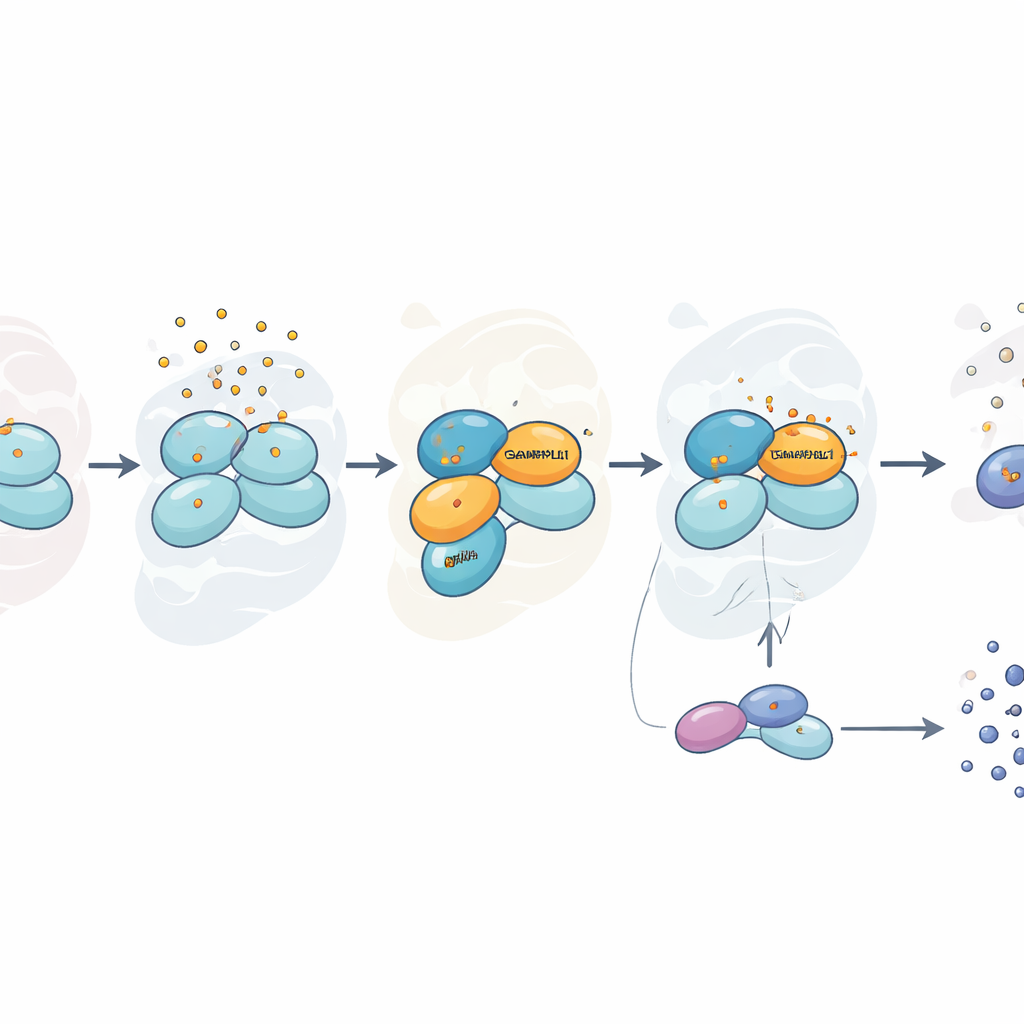
普遍的ではなく選択的なストレス応答
興味深いことに、このGABARAPL1への依存性はアーセナイトに特異的でした。細胞の水分バランスを変えるソルビトールや、別の酸化ダメージ源である過酸化水素で細胞をストレスにさらした場合、GABARAPL1がなくてもeIF2αのリン酸化やストレス顆粒の形成は通常どおり進行しました。しかしアーセナイト下では、GABARAPL1を欠く細胞はストレス応答が弱まるだけでなく、生存率試験で毒素に対してより耐性を示すように見えました。これは代謝活動を抑え、強いアラーム反応に伴う一部のダメージを回避したためと考えられます。同じファミリーに属する別の関連タンパク質LC3Bは部分的な影響しか示さず、複数のファミリーメンバーが協力しうるがGABARAPL1が主要な役割を果たすことを示唆しています。
細胞保護に対する意味合い
総じて、本研究はGABARAPL1がアーセナイトストレス経路におけるこれまで認識されていなかった補助因子であることを提案します。GABARAPL1はHSP90の補因子として働き、HRIの完全な活性化を支え、それがeIF2αを修飾してタンパク質合成を遅らせ、保護的なストレス顆粒の形成を促します。GABARAPL1がないと、この一連の出来事は弱まり、細胞はアーセナイトに対する応答が鈍くなり、生存とダメージのバランスが変化します。これらの知見は、細胞が特定の環境脅威をどのように解釈するかの理解を深め、毒性曝露、がん細胞の耐性、細胞ストレス応答を標的とした治療研究に今後の示唆を与える可能性があります。
引用: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
キーワード: 細胞ストレス応答, ヒ素毒性, ストレス顆粒, タンパク質品質管理, オートファジー関連タンパク質