Clear Sky Science · it
GABARAPL1 è importante per l'attivazione di HRI durante la risposta allo stress dipendente dalla fosforilazione di eIF2α indotta dall'arsenito di sodio
Perché questo è importante per le nostre cellule sotto stress
Ogni giorno le nostre cellule subiscono stress dall'ambiente, compresi metalli tossici come l'arsenico. Per sopravvivere devono rallentare rapidamente le attività normali e passare a una modalità di controllo dei danni. Questo studio rivela un attore inaspettato, una proteina chiamata GABARAPL1, che aiuta le cellule a percepire lo stress indotto dall'arsenico e a decidere se sospendere la produzione proteica e proteggere i loro messaggi genetici. Comprendere questa salvaguardia nascosta può fare luce su come le cellule affrontano l'inquinamento, perché alcune diventano più resistenti alle tossine e come i percorsi di controllo dello stress possano alterarsi nelle malattie.
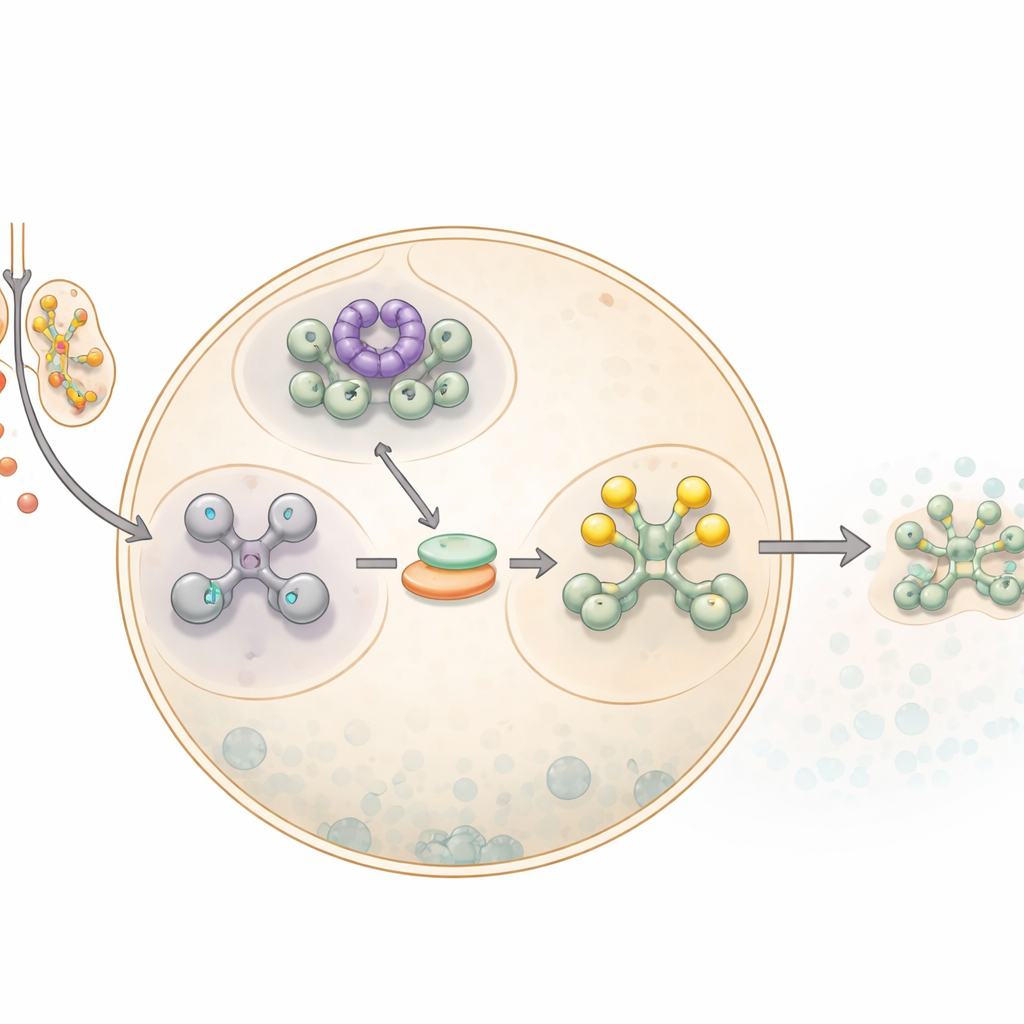
Come le cellule premono il pulsante di pausa
Quando le cellule incontrano l'arsenito di sodio, una forma di arsenico, attivano una rete di allarme più ampia nota come risposta integrata allo stress. Un passaggio chiave in questa risposta è l'arresto della maggior parte della produzione proteica. Ciò avviene modificando un fattore di traduzione di base, eIF2α, che normalmente aiuta ad avviare il processo di costruzione delle proteine a partire dagli RNA messaggeri. Una volta che eIF2α viene chimicamente marcato, o fosforilato, la cellula rallenta la sintesi proteica generale e convoglia gli RNA messaggeri non utilizzati in goccioline dense chiamate granuli di stress. Questi granuli agiscono come depositi temporanei, proteggendo gli RNA fino a quando il pericolo non è passato e dando alla cellula il tempo per riprogrammarne la produzione proteica.
Un ruolo sorprendente per una proteina del riciclo
GABARAPL1 appartiene a una famiglia di proteine note soprattutto per l'autofagia, il sistema interno di riciclo della cellula che degrada componenti indesiderati. I ricercatori hanno lavorato con cellule umane di carcinoma polmonare e hanno rimosso GABARAPL1 mediante editing genetico o silenziamento. Hanno quindi esposto le cellule all'arsenito e osservato cosa accadeva. Nelle cellule normali l'arsenito induceva rapidamente la formazione di granuli di stress e una forte fosforilazione di eIF2α, coerente con una robusta risposta allo stress. In netto contrasto, le cellule prive di GABARAPL1 formarono molti meno granuli di stress e mostrarono solo una debole fosforilazione di eIF2α, nonostante l'arsenito fosse chiaramente entrato nelle cellule e avesse attivato altre vie di segnalazione.
Individuare il collegamento interrotto nella catena di allarme
Per capire dove la catena di allarme si interrompeva, il team si è concentrato su HRI, una chinasi che agisce a monte di eIF2α e viene specificamente attivata dallo stress ossidativo correlato all'arsenito. Hanno scoperto che i primi passaggi di attivazione di HRI, che prevedono l'automodificazione della proteina, avvenivano ancora nelle cellule senza GABARAPL1. Tuttavia un passaggio cruciale successivo era compromesso: l'efficiente collaborazione tra HRI e una proteina chaperone chiamata HSP90, che aiuta HRI a raggiungere la sua forma completamente attiva. Utilizzando un metodo di imaging che rileva quando due proteine si avvicinano molto, i ricercatori osservarono che, sotto stress da arsenito, HSP90 e HRI si riassociavano nel tempo nelle cellule normali ma non riuscivano a farlo correttamente in assenza di GABARAPL1. Ciò indica che GABARAPL1 funge da sorta di impalcatura che mette insieme HSP90 e HRI al momento giusto.
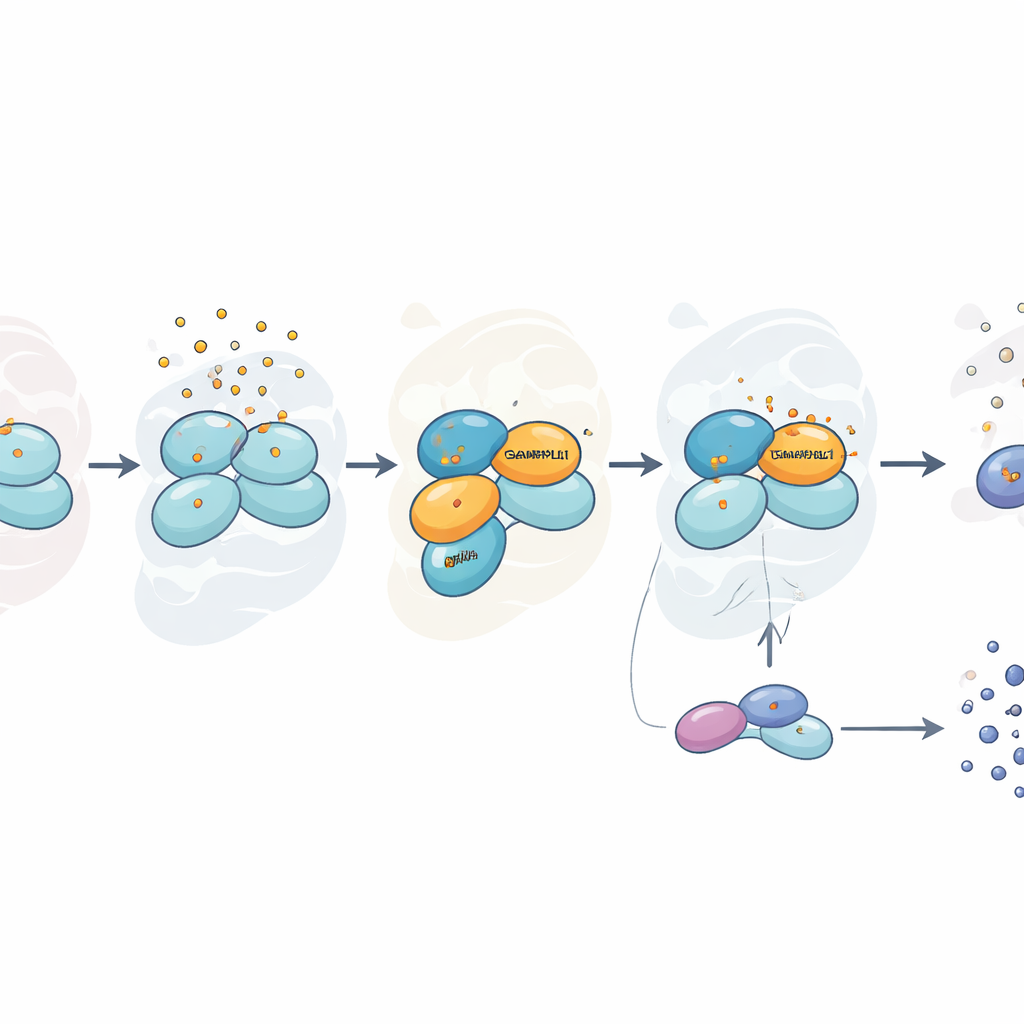
Uno stress selettivo, non universale
Interessante notare che questa dipendenza da GABARAPL1 era specifica per l'arsenito. Quando i ricercatori stressarono le cellule con sorbitolo, che altera l'equilibrio idrico cellulare, o con perossido di idrogeno, un'altra fonte di danno ossidativo, la fosforilazione di eIF2α e la formazione dei granuli di stress procedettero normalmente anche senza GABARAPL1. Sotto arsenito, invece, le cellule prive di GABARAPL1 non solo montarono una risposta allo stress più debole ma risultarono apparentemente più resistenti alla tossina nei test di vitalità, probabilmente perché attenuarono la loro attività metabolica ed evitarono parte dei danni associati a una reazione di allarme intensa. Un'altra proteina correlata della stessa famiglia, LC3B, mostrò solo un effetto parziale, suggerendo che più membri della famiglia possono cooperare ma che GABARAPL1 svolge un ruolo primario.
Cosa significa per la protezione cellulare
Complessivamente, lo studio propone che GABARAPL1 sia un aiuto finora non riconosciuto nella via di stress indotta dall'arsenito. Agendo come cofattore per HSP90, supporta la piena attivazione di HRI, che a sua volta modifica eIF2α, rallenta la produzione proteica e guida la formazione di granuli di stress protettivi. In assenza di GABARAPL1 questa catena di eventi è indebolita, lasciando le cellule meno reattive all'arsenito e alterando l'equilibrio tra sopravvivenza e danno. Questi approfondimenti arricchiscono la nostra comprensione di come le cellule interpretano minacce ambientali specifiche e potrebbero orientare ricerche future sull'esposizione a tossici, sulla resistenza delle cellule tumorali e sulle terapie che mirano ai percorsi di risposta allo stress cellulare.
Citazione: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Parole chiave: risposta cellulare allo stress, tossicità da arsenico, granuli di stress, controllo della qualità delle proteine, proteine correlate all'autofagia