Clear Sky Science · fr
GABARAPL1 est important pour l’activation de HRI lors de la réponse au stress dépendante de la phosphorylation de eIF2α en présence d’arsénite de sodium
Pourquoi cela importe pour nos cellules en situation de stress
Chaque jour, nos cellules sont bombardées par des stress environnementaux, y compris des métaux toxiques tels que l’arsenic. Pour survivre, elles doivent rapidement ralentir leurs activités normales et passer en mode contrôle des dommages. Cette étude met en lumière un acteur inattendu, une protéine appelée GABARAPL1, qui aide les cellules à détecter le stress induit par l’arsenite et à décider de suspendre la production de protéines et de protéger leurs messages génétiques. Comprendre ce garde-fou caché peut éclairer la manière dont les cellules font face à la pollution, pourquoi certaines deviennent plus résistantes aux toxines, et comment les voies de contrôle du stress peuvent dysfonctionner dans les maladies.
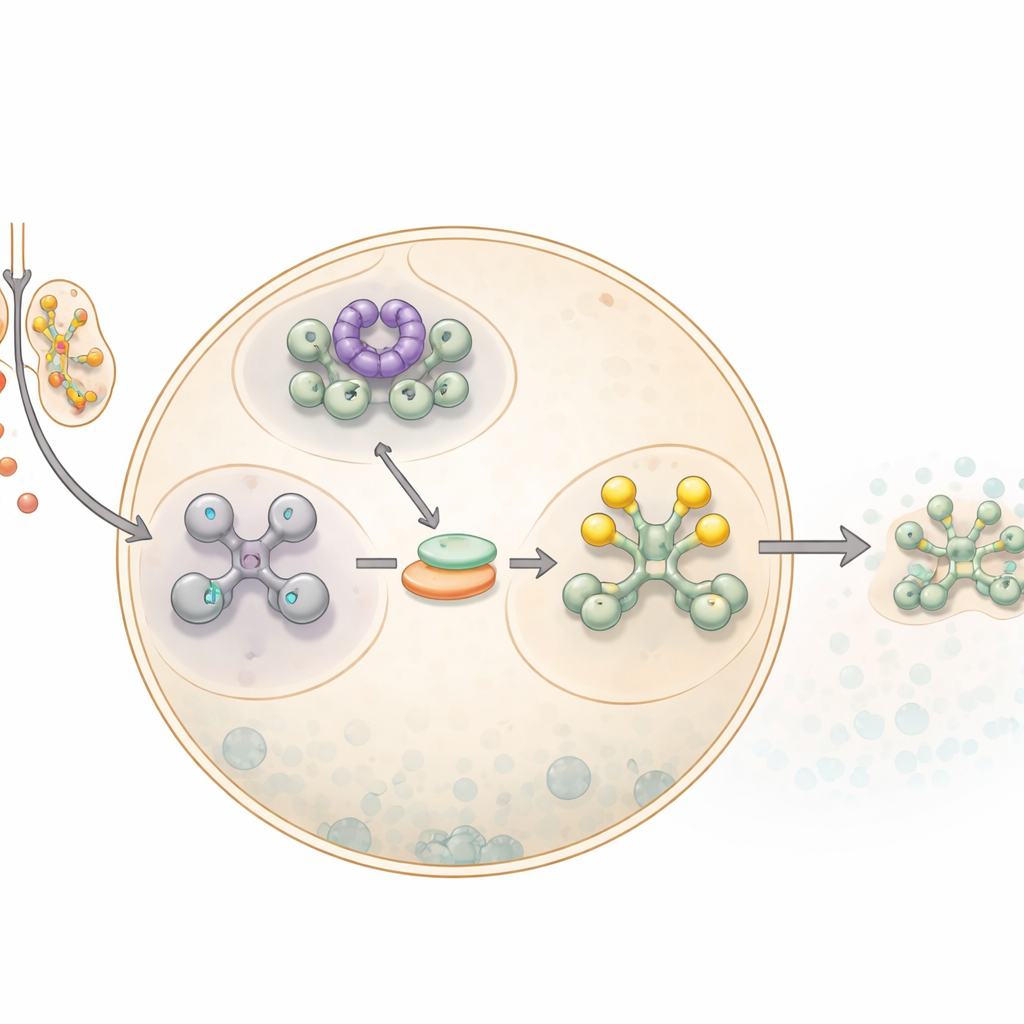
Comment les cellules appuient sur le bouton pause
Lorsque les cellules rencontrent de l’arsénite de sodium, une forme d’arsenic, elles activent un réseau d’alerte plus large connu sous le nom de réponse intégrée au stress. Une étape clé de cette réponse est l’arrêt de la majeure partie de la production protéique. Cela se fait par la modification d’un facteur central de la traduction, eIF2α, qui aide normalement à initier la synthèse des protéines à partir des ARN messagers. Une fois eIF2α chimiquement marqué, ou phosphorylé, la cellule ralentit la fabrication générale de protéines et redirige les ARNm inutilisés vers des gouttelettes denses appelées granules de stress. Ces granules servent de sites de stockage temporaires, protégeant les ARN jusqu’à ce que le danger soit passé et donnant à la cellule le temps de reprogrammer les protéines qu’elle produit.
Un rôle surprenant pour une protéine de recyclage
GABARAPL1 appartient à une famille de protéines surtout connue pour l’autophagie, le système interne de recyclage cellulaire qui dégrade les composants indésirables. Les chercheurs ont travaillé sur des cellules humaines de cancer du poumon et ont éliminé GABARAPL1 par édition génétique ou par silencement. Ils ont ensuite exposé les cellules à l’arsénite et observé les conséquences. Dans les cellules normales, l’arsénite déclenchait rapidement la formation de granules de stress et une forte phosphorylation de eIF2α, cohérentes avec une réponse au stress robuste. Par contraste frappant, les cellules dépourvues de GABARAPL1 formaient beaucoup moins de granules de stress et ne présentaient qu’une faible phosphorylation de eIF2α, bien que l’arsénite pénètre clairement dans les cellules et active d’autres voies de signalisation.
Identifier le maillon défaillant de la chaîne d’alerte
Pour comprendre où la chaîne d’alerte déraillait, l’équipe s’est concentrée sur HRI, une kinase qui se situe en amont d’eIF2α et est spécifiquement activée par le stress oxydatif lié à l’arsénite. Ils ont constaté que les étapes précoces d’activation de HRI, impliquant une auto-modification de la protéine, se produisaient encore dans les cellules sans GABARAPL1. Cependant, une étape ultérieure et cruciale était altérée : le partenariat efficace entre HRI et une protéine chaperonne appelée HSP90, qui aide HRI à atteindre sa forme pleinement active. En utilisant une méthode d’imagerie détectant la proximité entre deux protéines, les chercheurs ont observé que, sous stress par l’arsénite, HSP90 et HRI se réassociaient au fil du temps dans les cellules normales mais ne le faisaient pas correctement lorsque GABARAPL1 manquait. Cela suggère que GABARAPL1 agit comme une sorte d’échafaudage qui rapproche HSP90 et HRI au bon moment.
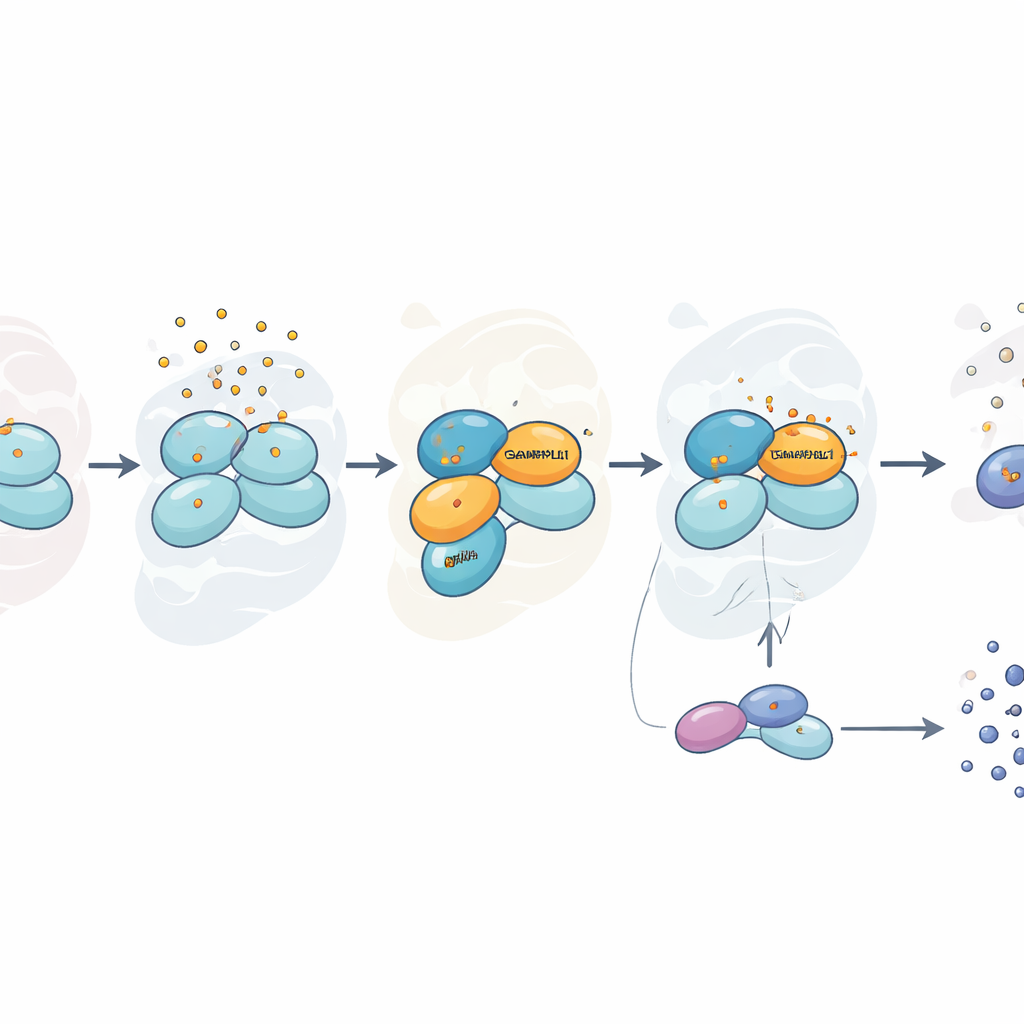
Un stress sélectif, pas universel
Fait intéressant, cette dépendance à GABARAPL1 était spécifique à l’arsénite. Lorsque les chercheurs ont soumis les cellules à du sorbitol, qui modifie l’équilibre hydrique cellulaire, ou au peroxyde d’hydrogène, une autre source de dommages oxydatifs, la phosphorylation d’eIF2α et la formation de granules de stress se déroulaient normalement même en l’absence de GABARAPL1. En présence d’arsénite, en revanche, les cellules sans GABARAPL1 non seulement montaient une réponse au stress plus faible mais semblaient aussi plus résistantes à la toxine lors de tests de viabilité, probablement parce qu’elles réduisaient leur activité métabolique et évitaient une partie des dommages associés à une réaction d’alarme intense. Une autre protéine apparentée de la même famille, LC3B, montrait un effet seulement partiel, laissant entendre que plusieurs membres de la famille peuvent coopérer mais que GABARAPL1 joue un rôle de premier plan.
Ce que cela signifie pour la protection cellulaire
En synthèse, l’étude propose que GABARAPL1 est un auxiliaire jusque-là méconnu de la voie de stress induite par l’arsénite. En servant de cofacteur pour HSP90, il favorise l’activation complète de HRI, qui à son tour modifie eIF2α, ralentit la production protéique et favorise la formation de granules de stress protecteurs. En l’absence de GABARAPL1, cette chaîne d’événements est affaiblie, laissant les cellules moins réactives à l’arsénite et modifiant leur équilibre entre survie et dégâts. Ces éléments approfondissent notre compréhension de la façon dont les cellules interprètent des menaces environnementales spécifiques et peuvent orienter de futures recherches sur l’exposition aux toxiques, la résistance des cellules cancéreuses et des thérapies ciblant les réponses cellulaires au stress.
Citation: Campenet, S., Lamarre, M., Durand, J. et al. GABARAPL1 is important for the activation of HRI during eIF2α phosphorylation-dependent stress response to sodium arsenite. Sci Rep 16, 10818 (2026). https://doi.org/10.1038/s41598-026-44621-2
Mots-clés: réponse cellulaire au stress, toxicité de l’arsenic, granules de stress, contrôle de la qualité des protéines, protéines liées à l’autophagie