Clear Sky Science · zh
用于光学相干断层扫描B扫中视网膜层与液体分割的多尺度自适应融合网络
为日常视力护理带来更清晰的眼底扫描
糖尿病和年龄相关性黄斑变性等疾病可以在我们察觉视觉改变之前,悄然损伤眼后方的感光组织——视网膜。被称为光学相干断层扫描(OCT)的现代扫描仪已能为医生提供视网膜的精细横截面视图,但人工解读这些图像既耗时又可能漏掉细微的预警信号。本研究提出了一种先进的计算系统 AMDF‑Net,旨在自动精确勾画视网膜的薄层结构和液体囊腔,从而有望加速并提高致盲性眼病的诊断和随访可靠性。
为何眼内液体如此重要
在多种常见眼病中——包括糖尿病性黄斑水肿、年龄相关性黄斑变性以及视网膜静脉或神经问题——都会出现视网膜内或视网膜下的微小液体积聚。其大小、形状与精确位置可告诉医生治疗是否有效或疾病是否在恶化。OCT 图像可详细捕捉这些特征,但视网膜由许多纸片般薄的层组成,层与层之间弯曲并重叠,液体会模糊边界并呈现不规则团块。传统计算程序,甚至早期的深度学习工具,在图像噪声大、对比度低或疾病表现异常时,常难以正确区分这些层与液体。
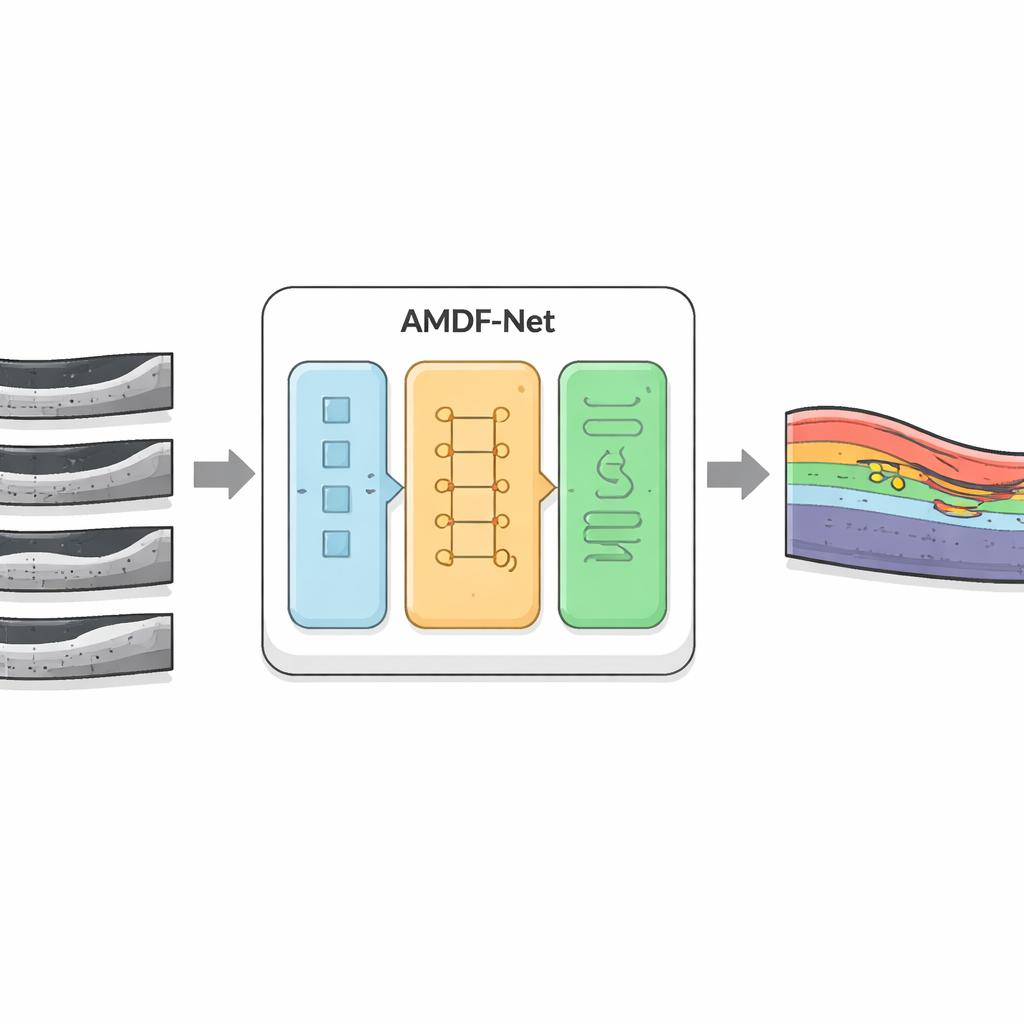
为OCT图像设计的新型数字助手
研究人员开发了 AMDF‑Net(自适应多域融合网络)以应对这些挑战。系统首先对原始 OCT 眼底扫描进行预处理:增强边缘、降低噪声并匹配亮度,使微弱结构更易辨识且不同扫描仪生成的图像更统一。随后数据通过两条互补通路:一条关注局部细节,例如层间的薄边界;另一条分析整幅扫描的广域模式,捕捉层的弯曲形态与液体聚集的趋势。一个特殊的融合模块将这两种视角合并,并采用注意力机制——本质上是一种自动对信息丰富区域“给予更多关注”的方法——突出那些更可能代表病变组织的特征。
同时观察解剖结构与疾病信号
除了勾勒正常解剖外,AMDF‑Net 包含一个面向疾病的模块,专门针对真实患者中出现的模式进行调优,例如视网膜内与视网膜下的液体囊腔或支持组织剥离的区域。该网络部分在训练过程中学习强调常见的病变影像模式,同时仍保持对正常层结构的识别。系统由精心设计的损失函数引导——该函数是一种模型试图优化的数学评分,既奖励区域填充的准确性,也奖励边界的清晰。通过在学习过程中结合基于区域和关注边缘的反馈,模型被推动生成不仅与专家标注高度重叠,而且轮廓平滑、具有临床意义的分割结果。
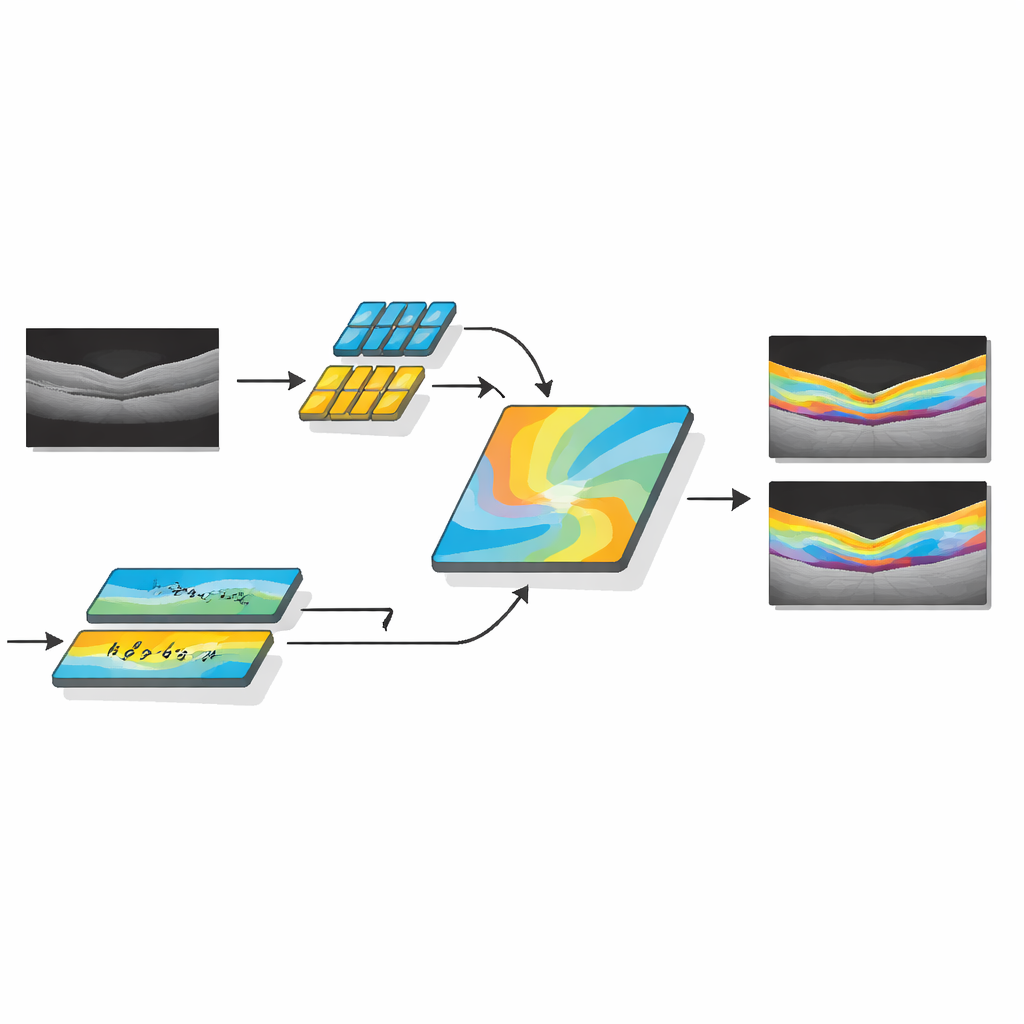
在多名患者与多种扫描仪上验证
为评估 AMDF‑Net 在实际中的表现,作者将其测试于三个知名的公开 OCT 数据集以及来自一家繁忙眼科医院的真实临床数据集。这些数据集涵盖不同疾病、不同品牌的扫描仪和多样的图像质量,包含特别棘手的视神经周围区域及许多算法易遗漏的微小液体囊腔。在所有测试中,AMDF‑Net 始终能与领先方法持平或优于它们,将常用准确度指标提高约三到五个百分点,并减少诸如断裂的层线或被误识为液体的错判等可见错误。重要的是,该系统在处理来自不同厂商的图像时性能仅有小幅下降,这对于最终在日常临床中部署至关重要。
对患者与临床的意义
对非专业读者而言,核心信息是 AMDF‑Net 类似一位训练有素的数字助手,能够快速且可靠地在 OCT 扫描中描绘视网膜结构与病灶。通过对大量图像进行此类处理,它可帮助眼科医生更早发现疾病、追踪就诊间的细微变化并更精确地制定治疗方案,即便在繁忙或资源有限的环境中亦然。尽管该方法目前比更简单的模型需要更多计算资源,作者指出未来通过模型改进与压缩技术可以将其加速到适合常规椅旁使用的水平。长期来看,像 AMDF‑Net 这样的工具可能通过将复杂的眼部扫描转化为清晰、可操作的视网膜健康地图,帮助保护视力。
引用: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
关键词: 光学相干断层扫描, 视网膜疾病, 深度学习分割, 医学影像人工智能, 黄斑水肿