Clear Sky Science · sv
Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans
Skarpare ögonavbildningar för vardaglig synvård
Sjukdomar som diabetes och åldersrelaterad makuladegeneration kan i det tysta skada näthinnan, det ljuskänsliga vävnadsskiktet längst bak i ögat, långt innan vi märker förändringar i synen. Moderna skannrar kallade optisk koherenstomografi (OCT) ger redan läkare detaljerade tvärsnittsbilder av näthinnan, men att tolka dessa bilder manuellt är tidsödande och kan missa subtila varningstecken. I den här studien presenteras ett avancerat computersystem, AMDF‑Net, utformat för att automatiskt följa näthinnans fina lager och vätskefickor med hög precision, vilket potentiellt möjliggör snabbare och mer pålitlig diagnos och uppföljning av blindaskapande ögonsjukdomar.
Varför ögonvätska är så viktig
I flera vanliga ögontillstånd—inklusive diabetiskt makulaödem, åldersrelaterad makuladegeneration och problem med näthinnans vener eller nerver—bildas små vätskepooler i eller under näthinnan. Deras storlek, form och exakta läge ger läkare vägledning om en behandling fungerar eller om sjukdomen förvärras. OCT‑bilder fångar dessa egenskaper i stor detalj, men näthinnan består av många pappers‑tunna lager som böjer sig och överlappar. Vätska kan sudda ut gränserna och uppträda i oregelbundna klumpar. Traditionella datorprogram och även tidigare djupinlärningsverktyg har ofta svårt att korrekt separera dessa lager och vätskor när bilder är brusiga, kontrasten är låg eller sjukdomsmönstret är ovanligt.
En ny digital assistent för OCT‑bilder
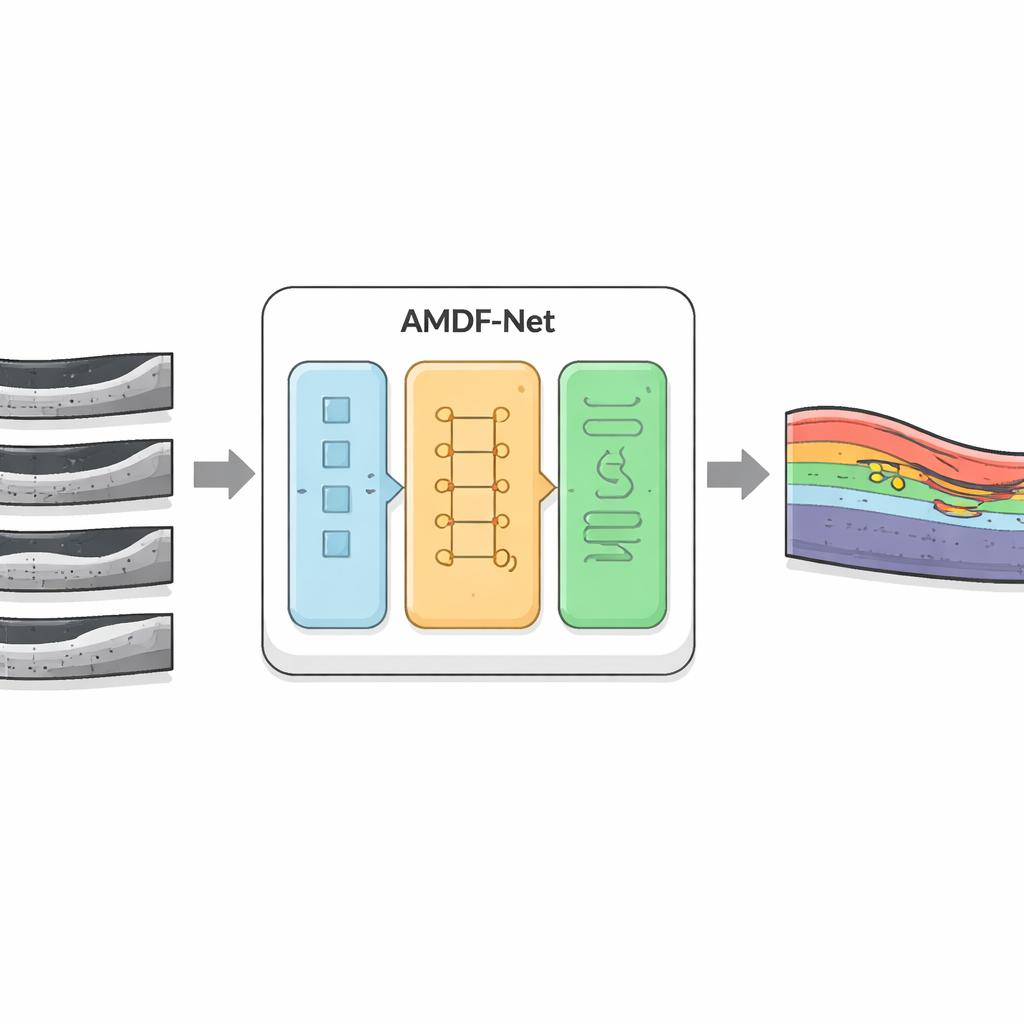
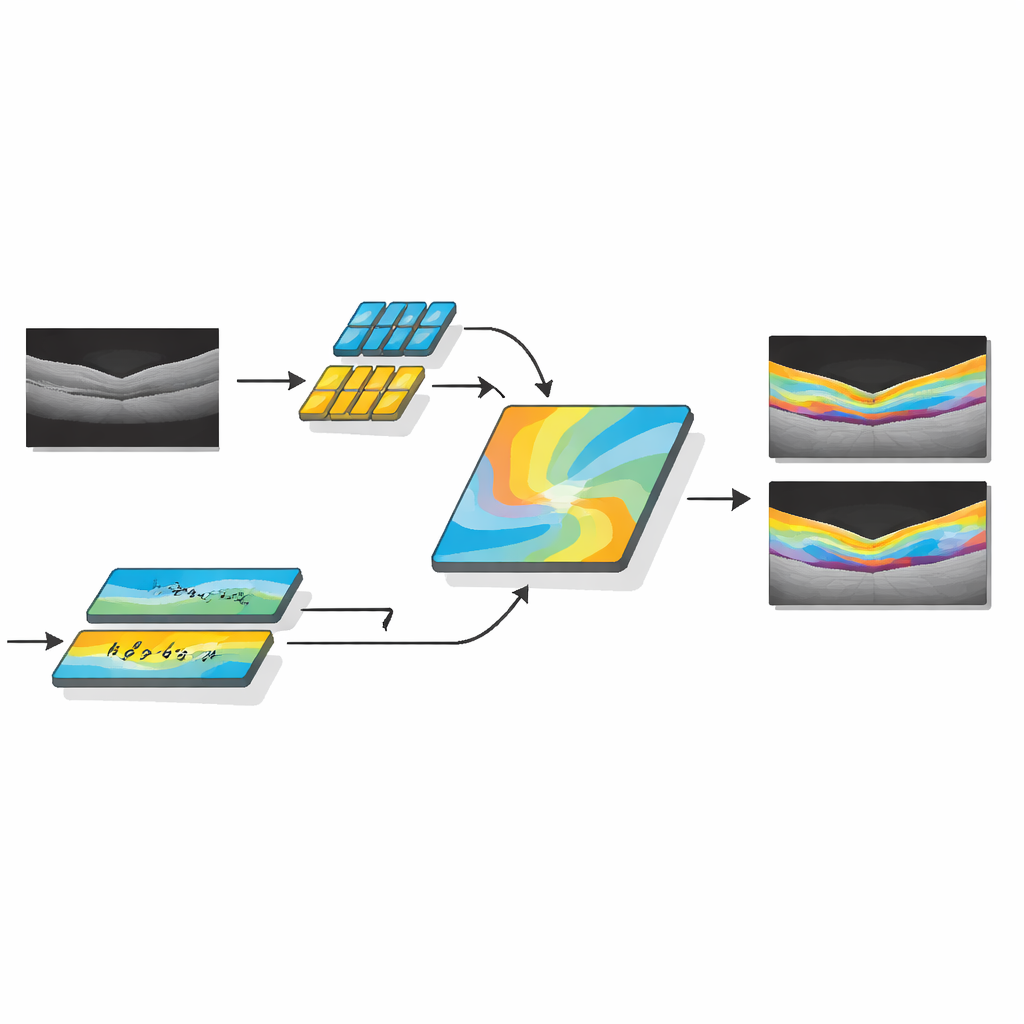
Forskarna utvecklade AMDF‑Net (Adaptive Multi‑Domain Fusion Network) för att möta dessa utmaningar direkt. Systemet tar råa OCT‑skanningar av ögat och förbehandlar dem först med kantförstärkning, brusreducering och ljushetsanpassning så att subtila strukturer framträder och bilder från olika skannrar blir mer jämförbara. Därefter behandlas data via två kompletterande banor: den ena fokuserar på små lokala detaljer som tunna gränser mellan lager, medan den andra analyserar bredare mönster över hela skanningen, fångar hur lagren böjer sig och var vätska tenderar att samlas. Ett särskilt fusionsblock kombinerar dessa två vyer och använder en uppmärksamhetsmekanism—i praktiken ett sätt att automatiskt ”ge mer uppmärksamhet” åt informativa regioner—för att lyfta fram egenskaper som särskilt sannolikt representerar sjuk vävnad.
Att se både anatomi och sjukdom samtidigt
Utöver att bara avgränsa normal anatomi inkluderar AMDF‑Net en sjukdoms‑inklusiv modul som är finjusterad för mönster som ses hos verkliga patienter, såsom intraretinala och subretinala vätskefickor eller områden där stödjevävnaden lyft sig. Denna del av nätverket lär sig under träningen att betona bildmönster som ofta signalerar sjukdom, samtidigt som den behåller överblick över normal lagerstruktur. Systemet styrs av en noggrant utformad förlustfunktion—en matematisk poäng den försöker optimera—som belönar både korrekt områdesfyllning och skarpa gränser. Genom att kombinera områdesbaserad och kantfokuserad återkoppling under inlärningen pressas modellen att leverera segmenteringar som inte bara överlappar väl med expertmarkeringar utan också har släta, kliniskt meningsfulla konturer.
Testad på många patienter och skannrar
För att bedöma hur väl AMDF‑Net fungerar i praktiken testade författarna det på tre välkända publika OCT‑datamängder och en verklig klinisk datamängd från ett upptaget ögonsjukhus. Dessa set täcker olika sjukdomar, skannermärken och bildkvaliteter, inklusive särskilt knepiga regioner runt synnerven och små vätskefickor som många algoritmer missar. I samtliga fall matchade eller överträffade AMDF‑Net konsekvent ledande metoder och förbättrade vanliga noggrannhetspoäng med ungefär tre till fem procentenheter samtidigt som synliga fel som brutna lagerlinjer eller felidentifierade vätskeklumpar minskade. Viktigt är att systemet hanterade bilder från olika tillverkare med endast små prestandafall, en nyckelförutsättning för framtida användning i vardagskliniker.
Vad detta betyder för patienter och kliniker
För icke‑specialister är kärnbudskapet att AMDF‑Net fungerar som en högt utbildad digital assistent som snabbt och pålitligt kan följa näthinnans struktur och problemområden i OCT‑bilder. Genom att tillämpas på stora mängder bilder kan det hjälpa ögonläkare att upptäcka sjukdom tidigare, följa subtila förändringar mellan besök och skräddarsy behandlingar mer precist, även i hektiska eller resursbegränsade miljöer. Medan metoden idag kräver mer beräkningskraft än enklare modeller noterar författarna att framtida förfiningar och komprimeringstekniker kan göra den snabb nog för rutinmässig användning vid patientstolen. På längre sikt kan verktyg som AMDF‑Net bidra till att bevara synen genom att omvandla komplexa ögonskanningar till tydliga, handlingsbara kartor över näthinnehälsa.
Citering: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Nyckelord: optical coherence tomography, retinal disease, deep learning segmentation, medical imaging AI, macular edema