Clear Sky Science · ru
Адаптивная сеть мультимасштабного слияния для сегментации слоёв сетчатки и жидкости на B‑срезах оптической когерентной томографии
Более чёткие сканы глаза для повседневной офтальмологической практики
Такие заболевания, как диабет и возрастная макулярная дегенерация, могут незаметно повреждать сетчатку — светочувствительную ткань на задней стенке глаза — задолго до того, как мы заметим ухудшение зрения. Современные сканеры оптической когерентной томографии (ОКТ) уже дают врачам подробные поперечные срезы сетчатки, но ручная интерпретация этих изображений медленна и может упускать тонкие признаки. В этом исследовании представлен усовершенствованный вычислительный инструмент AMDF‑Net, предназначенный для автоматического выделения тонких слоёв сетчатки и локусов жидкости с высокой точностью, что потенциально позволяет ускорить и сделать более надёжной диагностику и наблюдение угрожающих слепотой заболеваний глаз.
Почему жидкость в глазу так важна
При ряде распространённых заболеваний глаза — в том числе при диабетическом макулярном отёке, возрастной макулярной дегенерации и нарушениях вен или нервов сетчатки — в пределах или под сетчаткой образуются крошечные скопления жидкости. Их размер, форма и точное расположение помогают врачам понять, работает ли лечение или прогрессирует ли болезнь. ОКТ‑изображения фиксируют эти особенности в деталях, но сама сетчатка состоит из множества бумажно‑тонких слоёв, которые изгибаются и перекрываются. Жидкость размывает границы и может проявляться в виде неправильных пятен. Традиционные алгоритмы и даже ранние модели глубокого обучения часто испытывают трудности с корректным разделением слоёв и жидкости, когда изображения шумны, контраст низкий или паттерн болезни нетипичен.
Новый цифровой помощник для ОКТ‑сканов
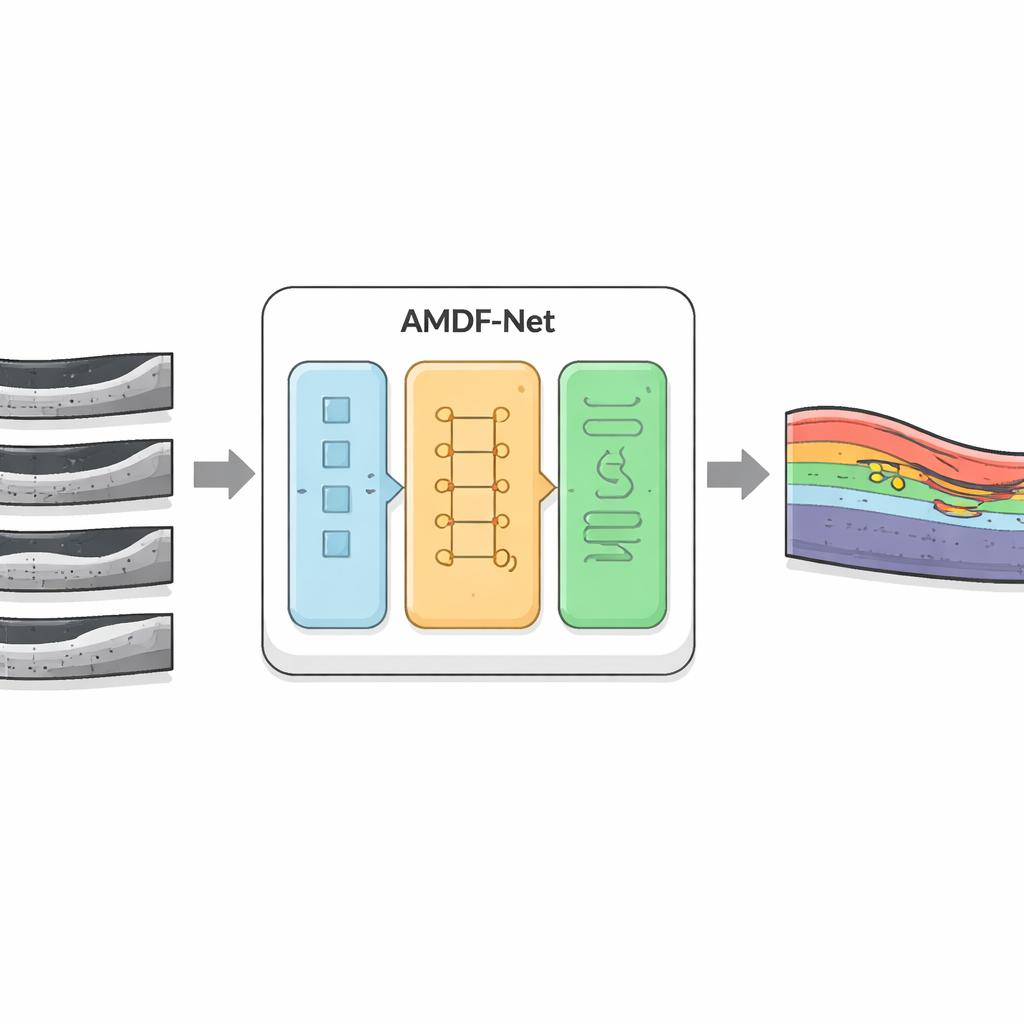
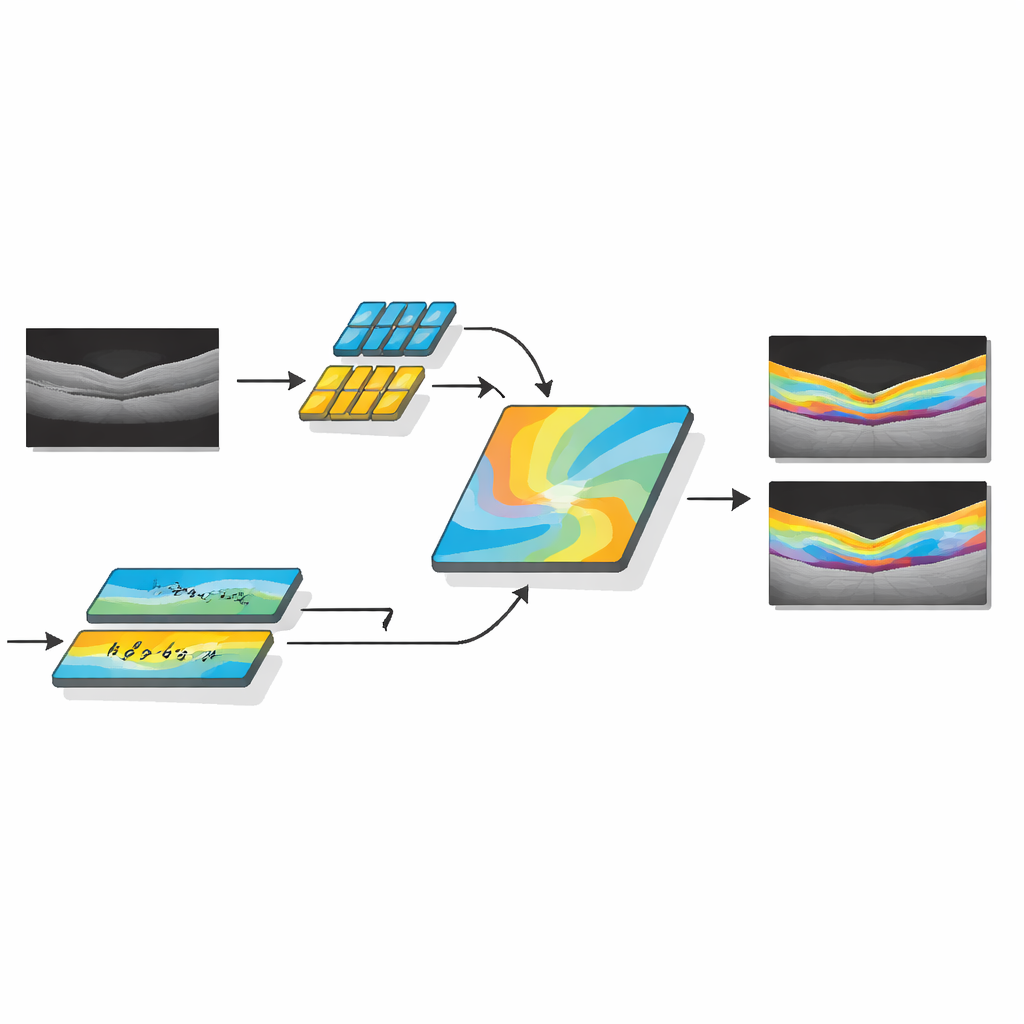
Исследователи разработали AMDF‑Net (Adaptive Multi‑Domain Fusion Network), чтобы напрямую решать эти задачи. Система принимает исходные ОКТ‑сканы и сначала улучшает их с помощью усиления краёв, подавления шума и выравнивания яркости, чтобы тонкие структуры стали более заметны, а изображения с разных аппаратов выглядели более сопоставимо. Затем данные проходят по двум дополняющимся путям: один сосредоточен на мелких локальных деталях, таких как тонкие границы между слоями, а другой анализирует более широкие паттерны по всему срезу, улавливая, как изгибаются слои и где обычно скапливается жидкость. Специальный блок слияния объединяет эти два представления и применяет механизм внимания — по сути, способ автоматически «уделять больше внимания» информативным областям — чтобы выделить признаки, особенно вероятно указывающие на патологию.
Совместный анализ анатомии и признаков болезни
Помимо простого выделения нормальной анатомии, AMDF‑Net включает модуль, ориентированный на проявления заболеваний, настроенный на паттерны, встречающиеся у реальных пациентов, такие как внутритканевая и субретинальная жидкость или участки отслоения поддерживающей ткани. Эта часть сети в процессе обучения учится подчёркивать образцы изображения, которые обычно сигнализируют о болезни, при этом сохраняя учёт нормальной структуры слоёв. Система управляется специально сконструированной функцией потерь — математическим показателем, который модель стремится оптимизировать — которая поощряет и точное заполнение областей, и чёткие границы. Сочетая обратную связь, ориентированную на регионы, и на края, модель оказывается настроенной так, чтобы выдавать сегментации, не только хорошо совпадающие с разметкой экспертов, но и обладающие гладкими, клинически значимыми контурами.
Проверено на больших наборах пациентов и разных сканерах
Чтобы оценить практическую эффективность AMDF‑Net, авторы протестировали её на трёх хорошо известных общественных коллекциях ОКТ и на реальном клиническом наборе данных из загруженной офтальмологической клиники. Эти наборы охватывают разные заболевания, марки сканеров и качества изображений, включая особенно сложные области вокруг зрительного нерва и крошечные скопления жидкости, которые многие алгоритмы пропускают. Во всех случаях AMDF‑Net стабильно сравнялась или превзошла ведущие методы, улучшив распространённые метрики точности примерно на три‑пять процентных пункта и уменьшив видимые ошибки, такие как разрывные линии слоёв или неверно распознанные участки жидкости. Важно, что система справлялась с изображениями от разных производителей с лишь незначительным падением производительности — ключевым требованием для возможного использования в повседневной клинике.
Что это значит для пациентов и клиник
Для непрофессионалов основной вывод таков: AMDF‑Net действует как высококвалифицированный цифровой ассистент, который быстро и надёжно трассирует структуру сетчатки и проблемные зоны на ОКТ‑сканах. Обрабатывая большие объёмы изображений, он может помочь офтальмологам раньше выявлять болезни, отслеживать тонкие изменения между визитами и точнее подбирать лечение, даже в загруженных или с ограниченными ресурсами условиях. Хотя метод сейчас требует больше вычислительных ресурсов, чем более простые модели, авторы отмечают, что будущие доработки и техники сжатия могут сделать его достаточно быстрым для рутинного использования у кресла пациента. В долгосрочной перспективе инструменты вроде AMDF‑Net могут помочь сохранить зрение, превращая сложные сканы глаза в понятные и применимые карты состояния сетчатки.
Цитирование: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Ключевые слова: оптическая когерентная томография, заболевания сетчатки, глубокое обучение — сегментация, ИИ для медицинской визуализации, макулярный отёк