Clear Sky Science · it
Rete adattiva multi-scala per la fusione nella segmentazione degli strati retinici e dei fluidi nelle B-scan di tomografia a coerenza ottica
Esami oculari più nitidi per la cura della vista di tutti i giorni
Malattie come il diabete e la degenerazione maculare legata all’età possono danneggiare silenziosamente la retina, il tessuto fotosensibile sul fondo dell’occhio, molto prima che si notino cambiamenti nella vista. Gli scanner moderni chiamati tomografia a coerenza ottica (OCT) forniscono già ai medici viste tomografiche dettagliate della retina, ma interpretare queste immagini manualmente è lento e può far perdere segnali d’allarme sottili. Questo studio presenta un sistema computerizzato avanzato, AMDF‑Net, progettato per tracciare automaticamente gli strati delicati della retina e le sacche di fluido con elevata precisione, permettendo potenzialmente diagnosi e monitoraggi più rapidi e affidabili delle malattie oculari che possono portare alla cecità.
Perché il fluido oculare è così importante
In diverse patologie oculari comuni — tra cui l’edema maculare diabetico, la degenerazione maculare legata all’età e problemi delle vene o dei nervi retinici — si formano piccole raccolte di fluido all’interno o sotto la retina. Dimensione, forma e posizione esatta di queste sacche informano il medico se un trattamento sta funzionando o se la malattia sta peggiorando. Le immagini OCT catturano questi elementi con grande dettaglio, ma la retina è composta da molti strati sottilissimi che si curvano e si sovrappongono. Il fluido può sfumare i confini e presentarsi come ammassi irregolari. I programmi tradizionali e persino strumenti di deep learning più datati spesso faticano a separare correttamente strati e fluidi quando le immagini sono rumorose, il contrasto è basso o il quadro patologico è atipico.
Un nuovo assistente digitale per le immagini OCT
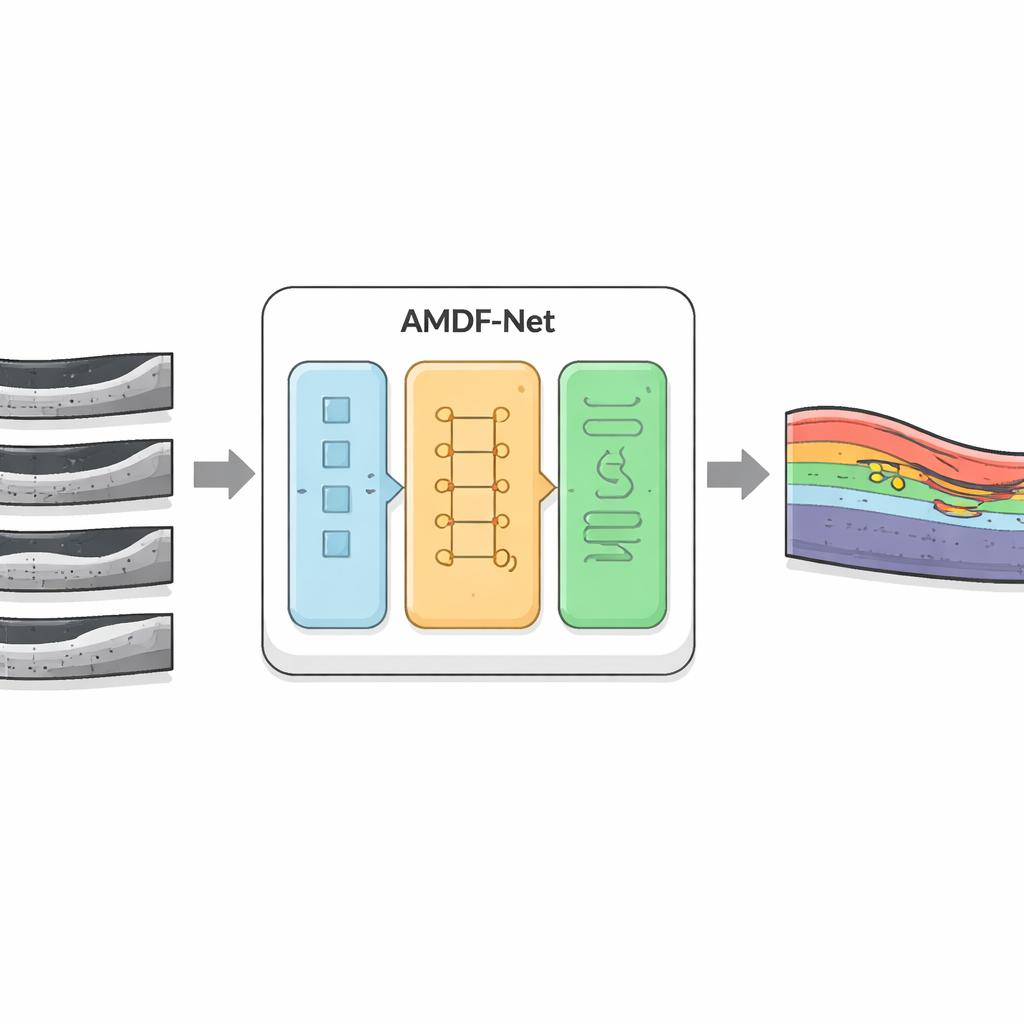
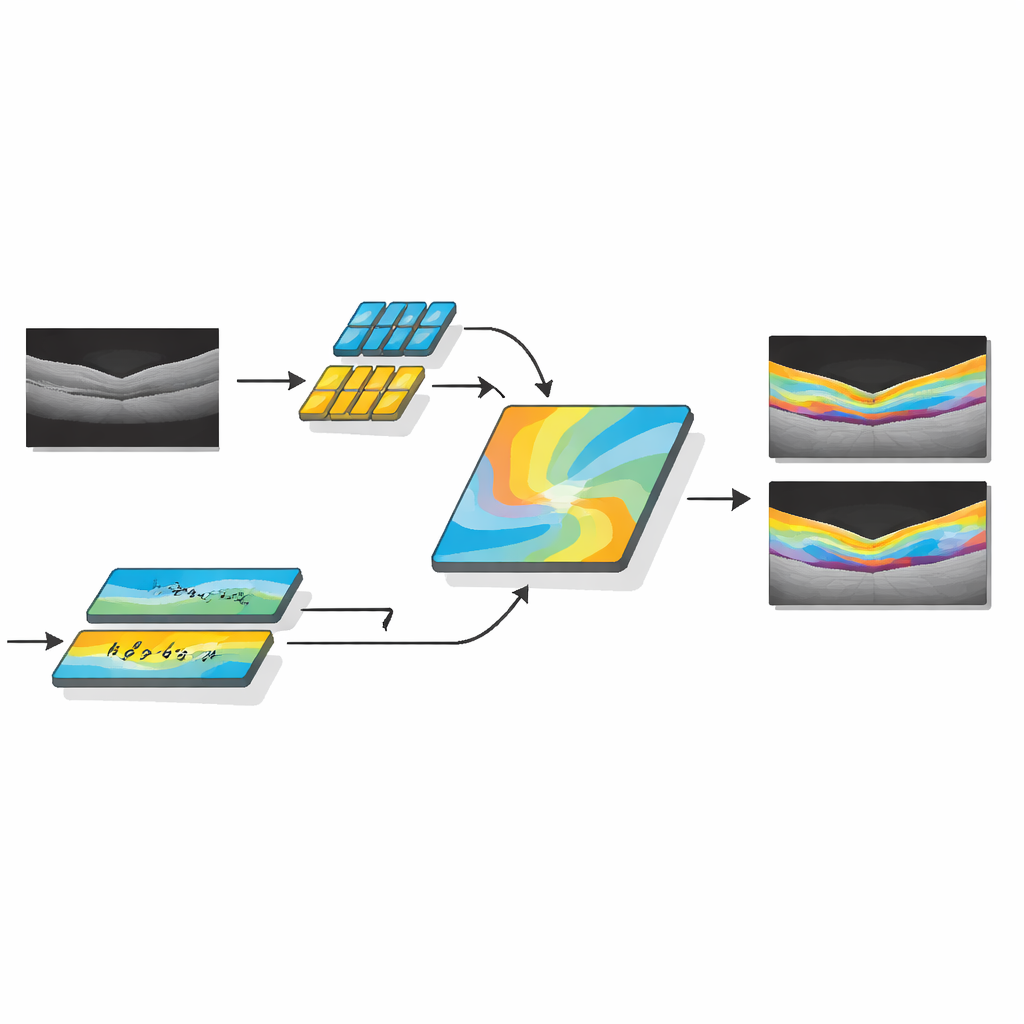
I ricercatori hanno sviluppato AMDF‑Net (Adaptive Multi‑Domain Fusion Network) per affrontare direttamente queste difficoltà. Il sistema prende in input scansioni OCT grezze e prima le pulisce usando miglioramento dei bordi, riduzione del rumore e allineamento della luminosità, in modo che le strutture sottili emergano e le immagini provenienti da scanner diversi risultino più uniformi. Poi elabora i dati attraverso due percorsi complementari: uno si concentra sui piccoli dettagli locali, come i confini sottili tra gli strati, mentre l’altro analizza schemi più ampi sull’intera scansione, catturando come gli strati si curvano e dove il fluido tende ad accumularsi. Un blocco di fusione speciale combina queste due visuali e usa un meccanismo di attenzione — sostanzialmente un modo per “prestare più attenzione” automaticamente alle regioni informative — per mettere in risalto le caratteristiche che molto probabilmente rappresentano tessuto malato.
Vedere insieme anatomia e patologia
Oltre a delineare semplicemente l’anatomia normale, AMDF‑Net include un modulo sensibile alla patologia tarato su schemi osservati in pazienti reali, come sacche di fluido intraretinico e subretinico o aree in cui il tessuto di supporto si è sollevato. Questa parte della rete apprende, durante l’addestramento, a enfatizzare i pattern di immagine che indicano comunemente malattia, mantenendo al contempo la struttura normale degli strati. Il sistema è guidato da una funzione di perdita accuratamente progettata — un punteggio matematico che cerca di ottimizzare — che premia sia il riempimento corretto delle regioni sia bordi netti. Combinando feedback basati sulla regione e focalizzati sui bordi durante l’apprendimento, il modello viene spinto a produrre segmentazioni che non solo si sovrappongono bene alle marcature di esperti, ma presentano anche contorni lisci e clinicamente significativi.
Testato su molti pazienti e scanner
Per valutare le prestazioni di AMDF‑Net nella pratica, gli autori lo hanno testato su tre collezioni OCT pubbliche ben note e su un dataset clinico reale proveniente da un affollato ospedale oculistico. Questi set coprono diverse malattie, marche di scanner e qualità d’immagine, incluse regioni particolarmente insidiose attorno al nervo ottico e piccole sacche di fluido che molti algoritmi perdono. In tutti i casi, AMDF‑Net ha costantemente eguagliato o superato i metodi di punta, migliorando gli score di accuratezza comuni di circa tre‑cinque punti percentuali e riducendo errori visibili come linee di strati interrotte o bolle di fluido mal identificate. È importante che il sistema abbia gestito immagini di diversi produttori con solo lievi cali di prestazione, requisito chiave per un uso futuro nelle cliniche quotidiane.
Cosa significa per pazienti e cliniche
Per i non specialisti, il messaggio principale è che AMDF‑Net funziona come un assistente digitale altamente addestrato che può tracciare in modo rapido e affidabile la struttura retinica e i punti problematici nelle scansioni OCT. Applicandolo a grandi volumi di immagini, potrebbe aiutare gli oculisti a individuare la malattia prima, monitorare cambiamenti sottili tra le visite e personalizzare i trattamenti con maggiore precisione, anche in contesti affollati o con risorse limitate. Sebbene il metodo richieda attualmente più potenza di calcolo rispetto a modelli più semplici, gli autori osservano che perfezionamenti futuri e tecniche di compressione potrebbero renderlo abbastanza veloce per l’uso di routine a bordo sedia. A lungo termine, strumenti come AMDF‑Net potrebbero contribuire a preservare la vista trasformando esami complessi in mappe chiare e utilizzabili della salute retinica.
Citazione: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Parole chiave: tomografia a coerenza ottica, malattie retiniche, segmentazione con deep learning, IA per immagini mediche, edema maculare