Clear Sky Science · nl
Multi-scale adaptive fusion network voor segmentatie van netvlieslagen en vloeistof in optische coherentietomografie B-scans
Scherpere oogscans voor dagelijkse oogzorg
Ziekten zoals diabetes en leeftijdsgebonden maculadegeneratie kunnen het netvlies, het lichtgevoelige weefsel achter in het oog, geruisloos beschadigen lang voordat we veranderingen in het zicht opmerken. Moderne scanners, optische coherentietomografie (OCT) genoemd, geven artsen al gedetailleerde dwarsdoorsneden van het netvlies, maar het handmatig interpreteren van deze beelden is traag en kan subtiele waarschuwingssignalen missen. Deze studie introduceert een geavanceerd computersysteem, AMDF‑Net, dat ontworpen is om automatisch de fragiele lagen van het netvlies en vochtophopingen met hoge precisie te volgen, wat mogelijk snellere en betrouwbaardere diagnose en monitoring van blindheid veroorzakende oogziekten mogelijk maakt.
Waarom oogsvocht zo belangrijk is
Bij meerdere veelvoorkomende oogaandoeningen — waaronder diabetisch macula-oedeem, leeftijdsgebonden maculadegeneratie en problemen met de retinale vene of zenuw — kunnen kleine plasjes vocht zich binnen of onder het netvlies vormen. Hun grootte, vorm en exacte locatie vertellen artsen of een behandeling werkt of een ziekte verergert. OCT-beelden leggen deze kenmerken in groot detail vast, maar het netvlies bestaat uit vele papierdunne lagen die krommen en elkaar overlappen. Vloeistof kan grenzen vervagen en in onregelmatige vlekken verschijnen. Traditionele computerprogramma’s, en zelfs eerdere deep‑learning‑hulpmiddelen, hebben vaak moeite om deze lagen en vochtophopingen correct te scheiden wanneer beelden ruisig zijn, het contrast laag is of het ziektepatroon ongebruikelijk is.
Een nieuwe digitale assistent voor OCT-beelden
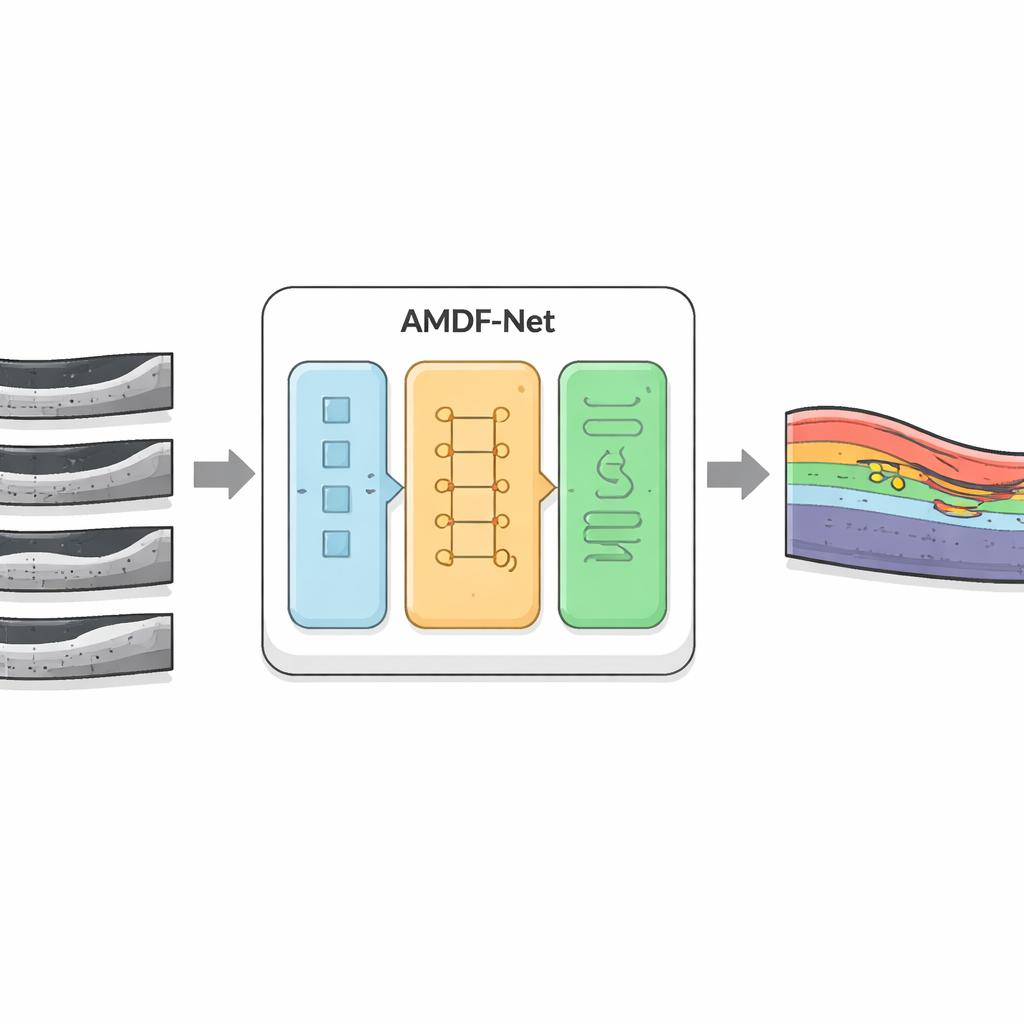
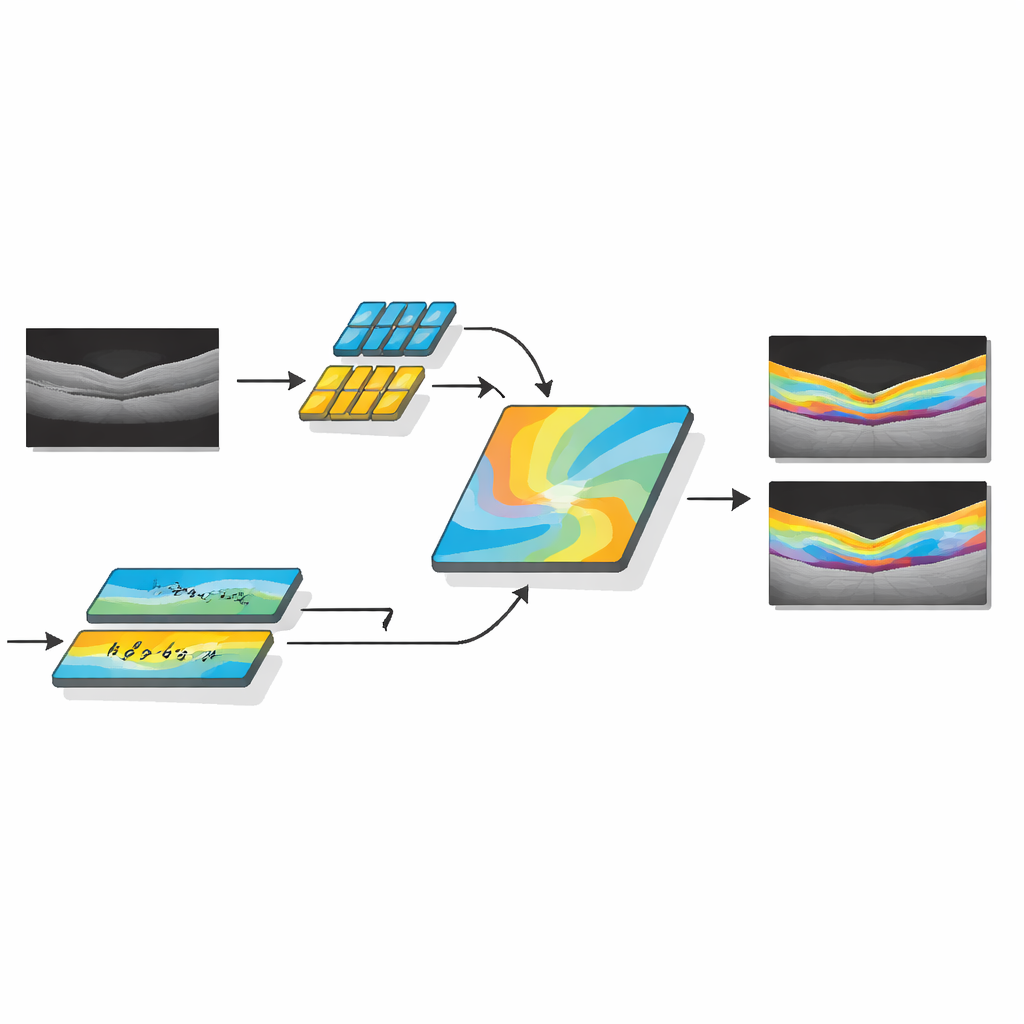
De onderzoekers ontwikkelden AMDF‑Net (Adaptive Multi‑Domain Fusion Network) om deze uitdagingen direct aan te pakken. Het systeem neemt ruwe OCT-oogscans en maakt ze eerst helderder door randversterking, ruisreductie en helderheidsaanpassing, zodat subtiele structuren beter zichtbaar worden en beelden van verschillende scanners meer op elkaar gaan lijken. Daarna voert het de gegevens door twee complementaire paden: het ene richt zich op kleine lokale details zoals dunne grenzen tussen lagen, terwijl het andere bredere patronen over de hele scan analyseert, en vastlegt hoe lagen buigen en waar vocht tendentieus ophoopt. Een speciaal fusieblok combineert deze twee aanzichten en gebruikt een aandachtmechanisme — in wezen een manier om automatisch “meer aandacht” te besteden aan informatieve regio’s — om kenmerken te benadrukken die waarschijnlijk ziek weefsel vertegenwoordigen.
Anatomie en ziekte samen in beeld
Verder dan alleen het omlijnen van gezonde anatomie bevat AMDF‑Net een ziekte‑inclusieve module die is afgestemd op patronen die bij echte patiënten voorkomen, zoals intraretinale en subretinale vochtophopingen of gebieden waar het ondersteunend weefsel is opgetild. Dit deel van het netwerk leert tijdens training beeldpatronen te benadrukken die vaak op ziekte wijzen, terwijl het de normale laagsstructuur blijft volgen. Het systeem wordt gestuurd door een zorgvuldig ontworpen verliesfunctie — een wiskundige score die het probeert te optimaliseren — die zowel nauwkeurige gebiedsinvulling als scherpe grenzen beloont. Door tijdens het leerproces feedback te combineren die zowel op regio’s als op randen is gericht, wordt het model gedwongen segmentaties te produceren die niet alleen goed overlappen met expertmarkeringen maar ook vloeiende, klinisch betekenisvolle contouren hebben.
Getest op veel patiënten en scanners
Om te beoordelen hoe goed AMDF‑Net in de praktijk werkt, testten de auteurs het op drie bekende openbare OCT‑datasets en een reëel klinisch gegevensbestand van een drukbezocht oogziekenhuis. Deze sets bestrijken verschillende ziekten, scanmerken en beeldkwaliteiten, inclusief vooral lastige regio’s rond de oogzenuw en kleine vochtophopingen die veel algoritmen missen. Over al deze datasets heen evenaarde of overtrof AMDF‑Net consequent toonaangevende methoden, verbeterde veelgebruikte nauwkeurigheidsscores met ongeveer drie tot vijf procentpunten en verminderde zichtbare fouten zoals gebroken laaglijnen of foutief geïdentificeerde vochtvlekken. Belangrijk is dat het systeem beelden van verschillende fabrikanten met slechts kleine prestatieverminderingen aan kon, een sleutelvereiste voor dagelijks klinisch gebruik.
Wat dit betekent voor patiënten en klinieken
Voor niet‑specialisten is de kernboodschap dat AMDF‑Net fungeert als een hoogopgeleide digitale assistent die snel en betrouwbaar de structuur van het netvlies en probleemgebieden in OCT‑scans kan uittekenen. Door dit op grote aantallen beelden toe te passen, kan het oogartsen helpen ziektes eerder te signaleren, subtiele veranderingen tussen bezoeken te volgen en behandelingen preciezer af te stemmen, zelfs in drukke of middelenarme omgevingen. Hoewel de methode momenteel meer rekenkracht vraagt dan eenvoudigere modellen, merken de auteurs op dat toekomstige verfijningen en compressietechnieken het snel genoeg kunnen maken voor routinematig gebruik aan de behandelstoel. Op de lange termijn kunnen hulpmiddelen zoals AMDF‑Net helpen het gezichtsvermogen te behouden door complexe oogscans om te zetten in heldere, bruikbare kaarten van netvliesgezondheid.
Bronvermelding: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Trefwoorden: optische coherentietomografie, netvliesaandoening, deep learning segmentatie, medische beeldvorming AI, maculair oedeem