Clear Sky Science · de
Multiskaliges adaptives Fusionsnetzwerk zur Segmentierung von Netzhautschichten und Flüssigkeit in OCT B‑Scans
Scharfere Netzhautaufnahmen für die alltägliche Augenversorgung
Erkrankungen wie Diabetes und altersbedingte Makuladegeneration können die Netzhaut, das lichtempfindliche Gewebe im Augenhintergrund, lange unbemerkt schädigen, bevor sich Sehstörungen zeigen. Moderne Geräte der optischen Kohärenztomographie (OCT) liefern Ärzten bereits detaillierte Querschnittsbilder der Netzhaut, doch die manuelle Auswertung ist zeitaufwendig und kann subtile Warnzeichen übersehen. Diese Studie stellt ein fortschrittliches Computersystem vor, AMDF‑Net, das dafür entwickelt wurde, die feinen Netzhautschichten und Flüssigkeitsansammlungen mit hoher Präzision automatisch zu markieren — was schnellere und verlässlichere Diagnosen und Verlaufsbeobachtungen bei erblindenden Augenerkrankungen ermöglichen könnte.
Warum Augenflüssigkeit so wichtig ist
Bei mehreren häufigen Augenerkrankungen — darunter diabetisches Makulaödem, altersbedingte Makuladegeneration sowie Gefäß- oder Nervenprobleme der Netzhaut — bilden sich winzige Flüssigkeitsansammlungen innerhalb oder unterhalb der Netzhaut. Größe, Form und genaue Lage dieser Flüssigkeitsherde geben Ärzten Hinweise darauf, ob eine Behandlung wirkt oder die Erkrankung fortschreitet. OCT‑Bilder erfassen diese Merkmale sehr detailliert, doch die Netzhaut besteht aus vielen papierdünnen Schichten, die sich krümmen und überlappen. Flüssigkeit verwischt Grenzen und erscheint in unregelmäßigen Gebilden. Traditionelle Programme und frühere Deep‑Learning‑Ansätze tun sich oft schwer, diese Schichten und Flüssigkeitsbereiche korrekt zu trennen, besonders wenn Bilder verrauscht, der Kontrast gering oder das Erkrankungsmuster ungewöhnlich ist.
Ein neuer digitaler Assistent für OCT‑Bilder
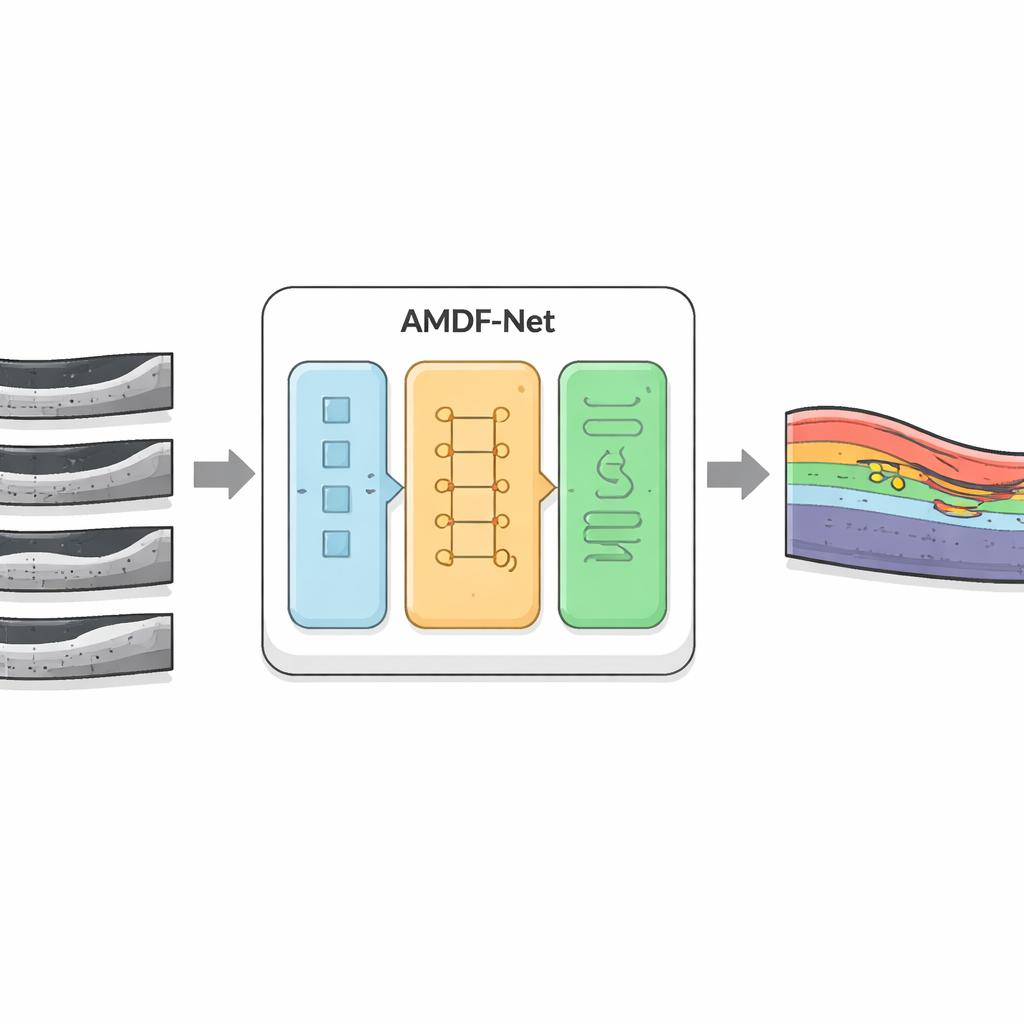
Die Autoren haben AMDF‑Net (Adaptive Multi‑Domain Fusion Network) entwickelt, um diese Herausforderungen direkt anzugehen. Das System nimmt rohe OCT‑Scans und bereitet sie zuerst mit Kantenschärfung, Rauschreduktion und Helligkeitsanpassung auf, sodass subtile Strukturen besser sichtbar werden und Bilder verschiedener Scanner einander ähnlicher erscheinen. Anschließend durchläuft die Aufnahme zwei komplementäre Pfade: Der eine konzentriert sich auf kleine lokale Details wie dünne Schichtgrenzen, der andere analysiert großflächigere Muster über den gesamten Scan und erfasst, wie sich Schichten biegen und wo sich Flüssigkeit typischerweise ansammelt. Ein spezieller Fusionsblock kombiniert diese beiden Sichten und nutzt einen Aufmerksamkeitsmechanismus — im Grunde eine Methode, automatisch „mehr Aufmerksamkeit“ auf informative Regionen zu richten — um Merkmale hervorzuheben, die besonders wahrscheinlich erkranktes Gewebe repräsentieren.
Anatomie und Krankheit zusammen sehen
Über die reine Abgrenzung der normalen Anatomie hinaus enthält AMDF‑Net ein krankheitsinklusives Modul, das auf in echten Patientendaten beobachtete Muster abgestimmt ist, etwa intraretinale und subretinale Flüssigkeitsansammlungen oder Bereiche, in denen sich das stützende Gewebe abgehoben hat. Dieser Teil des Netzwerks lernt während des Trainings, Bildmuster zu betonen, die häufig auf Erkrankungen hinweisen, behält dabei aber die normale Schichtstruktur im Blick. Das System wird durch eine sorgfältig gestaltete Verlustfunktion gesteuert — eine mathematische Bewertungsgröße, die es zu optimieren versucht — die sowohl exakte Flächendarstellungen als auch scharfe Kanten belohnt. Durch die Kombination von regionenbasiertem und kantenfokussiertem Feedback während des Lernens wird das Modell dazu angeleitet, Segmentierungen zu erzeugen, die nicht nur stark mit Expertenmarkierungen überlappen, sondern auch glatte, klinisch sinnvolle Konturen aufweisen.
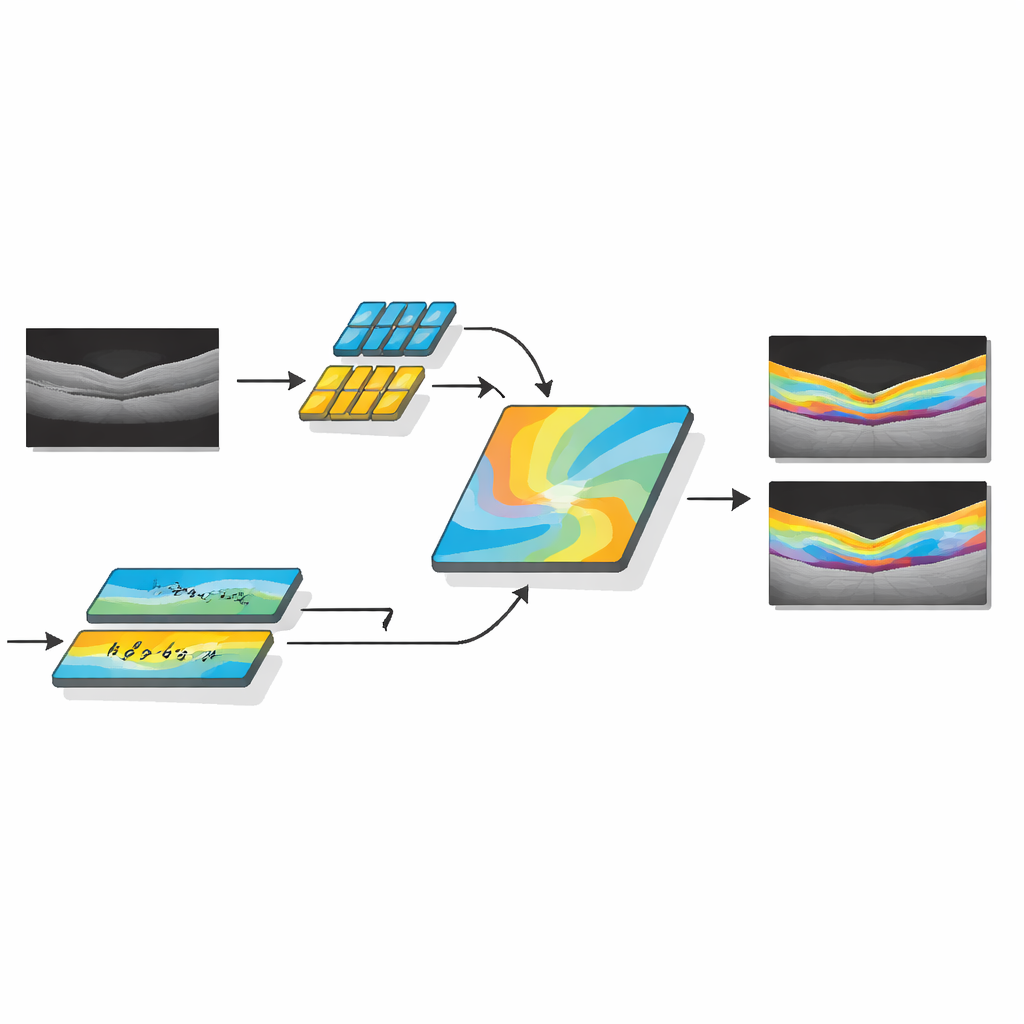
Getestet an vielen Patienten und Scannern
Um die praktische Leistungsfähigkeit von AMDF‑Net zu bewerten, testeten die Autoren das System an drei bekannten öffentlichen OCT‑Datensätzen und an einem klinischen Real‑World‑Datensatz eines belebten Augenklinikums. Diese Sets decken verschiedene Erkrankungen, Scannerhersteller und Bildqualitäten ab, einschließlich besonders schwieriger Bereiche rund um den Sehnerv und winziger Flüssigkeitsansammlungen, die viele Algorithmen übersehen. Über alle Datensätze hinweg erreichte AMDF‑Net durchgehend Ergebnisse, die mit führenden Methoden mithalten konnten oder diese übertrafen: Die gängigen Genauigkeitsmaße verbesserten sich um etwa drei bis fünf Prozentpunkte, und sichtbare Fehler wie unterbrochene Schichtlinien oder falsch identifizierte Flüssigkeitsinseln traten seltener auf. Wichtig ist, dass das System Bilder verschiedener Hersteller mit nur geringen Leistungseinbußen verarbeitete — eine Schlüsselerfordernis für den späteren Einsatz in der klinischen Praxis.
Was das für Patienten und Kliniken bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: AMDF‑Net fungiert wie ein hochqualifizierter digitaler Assistent, der OCT‑Scans schnell und verlässlich die Netzhautstruktur und Problembereiche entnimmt. Durch die Auswertung großer Bildmengen könnte es Augenärzten helfen, Erkrankungen früher zu erkennen, subtile Veränderungen zwischen Terminen zu verfolgen und Behandlungen präziser anzupassen — selbst in stark frequentierten oder ressourcenbegrenzten Einrichtungen. Zwar benötigt die Methode derzeit mehr Rechenleistung als einfachere Modelle, doch die Autoren weisen darauf hin, dass künftige Optimierungen und Komprimierungstechniken sie schnell genug für den routinemäßigen Einsatz am Behandlungsstuhl machen könnten. Langfristig könnten Werkzeuge wie AMDF‑Net dazu beitragen, das Sehvermögen zu erhalten, indem sie komplexe Netzhautbilder in klare, umsetzbare Karten der Netzhautgesundheit verwandeln.
Zitation: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Schlüsselwörter: optische Kohärenztomographie, Netzhauterkrankung, Tiefenlernsegmentierung, medizinische Bildgebung KI, makulödem