Clear Sky Science · pt
Rede de fusão adaptativa multiescala para segmentação de camadas retinianas e fluido em cortes B de tomografia de coerência óptica
Escaneamentos oculares mais nítidos para o cuidado visual cotidiano
Doenças como diabetes e degeneração macular relacionada à idade podem danificar silenciosamente a retina, o tecido sensível à luz na parte de trás do olho, muito antes de notarmos alterações na visão. Scanners modernos chamados tomografia de coerência óptica (OCT) já fornecem aos médicos vistas transversais detalhadas da retina, mas interpretar essas imagens manualmente é demorado e pode deixar passar sinais sutis de alerta. Este estudo apresenta um sistema computacional avançado, AMDF‑Net, projetado para traçar automaticamente as delicadas camadas da retina e bolsões de fluido com alta precisão, possibilitando diagnósticos e monitoramento de doenças oculares cegantes de forma mais rápida e confiável.
Por que o fluido ocular é tão importante
Em várias condições oculares comuns — incluindo edema macular diabético, degeneração macular relacionada à idade e problemas nas veias ou nervos retinais — pequenos acúmulos de fluido se formam dentro ou sob a retina. Seu tamanho, formato e localização exata indicam aos médicos se um tratamento está funcionando ou se a doença está piorando. As imagens OCT capturam essas características em grande detalhe, mas a retina é composta por muitas camadas finíssimas que se curvam e se sobrepõem. O fluido pode borrar limites e aparecer em manchas irregulares. Programas tradicionais e mesmo ferramentas de aprendizado profundo anteriores frequentemente têm dificuldade para separar corretamente essas camadas e fluidos quando as imagens estão ruidosas, com baixo contraste ou quando o padrão da doença é incomum.
Um novo assistente digital para imagens OCT
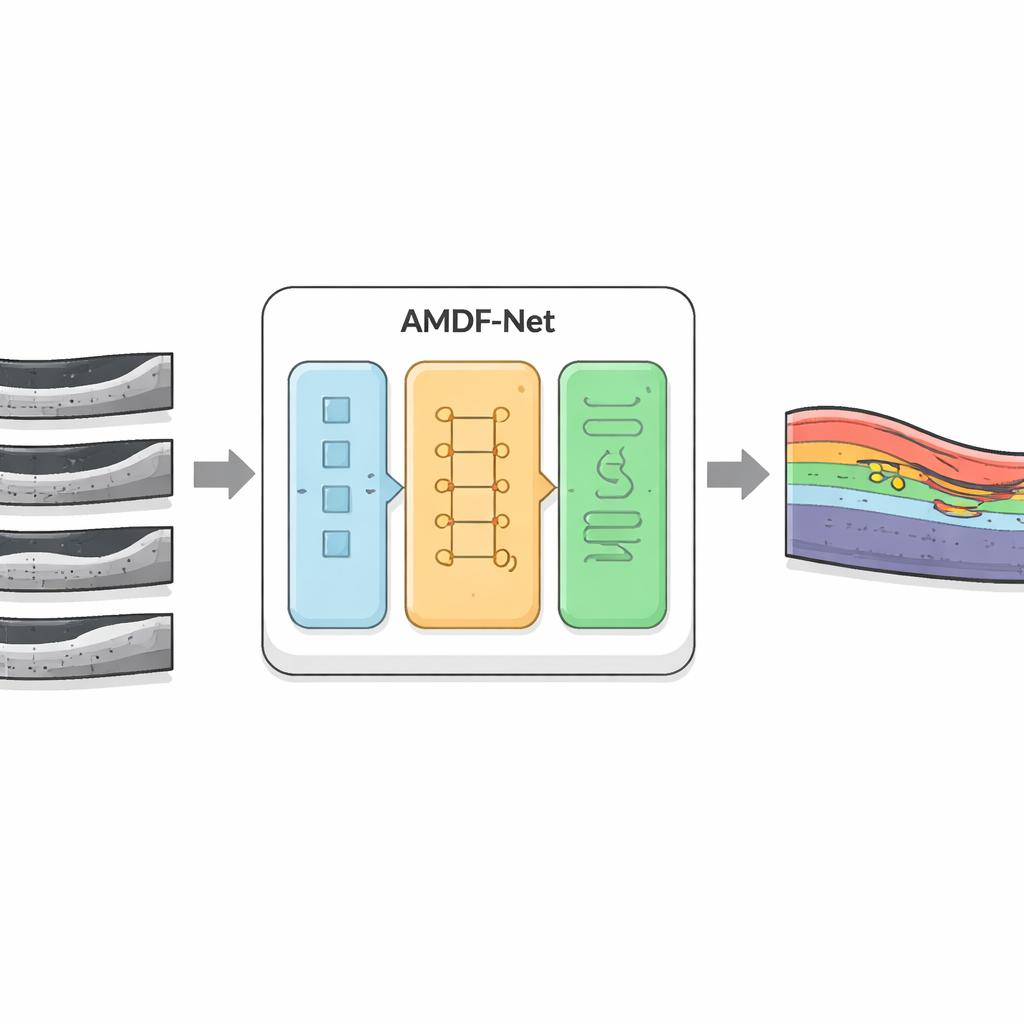
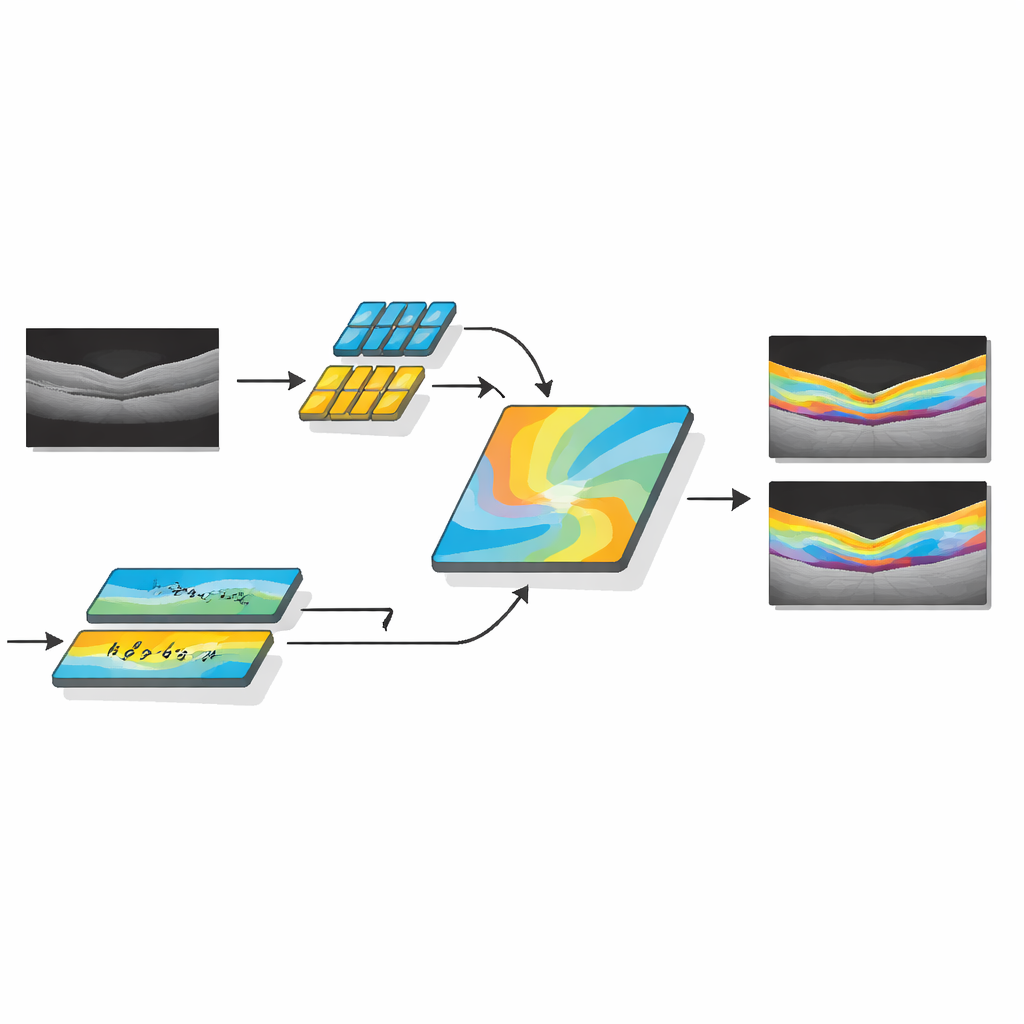
Os pesquisadores desenvolveram o AMDF‑Net (Adaptive Multi‑Domain Fusion Network) para enfrentar esses desafios de forma direta. O sistema recebe escaneamentos OCT brutos e primeiro os limpa usando realce de bordas, redução de ruído e equalização de brilho, de modo que estruturas sutis se destaquem e imagens de diferentes scanners fiquem mais semelhantes. Em seguida, os dados passam por duas vias complementares: uma foca em pequenos detalhes locais, como limites finos entre camadas, enquanto a outra analisa padrões mais amplos ao longo de todo o corte, capturando como as camadas se curvam e onde o fluido tende a se acumular. Um bloco especial de fusão combina essas duas visões e utiliza um mecanismo de atenção — essencialmente uma forma de ‘‘dar mais atenção’’ automaticamente às regiões informativas — para destacar características que têm maior probabilidade de representar tecido doente.
Vendo anatomia e doença ao mesmo tempo
Além de simplesmente delinear a anatomia saudável, o AMDF‑Net inclui um módulo inclusivo de doença ajustado a padrões observados em pacientes reais, como bolsões de fluido intrarretiniano e subretiniano ou áreas onde o tecido de suporte se elevou. Essa parte da rede aprende, durante o treinamento, a enfatizar padrões de imagem que comumente sinalizam doença, mantendo ao mesmo tempo o acompanhamento da estrutura normal das camadas. O sistema é orientado por uma função de perda cuidadosamente projetada — uma métrica matemática que busca otimizar — que recompensa tanto o preenchimento regional preciso quanto contornos nítidos. Ao combinar feedback baseado em regiões e voltado para bordas durante o aprendizado, o modelo é estimulado a produzir segmentações que não apenas se sobrepõem bem às marcações de especialistas, mas também apresentam contornos suaves e clinicamente significativos.
Testado em muitos pacientes e scanners
Para avaliar o desempenho do AMDF‑Net na prática, os autores o testaram em três conjuntos públicos bem conhecidos de OCT e em um conjunto clínico do mundo real proveniente de um hospital oftalmológico movimentado. Esses conjuntos cobrem diferentes doenças, marcas de scanner e qualidades de imagem, incluindo regiões especialmente difíceis ao redor do nervo óptico e pequenos bolsões de fluido que muitos algoritmos perdem. Em todos eles, o AMDF‑Net consistentemente igualou ou superou métodos líderes, melhorando as pontuações de acurácia comuns em aproximadamente três a cinco pontos percentuais e reduzindo erros visíveis, como linhas de camadas interrompidas ou bolsões de fluido identificados incorretamente. Importante, o sistema lidou com imagens de diferentes fabricantes com apenas pequenas quedas de desempenho, um requisito chave para uso eventual em clínicas rotineiras.
O que isso significa para pacientes e clínicas
Para não especialistas, a mensagem principal é que o AMDF‑Net age como um assistente digital altamente treinado que pode traçar rápida e confiavelmente a estrutura retiniana e os pontos problemáticos nas imagens OCT. Ao fazer isso em grande número de exames, ele pode ajudar oftalmologistas a detectar doenças mais cedo, acompanhar mudanças sutis entre visitas e ajustar tratamentos com mais precisão, mesmo em ambientes lotados ou com recursos limitados. Embora o método atualmente exija mais poder computacional do que modelos mais simples, os autores observam que refinamentos futuros e técnicas de compressão podem torná‑lo rápido o suficiente para uso rotineiro à beira do leito. A longo prazo, ferramentas como o AMDF‑Net podem ajudar a preservar a visão ao transformar exames oculares complexos em mapas claros e acionáveis da saúde retiniana.
Citação: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Palavras-chave: tomografia de coerência óptica, doença retinal, segmentação por deep learning, IA em imagens médicas, edema macular