Clear Sky Science · pl
Wieloskalowa adaptacyjna sieć fuzji do segmentacji warstw siatkówki i płynów w skanach OCT B
Bardziej szczegółowe skany oka dla codziennej opieki wzrokowej
Choroby takie jak cukrzyca czy zwyrodnienie plamki związane z wiekiem mogą przez długi czas dostatecznie cicho uszkadzać siatkówkę — światłoczułą tkankę z tyłu oka — zanim zauważymy zmiany w widzeniu. Nowoczesne skanery, zwane optyczną koherentną tomografią (OCT), już teraz dostarczają lekarzom szczegółowych przekrojowych obrazów siatkówki, ale ręczna interpretacja tych obrazów jest czasochłonna i może przeoczyć subtelne sygnały ostrzegawcze. Niniejsze badanie przedstawia zaawansowany system komputerowy, AMDF‑Net, zaprojektowany do automatycznego śledzenia delikatnych warstw siatkówki oraz kieszonek płynu z wysoką precyzją, co potencjalnie umożliwia szybszą i bardziej niezawodną diagnostykę oraz monitorowanie chorób oczu prowadzących do utraty wzroku.
Dlaczego płyn w oku jest tak istotny
W kilku powszechnych schorzeniach oka — w tym w cukrzycowym obrzęku plamki, zwyrodnieniu plamki związanym z wiekiem oraz zaburzeniach żylnych lub nerwowych siatkówki — w obrębie lub pod siatkówką tworzą się drobne zbiorniki płynu. Ich rozmiar, kształt i dokładne położenie informują lekarzy, czy leczenie działa, czy choroba się pogarsza. Obrazy OCT rejestrują te cechy w dużych szczegółach, ale siatkówka składa się z wielu papierowo cienkich warstw, które się wyginają i nakładają. Płyn może rozmazywać granice i pojawiać się w nieregularnych skupiskach. Tradycyjne programy komputerowe, a nawet wcześniejsze narzędzia uczenia głębokiego, często mają trudności z poprawnym rozdzieleniem tych warstw i płynów, gdy obrazy są zaszumione, kontrast jest niski lub wzorzec chorobowy jest nietypowy.
Nowy cyfrowy asystent dla obrazów OCT
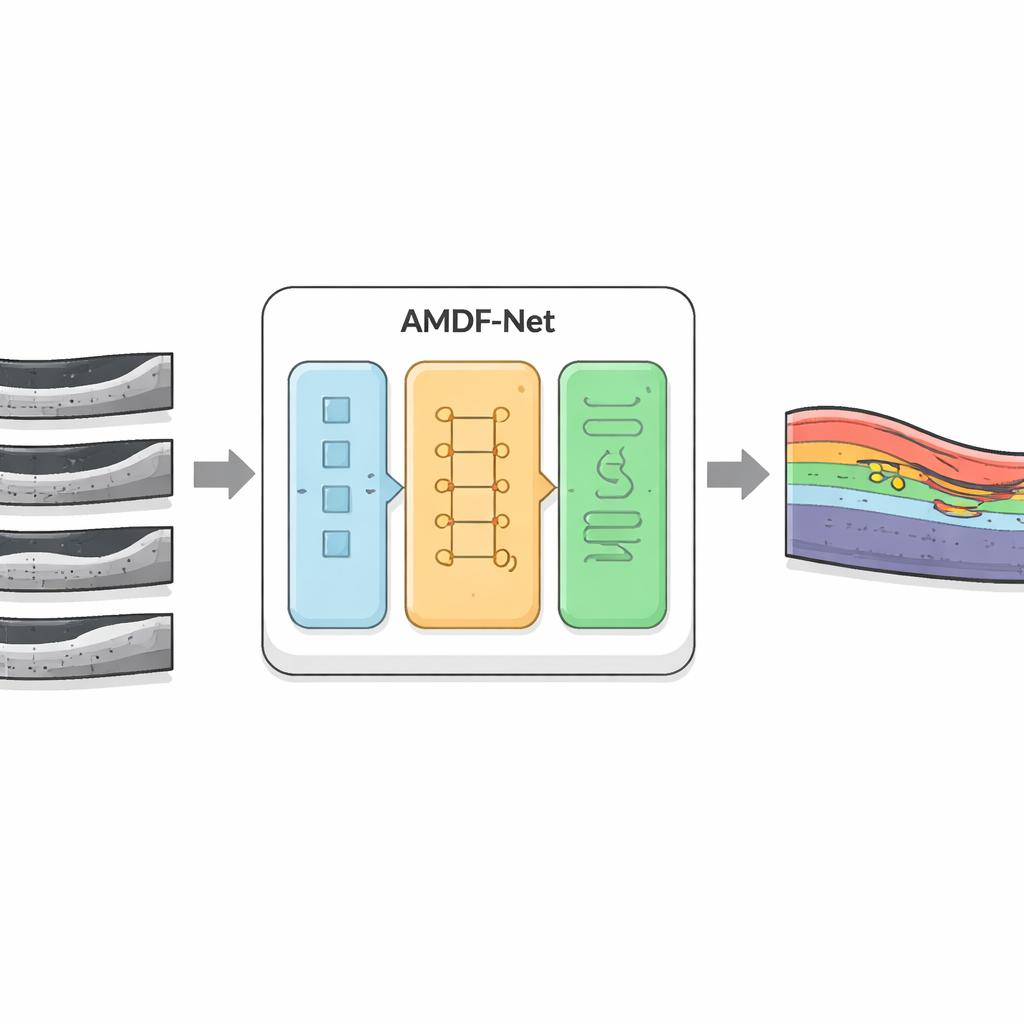
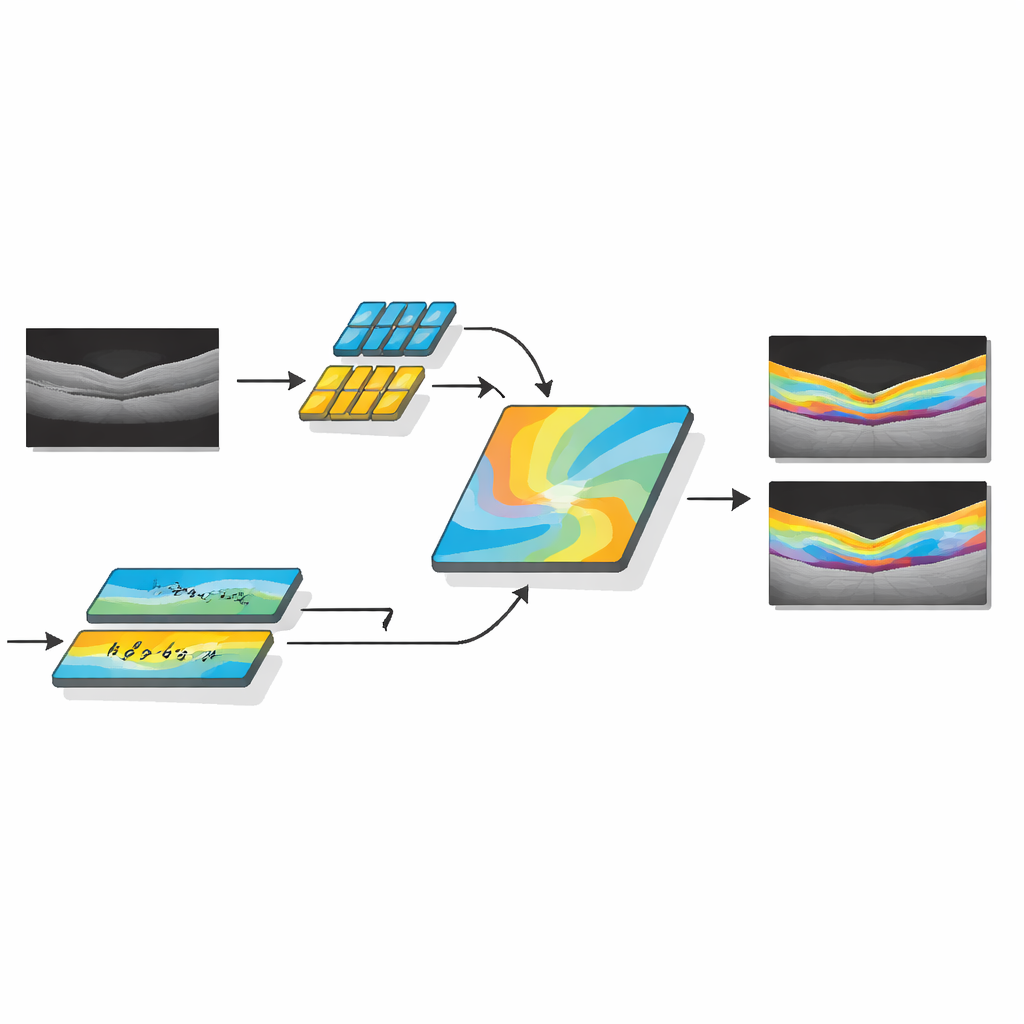
Naukowcy opracowali AMDF‑Net (Adaptive Multi‑Domain Fusion Network), aby sprostać tym wyzwaniom. System wczytuje surowe skany OCT oka i najpierw poprawia ich jakość, stosując wzmocnienie krawędzi, redukcję szumów i wyrównanie jasności, tak aby subtelne struktury były bardziej widoczne, a obrazy z różnych skanerów wyglądały podobniej. Następnie dane przechodzą przez dwie komplementarne ścieżki: jedna koncentruje się na drobnych lokalnych detalach, takich jak cienkie granice między warstwami, a druga analizuje szersze wzorce w całym skanie, wychwytując, jak warstwy się wyginają i gdzie zwykle gromadzi się płyn. Specjalny blok fuzji łączy te dwa spojrzenia i wykorzystuje mechanizm uwagi — w praktyce sposób automatycznego „zwracania większej uwagi” na informatywne obszary — aby wyróżnić cechy szczególnie prawdopodobne do reprezentowania tkanki chorobowej.
Widzenie anatomii i choroby jednocześnie
Ponad samo zarysowanie prawidłowej anatomii, AMDF‑Net zawiera moduł uwzględniający cechy chorobowe, dostrojony do wzorców obserwowanych u rzeczywistych pacjentów, takich jak kieszonki płynu wewnątrzsiatkówkowego i podsiatkówkowego czy obszary, gdzie tkanka podporowa się unosi. Ta część sieci uczy się podczas treningu podkreślać wzorce na obrazie, które często sygnalizują chorobę, przy jednoczesnym zachowaniu informacji o normalnej strukturze warstw. System jest kierowany starannie zaprojektowaną funkcją straty — matematycznym wskaźnikiem, który optymalizuje — nagradzając zarówno dokładne wypełnienie obszarów, jak i ostre krawędzie. Łącząc informacje zwrotne oparte na regionach i skoncentrowane na krawędziach podczas uczenia, model jest wymuszany do tworzenia segmentacji, które nie tylko dobrze pokrywają się z oznaczeniami ekspertów, lecz także mają gładkie, klinicznie istotne kontury.
Przetestowany na wielu pacjentach i skanerach
Aby ocenić praktyczną skuteczność AMDF‑Net, autorzy przetestowali go na trzech dobrze znanych publicznych zbiorach OCT oraz na rzeczywistym klinicznym zbiorze danych z ruchliwego szpitala okulistycznego. Zbiory te obejmują różne choroby, marki skanerów i jakość obrazów, w tym szczególnie trudne okolice nerwu wzrokowego oraz drobne kieszonki płynu, które wiele algorytmów pomija. We wszystkich przypadkach AMDF‑Net konsekwentnie dorównywał bądź przewyższał wiodące metody, poprawiając typowe miary dokładności o około trzy do pięciu punktów procentowych i redukując widoczne błędy, takie jak przerwane linie warstw czy błędnie zidentyfikowane skupiska płynu. Co ważne, system radził sobie z obrazami od różnych producentów przy jedynie niewielkim spadku wydajności — kluczowy warunek do zastosowania w codziennych warunkach klinicznych.
Co to oznacza dla pacjentów i klinik
Dla osób niebędących specjalistami kluczowa informacja jest taka, że AMDF‑Net działa jak wysoko wytrenowany cyfrowy asystent, który szybko i niezawodnie potrafi odtworzyć strukturę siatkówki i wskazać problematyczne obszary na skanach OCT. Przetwarzając duże liczby obrazów, może pomóc okulistom wcześniej wykrywać choroby, śledzić subtelne zmiany między wizytami i precyzyjniej dobierać leczenie, nawet w zatłoczonych lub ograniczonych zasobowo warunkach. Chociaż metoda obecnie wymaga większej mocy obliczeniowej niż prostsze modele, autorzy zaznaczają, że przyszłe udoskonalenia i techniki kompresji mogą uczynić ją wystarczająco szybką do rutynowego zastosowania przy pacjencie. W dłuższej perspektywie narzędzia takie jak AMDF‑Net mogą pomóc zachować wzrok, przekształcając złożone skany oka w czytelne, praktyczne mapy zdrowia siatkówki.
Cytowanie: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Słowa kluczowe: tomografia koherentna optyczna, choroba siatkówki, segmentacja uczeniem głębokim, Sztuczna inteligencja w obrazowaniu medycznym, obrzęk plamki