Clear Sky Science · fr
Réseau de fusion adaptative multi-échelle pour la segmentation des couches rétiniennes et des liquides dans les coupes B en tomographie par cohérence optique
Des scans oculaires plus nets pour les soins visuels courants
Des maladies comme le diabète et la dégénérescence maculaire liée à l'âge peuvent endommager silencieusement la rétine, le tissu photosensible au fond de l'œil, bien avant que nous remarquions des changements de vision. Les appareils modernes appelés tomographes par cohérence optique (OCT) fournissent déjà aux médecins des vues en coupe détaillées de la rétine, mais l'interprétation manuelle de ces images est lente et peut laisser échapper des signes d'alerte subtils. Cette étude présente un système informatique avancé, AMDF‑Net, conçu pour tracer automatiquement avec une grande précision les couches délicates de la rétine et les poches de liquide, permettant potentiellement un diagnostic et un suivi des maladies oculaires menaçant la vue plus rapides et plus fiables.
Pourquoi le liquide intraoculaire est si important
Dans plusieurs affections oculaires courantes — notamment l'œdème maculaire diabétique, la dégénérescence maculaire liée à l'âge et des problèmes veineux ou nerveux rétiniens — de petites poches de liquide se forment dans ou sous la rétine. Leur taille, leur forme et leur emplacement précis indiquent aux cliniciens si un traitement fonctionne ou si la maladie s'aggrave. Les images OCT captent ces caractéristiques en détail, mais la rétine est composée de nombreuses couches d'une finesse extrême qui se courbent et se chevauchent. Le liquide peut estomper les frontières et apparaître en amas irréguliers. Les programmes classiques, et même des outils d'apprentissage profond antérieurs, peinent souvent à séparer correctement ces couches et ces liquides lorsque les images sont bruitées, peu contrastées ou présentent des schémas pathologiques atypiques.
Un nouvel assistant numérique pour les images OCT
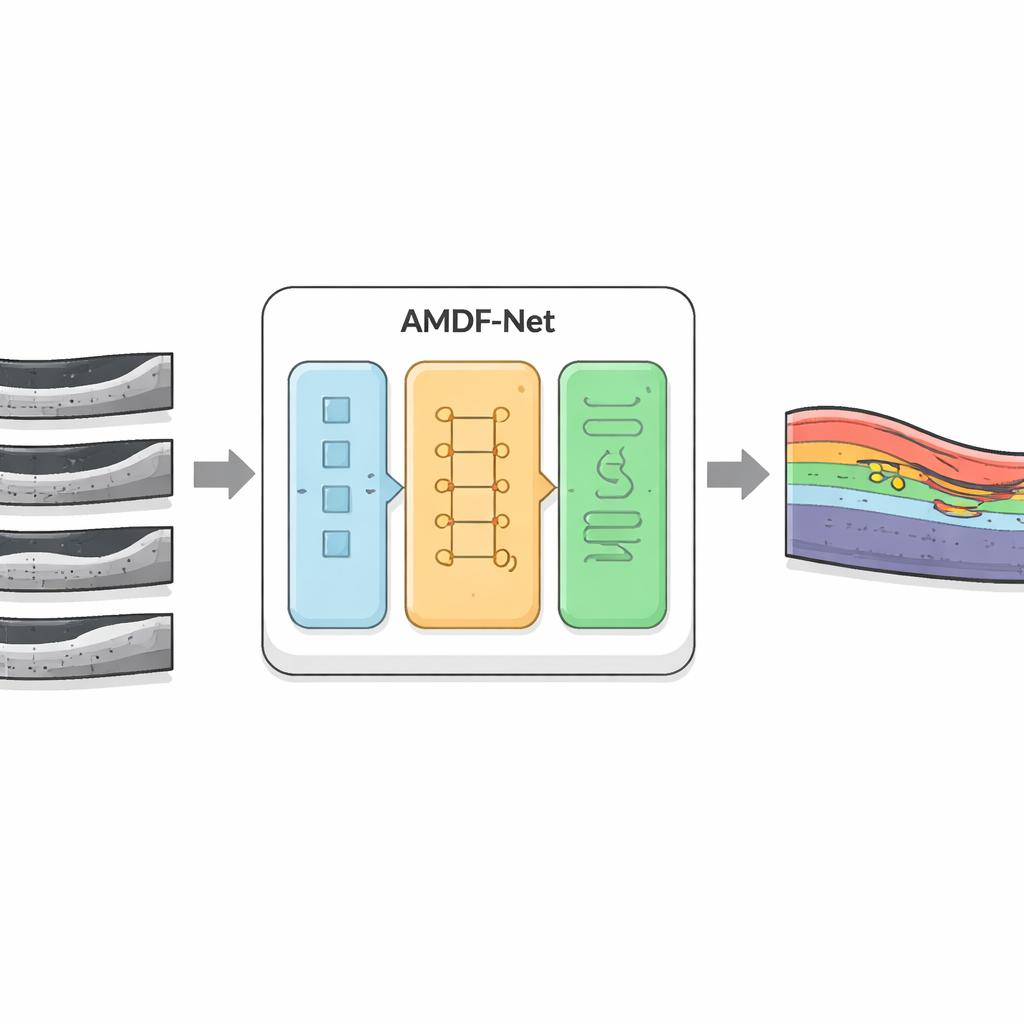
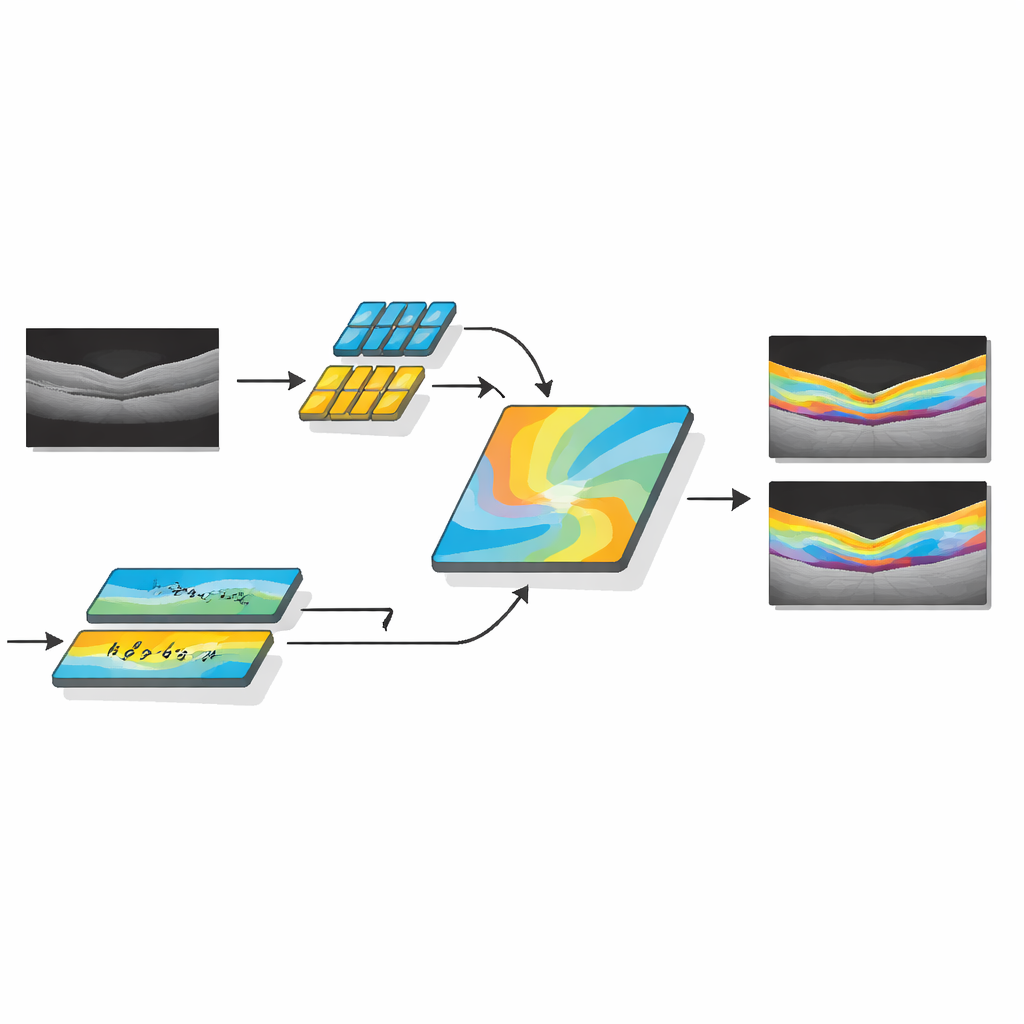
Les chercheurs ont développé AMDF‑Net (Adaptive Multi‑Domain Fusion Network) pour relever ces défis directement. Le système prend des scans OCT bruts et commence par les améliorer en renforçant les contours, en réduisant le bruit et en uniformisant la luminosité afin que les structures subtiles ressortent et que les images provenant de différents appareils se ressemblent davantage. Ensuite, il traite les données via deux voies complémentaires : l'une se concentre sur les petits détails locaux comme les fines limites entre les couches, tandis que l'autre analyse des motifs plus larges sur l'ensemble de la coupe, capturant la façon dont les couches se courbent et où le liquide a tendance à s'accumuler. Un bloc de fusion spécial combine ces deux vues et utilise un mécanisme d'attention — essentiellement un moyen de « prêter plus attention » automatiquement aux régions informatives — pour mettre en évidence les caractéristiques les plus susceptibles de représenter un tissu malade.
Voir à la fois l'anatomie et la maladie
Au‑delà du simple tracé de l'anatomie normale, AMDF‑Net intègre un module inclusif de pathologie réglé sur les motifs observés chez de vrais patients, comme des poches de liquide intrarétinien et sous‑rétinien ou des zones où le tissu de soutien s'est soulevé. Cette partie du réseau apprend, lors de l'entraînement, à accentuer les motifs d'image qui signalent couramment une maladie, tout en conservant la structure normale des couches. Le système est guidé par une fonction de perte soigneusement conçue — un score mathématique qu'il tente d'optimiser — qui récompense à la fois le remplissage régional précis et les frontières nettes. En combinant des retours axés sur la région et sur les contours pendant l'apprentissage, le modèle est poussé à produire des segmentations qui non seulement recouvrent bien les annotations d'experts, mais présentent aussi des contours lisses et cliniquement pertinents.
Testé sur de nombreux patients et appareils
Pour évaluer les performances pratiques d'AMDF‑Net, les auteurs l'ont testé sur trois collections OCT publiques bien connues et un jeu de données clinique du monde réel provenant d'un grand hôpital ophtalmologique. Ces ensembles couvrent différentes maladies, marques d'appareils et qualités d'image, incluant des régions particulièrement délicates autour du nerf optique et de minuscules poches de liquide que de nombreux algorithmes manquent. Sur l'ensemble de ces jeux, AMDF‑Net a constamment égalé ou surpassé les méthodes de pointe, améliorant les scores d'exactitude usuels d'environ trois à cinq points de pourcentage et réduisant les erreurs visibles comme des lignes de couche rompues ou des amas de liquide mal identifiés. Fait important, le système a traité des images de différents fabricants avec seulement de légères baisses de performance, condition clé pour une utilisation future en clinique quotidienne.
Ce que cela signifie pour les patients et les cliniques
Pour les non‑spécialistes, l'idée principale est qu'AMDF‑Net agit comme un assistant numérique hautement qualifié capable de tracer rapidement et de manière fiable la structure rétinienne et les points problématiques sur les scans OCT. En appliquant cela à de grands volumes d'images, il pourrait aider les ophtalmologistes à détecter la maladie plus tôt, à suivre des changements subtils entre les visites et à adapter les traitements avec plus de précision, même dans des contextes chargés ou à ressources limitées. Si la méthode demande actuellement plus de puissance de calcul que des modèles plus simples, les auteurs notent que des affinements et des techniques de compression futures pourraient la rendre suffisamment rapide pour une utilisation courante au chevet du patient. À long terme, des outils comme AMDF‑Net pourraient contribuer à préserver la vue en transformant des scans oculaires complexes en cartes claires et exploitables de la santé rétinienne.
Citation: Mani, P., Ramachandran, N., Sowmya, V. et al. Multi-scale adaptive fusion network for retinal layer and fluid segmentation in optical coherence tomography B-scans. Sci Rep 16, 10600 (2026). https://doi.org/10.1038/s41598-026-44006-5
Mots-clés: tomographie par cohérence optique, maladie rétinienne, segmentation par apprentissage profond, IA en imagerie médicale, œdème maculaire