Clear Sky Science · zh
通过甲基化表观遗传调控糖皮质激素受体基因与创伤后应激障碍相关
为何有些心智会弯曲但不破裂
并非所有经历战争、袭击或灾难的人都会发展为创伤后应激障碍(PTSD)。这种对创伤影响的不同程度提出了一个基础性问题:是什么让一只大脑易受伤害,而另一只却表现出韧性?在这项大鼠研究中,研究者将视线从行为表象延伸到DNA上的化学标记层面,探讨大脑应激回路中细微的开关如何使个体在创伤后倾向于长期的恐惧、焦虑和低落情绪。
同一创伤事件为何结果大相径庭
为了模拟创伤,研究团队让大鼠经历了一系列强烈的应激—约束、强迫游泳、麻醉气味暴露及轻度电击—这种方法称为单次持久应激模型。随后动物被安置一周不受干扰,再用一组标准测试评估绝望样行为、焦虑和快感缺失。尽管所有大鼠经历了相同的折磨,它们的反应却各不相同。有些在强迫游泳测试中明显不动、开放空间探索减少并对加糖水兴趣减弱;这些被归为高易感性动物。另一些的行为与未受应激的大鼠相似,被视为低易感性,作为韧性的代理指标。 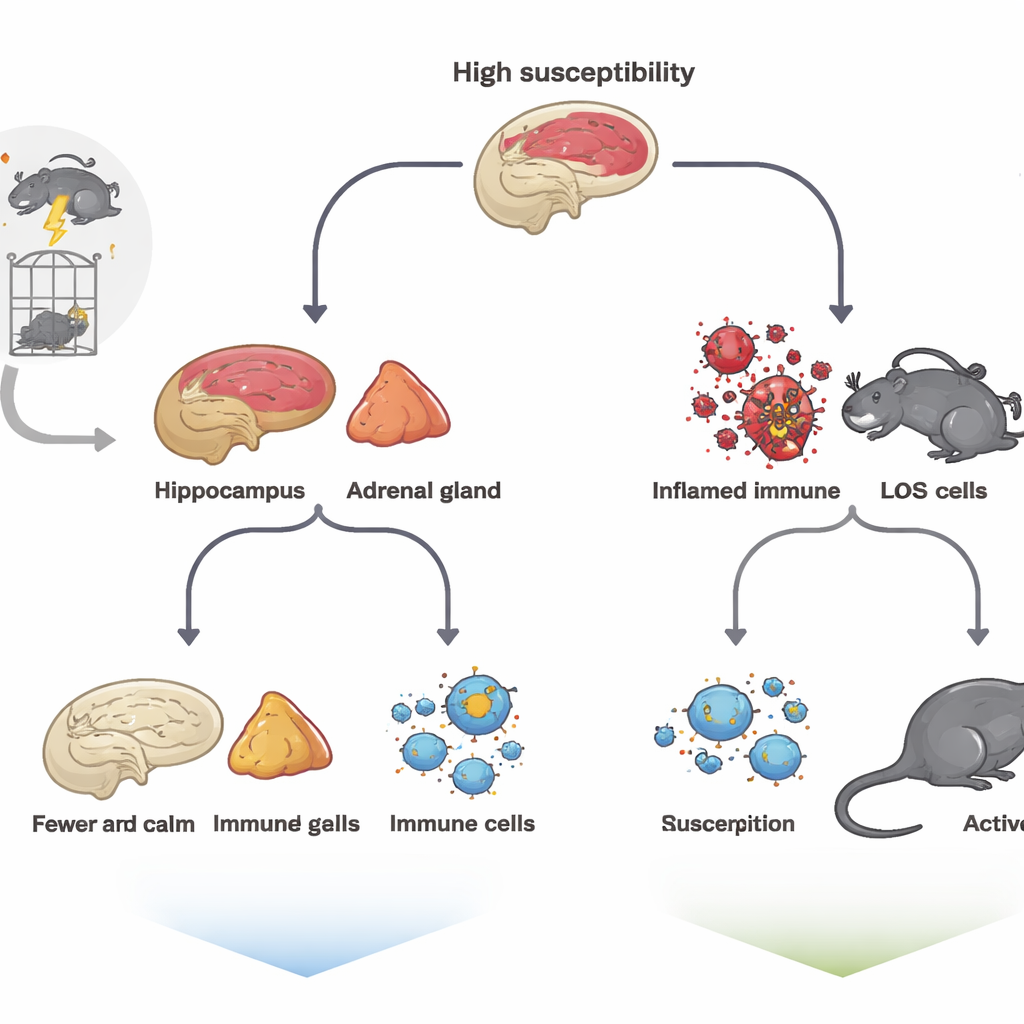
关键脑受体上的化学调光器
研究者聚焦于大脑中的一种受体mGluR5,它帮助神经元调整连接,并参与恐惧学习与情绪调节。他们并非寻找该受体基因的突变,而是检查DNA甲基化——这些小的化学标记像调光开关,通常在某些位点富集时会降低基因表达。在与记忆和应激控制密切相关的海马体中,高易感性大鼠表现出mGluR5基因活性下降,同时该基因调控区的特定位点甲基化水平升高。低易感性大鼠则未显示此模式。这种更强的化学标记与降低的基因活性并列出现,表明创伤经历实际上“调低”了一个通常有助于大脑适应应激的受体。
应激激素、炎症与细胞磨损
基因调控的改变并非孤立发生。高易感性大鼠显示出体内主要应激激素系统的激增。释放促肾上腺皮质激素释放因子的深部脑区细胞更为活跃,血液中皮质酮(啮齿类动物对应皮质醇)的含量升高。同时,它们的免疫系统倾向于更具敌意的状态。促炎信号白细胞介素‑1β水平升高,而具有镇静作用的白细胞介素‑10水平降低。大脑固有免疫细胞小胶质细胞处于更活跃状态。这些动物还显示出明显的氧化应激迹象:细胞膜脂质损伤的化学副产物增多,以及谷胱甘肽和超氧化物歧化酶等天然抗氧化物水平降低。相比之下,低易感性大鼠在激素、免疫和抗氧化指标上维持了更为平衡的状态。
将大脑开关与全身应激反应联系起来
通过结合行为、脑组织分析和血液测量,研究勾勒出一幅协调一致的图景。出现类PTSD症状的动物,其海马体内mGluR5被DNA甲基化抑制,同时应激激素高涨、炎症加剧、对氧化损伤的细胞防御衰弱。尽管也面临相同的创伤,那些保持韧性的动物则避免了这一整套变化。该研究在大鼠身上、并集中于一个脑区和一种表观遗传调控形式,但它强调了DNA上一处微小化学变化如何向外扩散,重塑大脑与全身的应激网络。 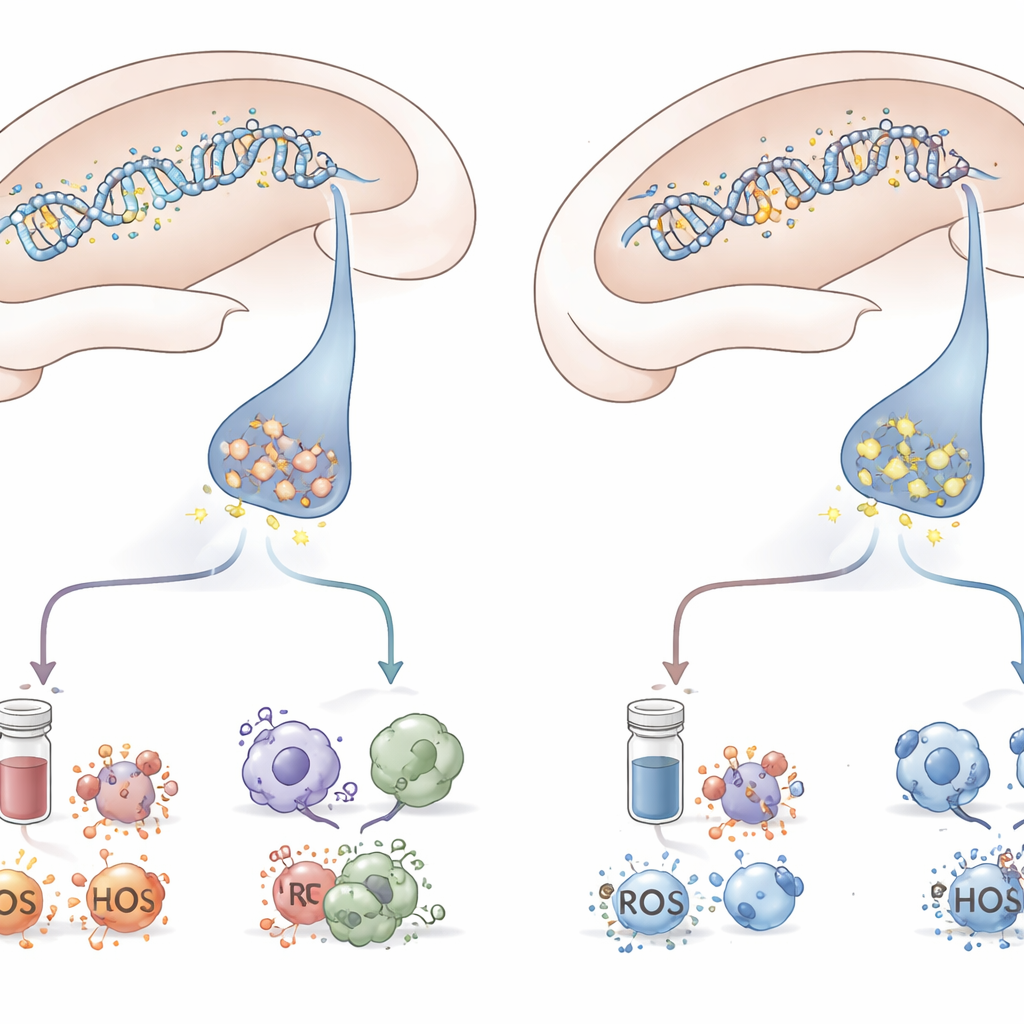
这对经历创伤的人意味着什么
对普通读者而言,核心信息是:对PTSD的易感性可能不仅取决于生活事件,还取决于创伤后我们基因的化学调谐方式。在这项研究中,mGluR5基因上更重的甲基化像刹车一样抑制了有益的脑受体,并与过度活跃的应激激素、隐隐的炎症和更大的细胞压力并存。这些发现提示,人类中类似的表观遗传标记未来或可帮助识别谁在创伤后风险最大,以指导早期支持与治疗。它们也暗示,旨在温和重置这些分子开关的疗法——无论是通过药物、生活方式改变,还是未来的表观遗传工具——或许有望将易感性转向韧性。
引用: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
关键词: 创伤后应激障碍, 表观遗传学, DNA甲基化, 应激韧性, 海马体