Clear Sky Science · ar
تنظيم التعبير الجيني اللاجيني لمستقبل الجلوكوكورتيكويد من خلال المثيلة مرتبط باضطراب ما بعد الصدمة
لماذا تنثني بعض العقول دون أن تنكسر
ليس كل من يعيش الحرب أو الاعتداء أو الكارثة يصاب باضطراب ما بعد الصدمة. هذا التفاوت في أثر الصدمة يطرح سؤالاً أساسياً: ما الذي يجعل دماغاً واحداً عرضة بينما يثبت آخر في وجهها؟ في هذه الدراسة على الفئران، نظر الباحثون تحت سطح السلوك إلى مستوى الوسوم الكيميائية على الحمض النووي، مستكشفين كيف يمكن لمفاتيح دقيقة في دوائر الإجهاد الدماغية أن تميل ببعض الأفراد نحو خوف وقلق ومزاج منخفض تستمر لفترة طويلة بعد الصدمة.
من حدث صادم واحد إلى نتائج مختلفة جداً
لتمثيل الصدمة، عرّض الفريق الفئران لتسلسل مكثف من المؤثرات المسببة للإجهاد — التقييد، السباحة القسرية، التعرض لأبخرة مخدرة، وصدمات كهربائية خفيفة — والمعروف بنموذج الإجهاد المطوّل المفرد. بعد ذلك تُركت الحيوانات لمدة أسبوع دون إزعاج ثم خضعت لسلسلة من الاختبارات القياسية التي تقيس سلوكيات تشبه اليأس والقلق وفقدان المتعة. على الرغم من أن كل الفئران واجهت نفس المحنة، إلا أن استجاباتها تباينت. أظهر بعضها خمولاً واضحاً في اختبار السباحة القسرية، وقلة استكشاف للمساحات المفتوحة، واهتماماً أقل بالماء المحلى؛ وصُنّف هؤلاء كحيوانات ذات قابلية عالية. تصرف آخرون مثل الفئران غير المتعرضة للإجهاد واعتُبروا منخفضي القابلية، كمؤشر على المرونة. 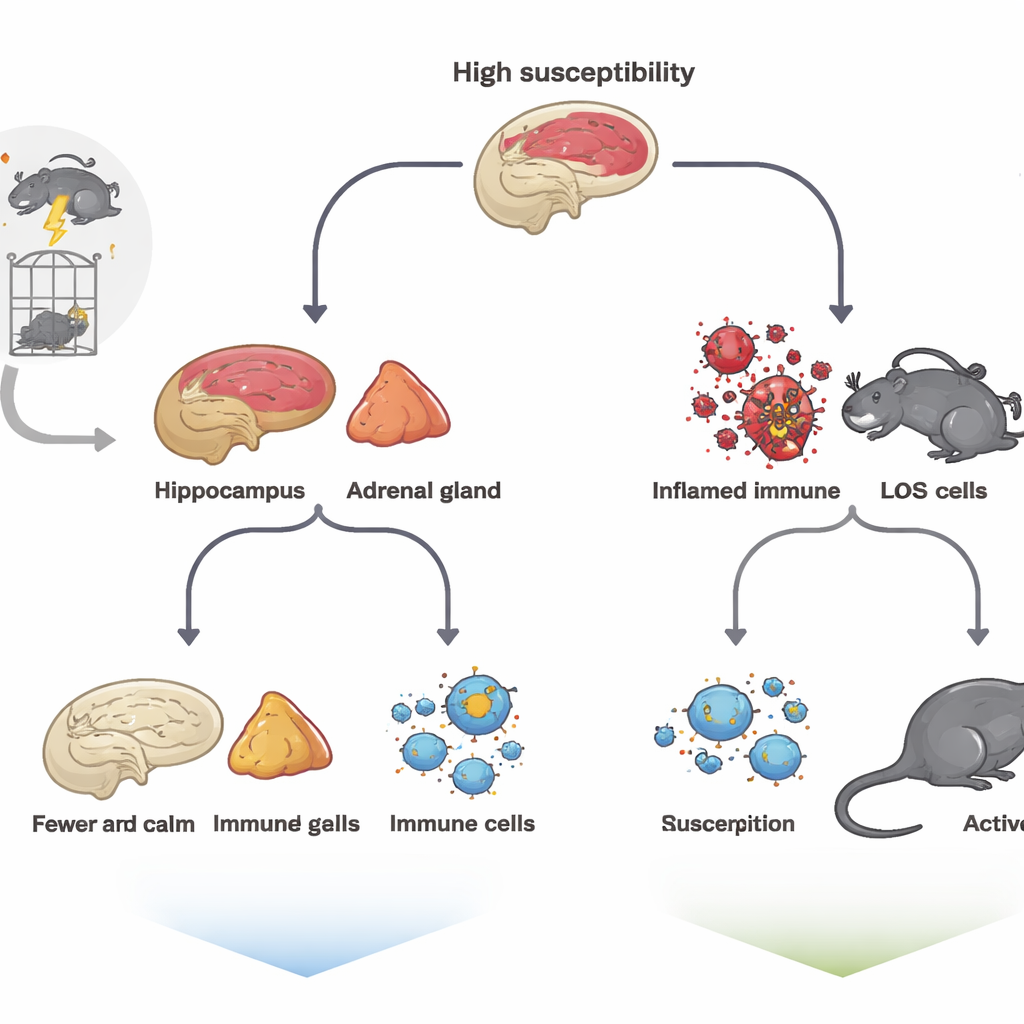
مفتاح كيميائي يخفت عمل مستقبل دماغي مهم
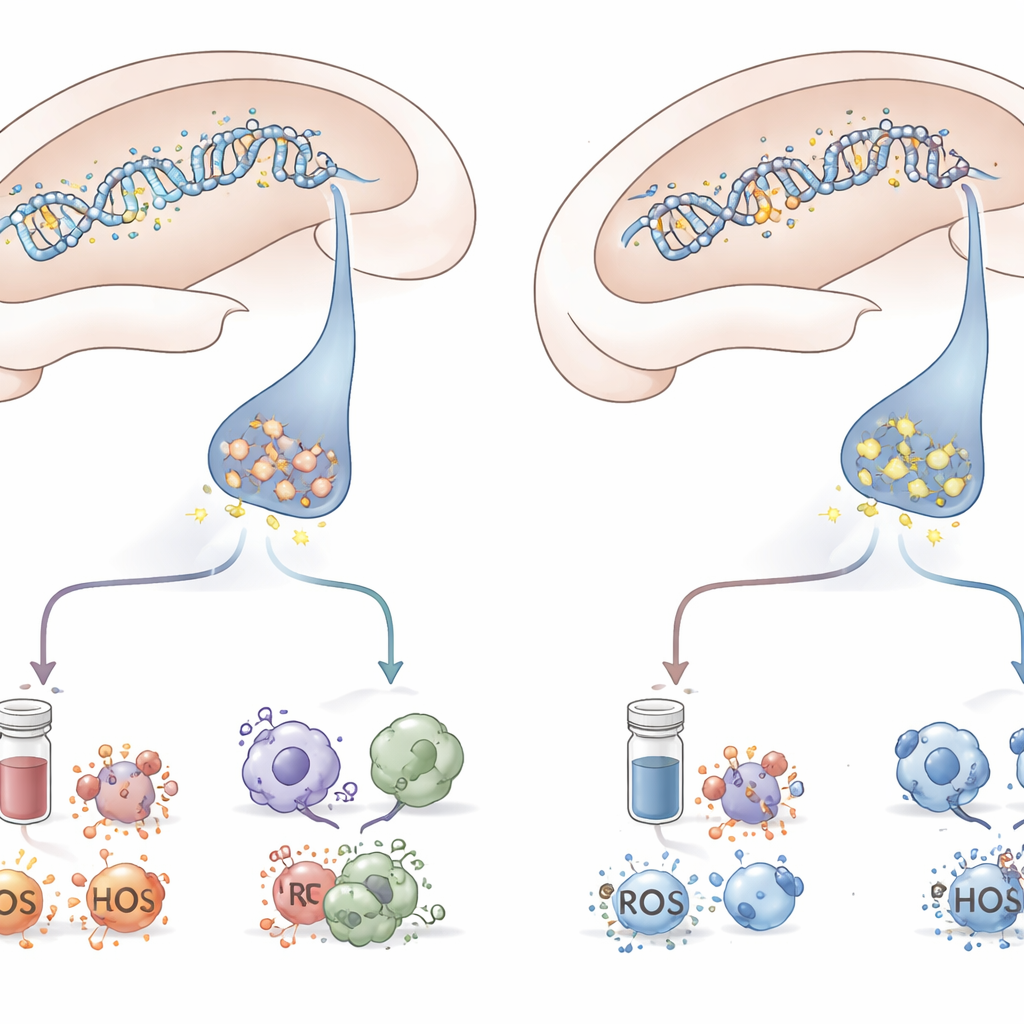
ركّز الباحثون على مستقبل في الدماغ يُدعى mGluR5، يساعد الخلايا العصبية على تعديل اتصالاتها ويشارك في تعلم الخوف وتنظيم العاطفة. بدلاً من البحث عن طفرات في جين المستقبل، فحصوا مثيلة الحمض النووي — وسوم كيميائية صغيرة تعمل كمفاتيح لتخفيف نشاط الجينات عادة عندما تتجمع في مواضع معينة. في الحصين، المنطقة الحيوية للذاكرة والسيطرة على الإجهاد، كان لدى الفئران ذات القابلية العالية نشاط أقل لجين mGluR5 ومثيلة أعلى في مواقع محددة بمنطقة التحكم في الجين. لم تُظهر الفئران منخفضة القابلية هذا النمط. يقترح اقتران الوسوم الكيميائية الأثقل مع النشاط الجيني المخفض أن تجربة الصدمة قد "أخفت" فعلياً مستقبلًا يساعد الدماغ عادة على التكيف مع الإجهاد.
هرمونات الإجهاد والالتهاب والتلف الخلوي
لم تحدث تغييرات ضبط الجين بمعزل عن غيرها. أظهرت الفئران ذات القابلية العالية ارتفاعاً في نظام الهرمونات الرئيسي المسؤول عن الإجهاد. كانت الخلايا في منطقة دماغية عميقة تطلق عامل تحرير الكورتيكوتروبين — وهو محفز رئيسي لسلسلة الاستجابة للإجهاد — أكثر نشاطاً، وكانت مستويات الكورتيكوستيرون في الدم، النظير القارض للكورتيزول، مرتفعة. في الوقت نفسه، مال جهاز المناعة لديهم إلى حالة أكثر عدائية. كانت مستويات إشارة التهابية منشّطة، إنترلوكين‑1β، أعلى، بينما كانت مستويات إشارة مهدئة، إنترلوكين‑10، أقل. كانت الخلايا الميكروغلية، خلايا المناعة المقيمة في الدماغ، أكثر تنشيطاً. كما أظهرت هذه الحيوانات علامات واضحة للإجهاد التأكسدي: مزيد من نواتج التحلل الكيميائي للدهون في أغشية الخلايا، وانخفاض في مستويات مضادات الأكسدة الطبيعية مثل الغلوتاثيون وإنزيم فرزوزديسميوتاز الفائق. بالمقابل، حافظت الفئران منخفضة القابلية على ملفات هرمونية ومناعية ومضادة للأكسدة أكثر توازناً.
ربط مفاتيح الدماغ بردود فعل الإجهاد في الجسم كله
بجمع السلوك وتحليل نسيج الدماغ وقياسات الدم، ترسم الدراسة صورة منسقة. كانت الحيوانات التي انسحقت أمام أعراض تشبه اضطراب ما بعد الصدمة هي نفسها التي قامت فيها مثيلة الحمض النووي بكبح mGluR5 في الحصين، بينما ارتفعت هرمونات الإجهاد واندلع الالتهاب وفشلت دفاعات الخلايا ضد الضرر التأكسدي. أولئك الذين ظلوا مرنين رغم خوضهم نفس المحنة تجنبوا هذا التسلسل الكامل من التغييرات. وعلى الرغم من أن العمل أُجري على فئران وتركز على منطقة دماغية واحدة وشكل واحد من الرقابة اللاجينية، إلا أنه يبرز كيف أن تغييرًا كيميائياً صغيرًا على الحمض النووي يمكن أن يمتد ليعيد تشكيل شبكات الإجهاد في الدماغ والجسم.
ما يعنيه هذا للأشخاص الذين يعيشون مع الصدمة
للقارئ العام، الرسالة الأساسية هي أن القابلية لاضطراب ما بعد الصدمة قد تعتمد ليس فقط على الأحداث الحياتية بل أيضاً على كيفية ضبط جيناتنا كيميائياً بعد الصدمة. في هذه الدراسة، عملت المثيلة الأثقل على جين mGluR5 كفرامل على مستقبل دماغي مفيد ورافقت ذلك هرمونات إجهاد مفرطة، والتهاب مستمر، وإجهاد خلوي أكبر. تشير هذه النتائج إلى أن علامات لاجينية مشابهة لدى البشر قد تساعد يومًا ما في تحديد من هم الأكثر عرضة بعد الصدمة، مما يوجّه التدخلات والدعم المبكر. وتلمح أيضاً إلى أن علاجات تهدف بلطف إلى إعادة ضبط هذه المفاتيح الجزيئية — سواء عبر أدوية أو تغييرات في نمط الحياة أو أدوات لاجينية مستقبلية — قد تساعد يوماً في تحويل التوازن من القابلية نحو المرونة.
الاستشهاد: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
الكلمات المفتاحية: اضطراب ما بعد الصدمة, علم فوق الجينات (الإبيجينيتيكس), مثيلة الحمض النووي, المرونة تجاه الإجهاد, الحصين