Clear Sky Science · es
La regulación epigenética del gen del receptor de glucocorticoides mediante metilación se vincula con el trastorno por estrés postraumático
Por qué algunas mentes se doblan pero no se rompen
No todas las personas que atraviesan la guerra, una agresión o un desastre desarrollan trastorno por estrés postraumático (TEPT). Este costo desigual del trauma plantea una pregunta fundamental: ¿qué hace que un cerebro sea vulnerable mientras otro resulta resiliente? En este estudio con ratas, los investigadores miraron debajo de la superficie del comportamiento hasta el nivel de etiquetas químicas en el ADN, explorando cómo interruptores sutiles en el circuito cerebral del estrés pueden inclinar a algunos individuos hacia el miedo, la ansiedad y el ánimo bajo de larga duración tras un trauma.
Del mismo evento traumático a resultados muy diferentes
Para imitar el trauma, el equipo expuso a las ratas a una secuencia intensa de estresores—restricción, nado forzado, exposición a vapores anestésicos y descargas eléctricas leves—conocida como el modelo de estrés prolongado único. Después, los animales quedaron en reposo durante una semana y luego se examinaron con una batería de pruebas estándar que miden comportamientos tipo desesperanza, ansiedad y pérdida de placer. Aunque todas las ratas habían afrontado la misma prueba, sus respuestas divergieron. Algunas mostraron inmovilidad marcada en la prueba de nado forzado, menor exploración de espacios abiertos y menos interés por agua azucarada; a estas se las etiquetó como animales de alta susceptibilidad. Otras se comportaron muy parecido a ratas no estresadas y se consideraron de baja susceptibilidad, un proxy de resiliencia. 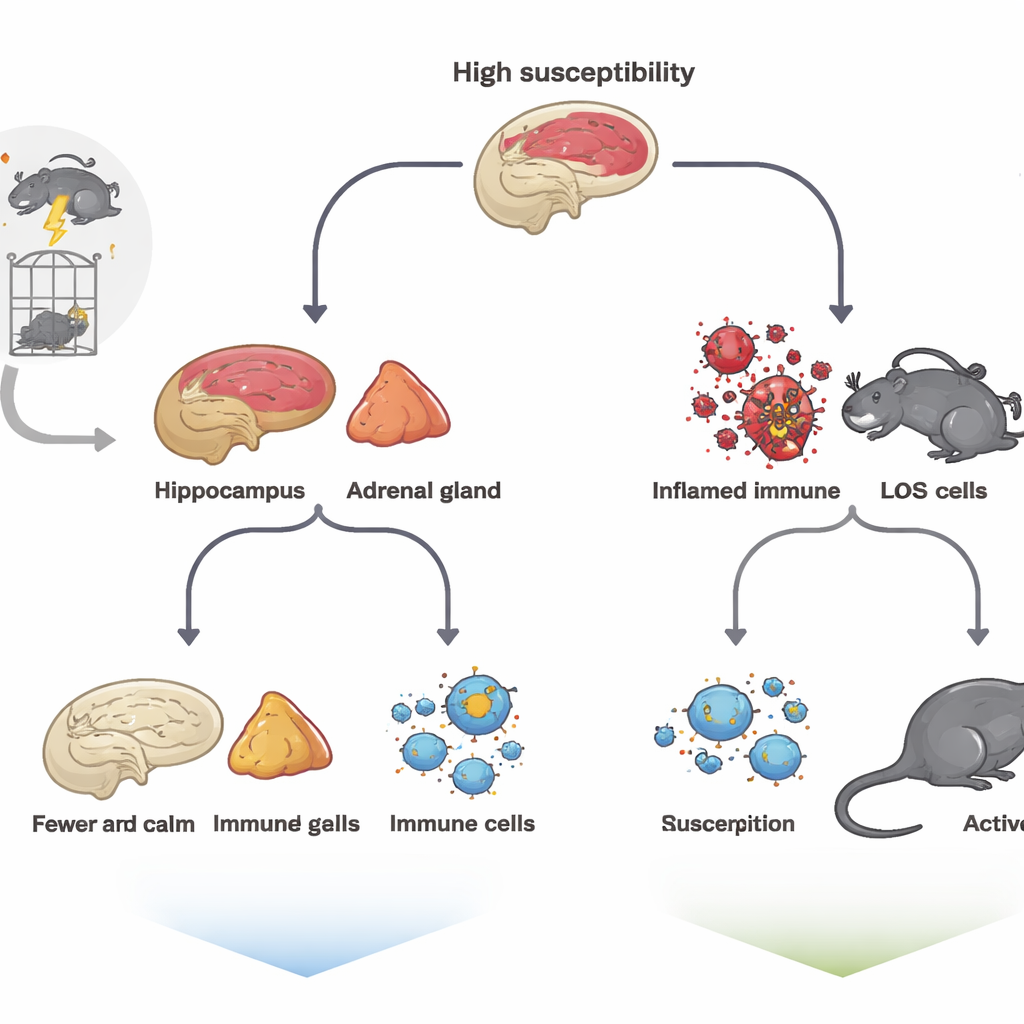
Un atenuador químico en un receptor cerebral clave
Los investigadores se centraron en un receptor cerebral llamado mGluR5, que ayuda a las neuronas a ajustar sus conexiones y participa en el aprendizaje del miedo y la regulación emocional. En lugar de buscar mutaciones en el gen del receptor, examinaron la metilación del ADN—pequeñas etiquetas químicas que actúan como atenuadores, generalmente reduciendo la expresión génica cuando se acumulan en ciertos sitios. En el hipocampo, una región crítica para la memoria y el control del estrés, las ratas de alta susceptibilidad mostraron tanto menor actividad del gen mGluR5 como mayor metilación en sitios específicos de la región de control del gen. Las ratas de baja susceptibilidad no presentaron este patrón. Esta combinación de mayor etiquetado químico con reducción de la actividad génica sugiere que la experiencia traumática había «rebajado» efectivamente un receptor que normalmente ayuda al cerebro a adaptarse al estrés.
Hormonas del estrés, inflamación y desgaste celular
Los cambios en el control génico no ocurrieron de forma aislada. Las ratas de alta susceptibilidad mostraron un pico en el principal sistema hormonal del estrés del organismo. Las células en una región profunda del cerebro que libera factor liberador de corticotropina—un desencadenante clave de la cascada del estrés—estaban más activas, y los niveles sanguíneos de corticosterona, el equivalente en roedores del cortisol, se encontraban elevados. Al mismo tiempo, sus sistemas inmunitarios se inclinaron hacia un estado más hostil. Los niveles de una señal proinflamatoria, la interleucina‑1β, eran más altos, mientras que los de la señal calmante interleucina‑10 eran más bajos. Las microglías, las células inmunitarias residentes del cerebro, presentaban mayor activación. Estos animales también mostraron signos claros de estrés oxidativo: más subproductos químicos derivados del daño a los lípidos de las membranas celulares y niveles reducidos de antioxidantes naturales como el glutatión y la superóxido dismutasa. Las ratas de baja susceptibilidad, en contraste, mantuvieron perfiles más equilibrados de hormonas, respuesta inmune y antioxidantes.
Vinculando interruptores cerebrales con respuestas de estrés de todo el organismo
Al combinar comportamiento, análisis de tejido cerebral y mediciones sanguíneas, el estudio dibuja un cuadro coordinado. Los animales que sucumbieron a síntomas tipo TEPT fueron aquellos en los que la metilación del ADN suprimió mGluR5 en el hipocampo, mientras las hormonas del estrés se disparaban, la inflamación estallaba y las defensas celulares frente al daño oxidativo flaqueaban. Los que permanecieron resilientes, pese a afrontar la misma experiencia, evitaron toda esta cascada de cambios. Aunque el trabajo se realizó en ratas y se centró en una región cerebral y una forma de control epigenético, subraya cómo un pequeño cambio químico en el ADN puede propagarse y remodelar las redes del estrés en el cerebro y el cuerpo.
Qué significa esto para las personas que viven con trauma
Para un lector no especializado, el mensaje central es que la vulnerabilidad al TEPT puede depender no solo de los eventos de la vida sino también de cómo se afinan químicamente nuestros genes tras un trauma. En este estudio, una mayor metilación del gen mGluR5 actuó como un freno sobre un receptor cerebral beneficioso y fue mano a mano con hormonas del estrés sobreactivadas, inflamación latente y mayor desgaste celular. Estos hallazgos sugieren que marcas epigenéticas similares en humanos podrían algún día ayudar a identificar a quienes tienen mayor riesgo tras un trauma, orientando intervenciones y tratamientos tempranos. También apuntan a que terapias dirigidas a reajustar suavemente estos interruptores moleculares—ya sea mediante fármacos, cambios en el estilo de vida o futuras herramientas epigenéticas—podrían en el futuro ayudar a inclinar la balanza de la susceptibilidad hacia la resiliencia.
Cita: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Palabras clave: trastorno por estrés postraumático, epigenética, metilación del ADN, resiliencia al estrés, hipocampo