Clear Sky Science · pl
Regulacja epigenetyczna genu receptora glukokortykoidowego przez metylację wiąże się z zespołem stresu pourazowego
Dlaczego niektóre umysły uginają się, lecz się nie łamią
Nie każdy, kto przeżyje wojnę, napaść czy katastrofę, rozwija zespół stresu pourazowego (PTSD). Ten nierównomierny ciężar traumy stawia podstawowe pytanie: co czyni jeden mózg podatnym, a inny odpornym? W badaniu na szczurach naukowcy zajrzeli głębiej niż zachowanie, na poziom chemicznych znaków na DNA, badając, jak subtelne przełączniki w obwodach stresu mózgu mogą przechylić niektóre osobniki w stronę długotrwałego lęku, strachu i obniżonego nastroju po traumie.
Z jednego traumatycznego wydarzenia do bardzo różnych konsekwencji
Aby naśladować traumę, zespół poddał szczury intensywnej sekwencji stresorów — unieruchomieniu, wymuszonemu pływaniu, ekspozycji na opary anestetyku i łagodnemu wstrząsowi elektrycznemu — znanej jako model pojedynczego przedłużonego stresu. Potem zwierzęta pozostawiono w spokoju na tydzień i poddano baterii standardowych testów mierzących zachowania przypominające beznadziejność, lęk oraz utratę przyjemności. Mimo że wszystkie szczury doświadczyły tego samego koszmaru, ich reakcje się rozeszły. Niektóre wykazywały nasilone bezruchy w teście wymuszonego pływania, zmniejszoną eksplorację otwartych przestrzeni i mniejsze zainteresowanie osłodzoną wodą; te oznaczono jako zwierzęta o wysokiej podatności. Inne zachowywały się podobnie do nienarażonych szczurów i uznano je za o niskiej podatności, co jest przybliżeniem odporności. 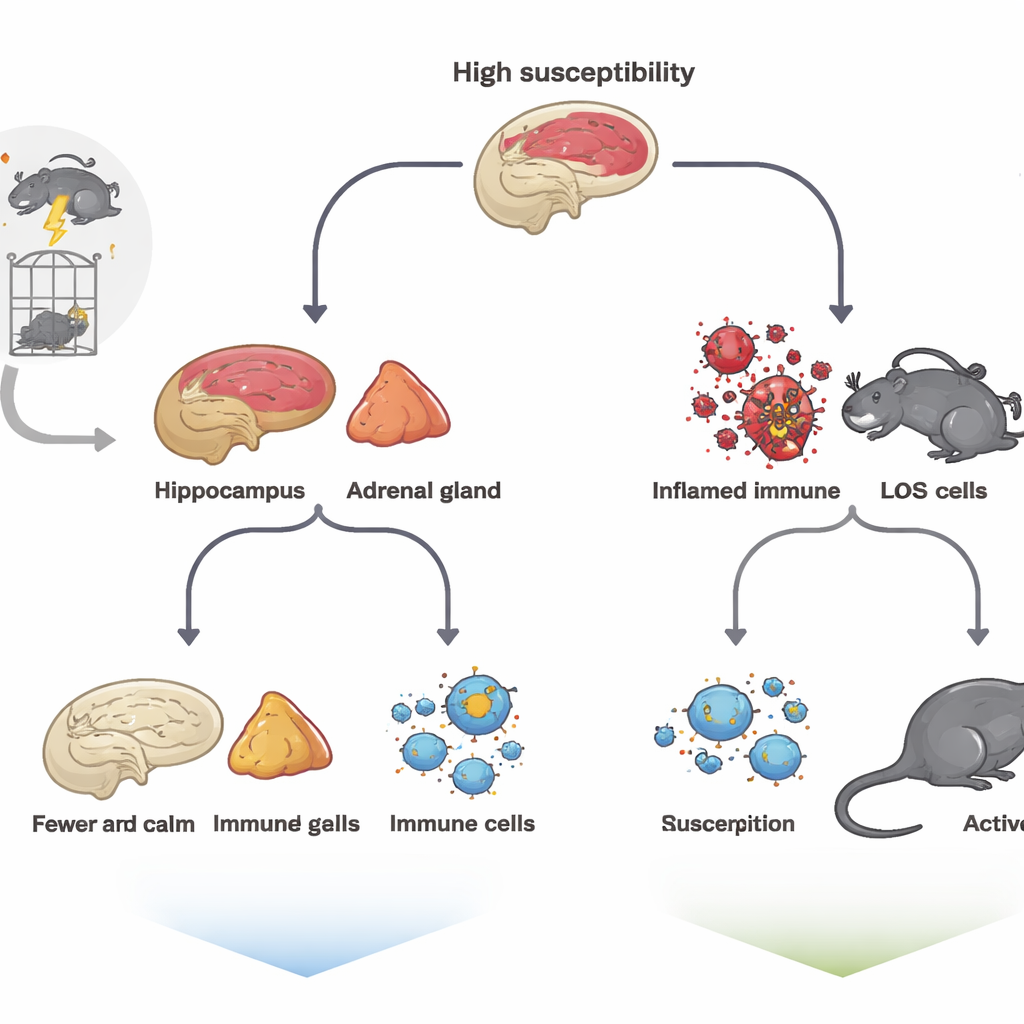
Chemiczny ściemniacz na kluczowym receptorze mózgu
Naukowcy skoncentrowali się na receptorze w mózgu zwanym mGluR5, który pomaga komórkom nerwowym dostosowywać połączenia i uczestniczy w uczeniu się strachu oraz regulacji emocji. Zamiast poszukiwać mutacji w genie receptora, zbadali metylację DNA — drobne chemiczne znaczniki działające jak ściemniacze, zwykle wyciszające geny, gdy gromadzą się w określonych miejscach. W hipokampie, obszarze kluczowym dla pamięci i kontroli stresu, szczury o wysokiej podatności miały zarówno niższą aktywność genu mGluR5, jak i wyższą metylację w określonych miejscach w regionie kontrolnym tego genu. Szczury o niskiej podatności nie wykazywały takiego wzorca. To skojarzenie cięższego chemicznego znakowania z obniżoną aktywnością genu sugeruje, że doświadczenie traumy skutecznie „przycisnęło” receptor, który zwykle pomaga mózgowi adaptować się do stresu.
Hormony stresu, zapalenie i zużycie komórek
Zmiany w kontroli genu nie zachodziły w izolacji. Szczury o wysokiej podatności wykazały wzrost aktywności głównego układu odpowiedzialnego za hormony stresu. Komórki w głębokim obszarze mózgu uwalniające czynnik uwalniający kortykotropinę — kluczowy wyzwalacz kaskady stresowej — były bardziej aktywne, a poziomy kortykosteronu we krwi, odpowiednika kortyzolu u gryzoni, były podwyższone. Jednocześnie ich układy odpornościowe przesunęły się w stronę stanu bardziej prozapalnego. Poziomy prozapalnego sygnału interleukiny‑1β były wyższe, podczas gdy poziomy uspokajającej interleukiny‑10 były niższe. Mikroglej, komórki odpornościowe mózgu, wykazywał większą aktywację. Zwierzęta te miały też wyraźne oznaki stresu oksydacyjnego: więcej produktów ubocznych uszkodzeń lipidów błon komórkowych oraz obniżone poziomy naturalnych przeciwutleniaczy, takich jak glutation i dysmutaza ponadtlenkowa. Szczury o niskiej podatności, przeciwnie, utrzymywały bardziej zrównoważone profile hormonalne, immunologiczne i antyoksydacyjne.
Łączenie przełączników mózgowych z reakcjami stresowymi całego organizmu
Poprzez połączenie zachowania, analizy tkanki mózgowej i pomiarów we krwi, badanie maluje zsynchronizowany obraz. Zwierzęta, które uległy objawom przypominającym PTSD, to te, u których metylacja DNA tłumiła mGluR5 w hipokampie, podczas gdy hormony stresu wzrastały, zapalenie nasilało się, a obrony komórek przed uszkodzeniem oksydacyjnym zawodziły. Te, które pozostały odporne, mimo że przeszły tę samą próbę, uniknęły całego łańcucha zmian. Chociaż badanie przeprowadzono na szczurach i skupiono się na jednym regionie mózgu oraz jednej formie kontroli epigenetycznej, podkreśla, jak mała chemiczna zmiana na DNA może rozlać się na całą sieć stresu w mózgu i ciele. 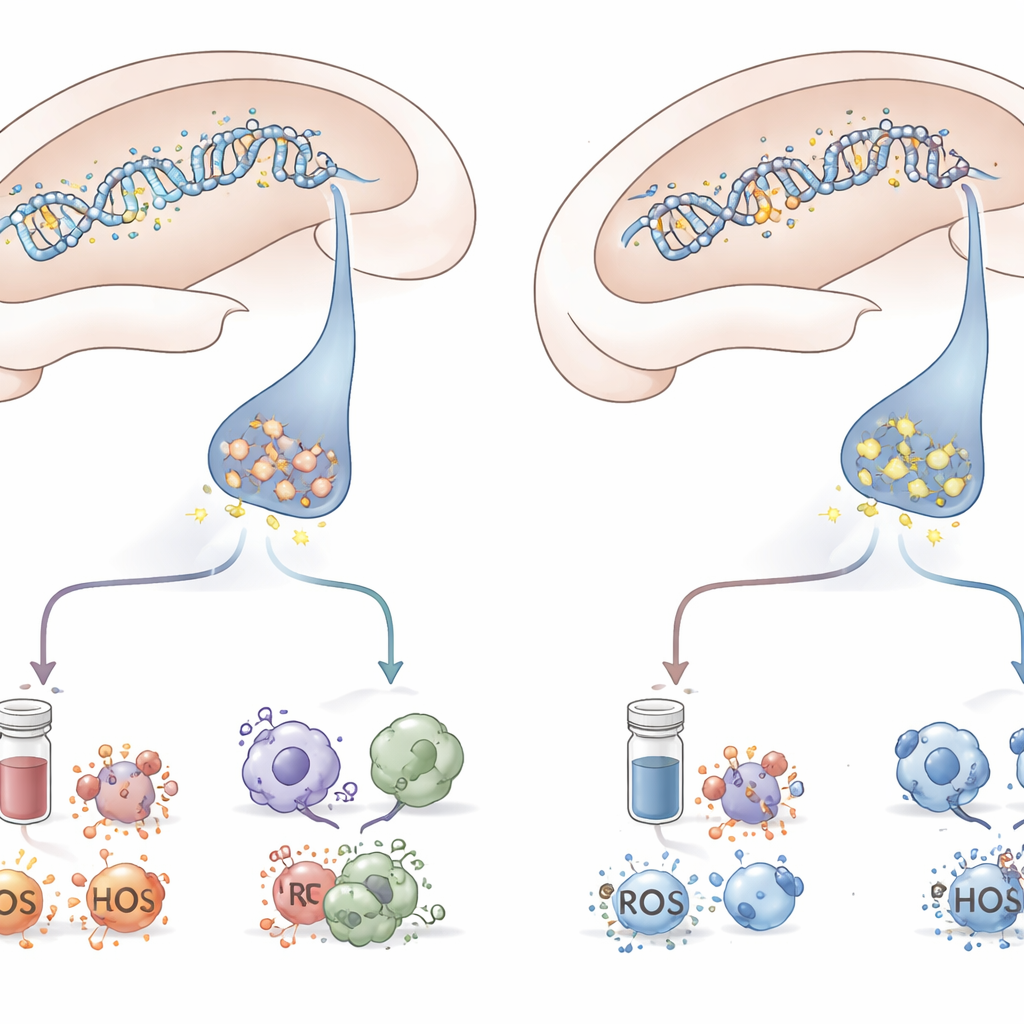
Co to znaczy dla ludzi żyjących z traumą
Dla czytelnika niebędącego specjalistą główny przekaz jest taki, że podatność na PTSD może zależeć nie tylko od wydarzeń życiowych, lecz także od tego, jak nasze geny zostają chemicznie dostrojone po traumie. W tym badaniu cięższa metylacja genu mGluR5 działała jak hamulec na pomocniczy receptor mózgu i szła w parze z nadaktywnością hormonów stresu, tlącym się zapaleniem i większym obciążeniem komórek. Wyniki te sugerują, że podobne znaki epigenetyczne u ludzi mogłyby w przyszłości pomóc zidentyfikować osoby o największym ryzyku po traumie, kierując wczesnym wsparciem i leczeniem. Sugerują też, że terapie mające na celu subtelne przywrócenie równowagi tych molekularnych przełączników — czy to za pomocą leków, zmian stylu życia, czy przyszłych narzędzi epigenetycznych — mogą kiedyś pomóc przesunąć balans od podatności ku odporności.
Cytowanie: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Słowa kluczowe: zespół stresu pourazowego, epigenetyka, metylacja DNA, odporność na stres, hipokamp