Clear Sky Science · de
Epigenetische Regulation des Glukokortikoidrezeptor-Gens durch Methylierung steht im Zusammenhang mit posttraumatischer Belastungsstörung
Warum manche Köpfe sich biegen, aber nicht brechen
Nicht jeder, der Krieg, Übergriff oder Katastrophe erlebt, entwickelt eine posttraumatische Belastungsstörung (PTBS). Diese ungleiche Belastung durch Traumata wirft eine grundlegende Frage auf: Was macht ein Gehirn verwundbar, während ein anderes widerstandsfähig bleibt? In dieser Rattenstudie schauten die Forschenden unter die Oberfläche des Verhaltens bis hin zu chemischen Markierungen auf der DNA und untersuchten, wie subtile Schalter in der Stressverschaltung des Gehirns einzelne Individuen nach einem Trauma zu anhaltender Angst, Furcht und gedrückter Stimmung neigen lassen können.
Vom einzelnen Trauma zu sehr unterschiedlichen Folgen
Um ein Trauma zu simulieren, setzten die Forschenden die Ratten einer intensiven Abfolge von Stressoren aus — Einschnürung, erzwungenes Schwimmen, Exposition gegenüber Narkosegasen und leichte elektrische Schocks — bekannt als das Single-Prolonged-Stress-Modell. Danach wurden die Tiere eine Woche lang in Ruhe gelassen und anschließend mit einer Reihe standardisierter Tests untersucht, die depressionsähnliches Verhalten, Angst und Verlust an Freude messen. Obwohl alle Ratten dasselbe Erlebnis durchlitten hatten, gingen ihre Reaktionen auseinander. Einige zeigten deutliche Bewegungsstarre im erzwungenen Schwimmtest, verringerte Erkundung offener Flächen und geringeres Interesse an gesüßtem Wasser; diese wurden als hoch anfällige Tiere eingestuft. Andere verhielten sich weitgehend wie ungestresste Ratten und galten als wenig anfällig — ein Proxy für Resilienz. 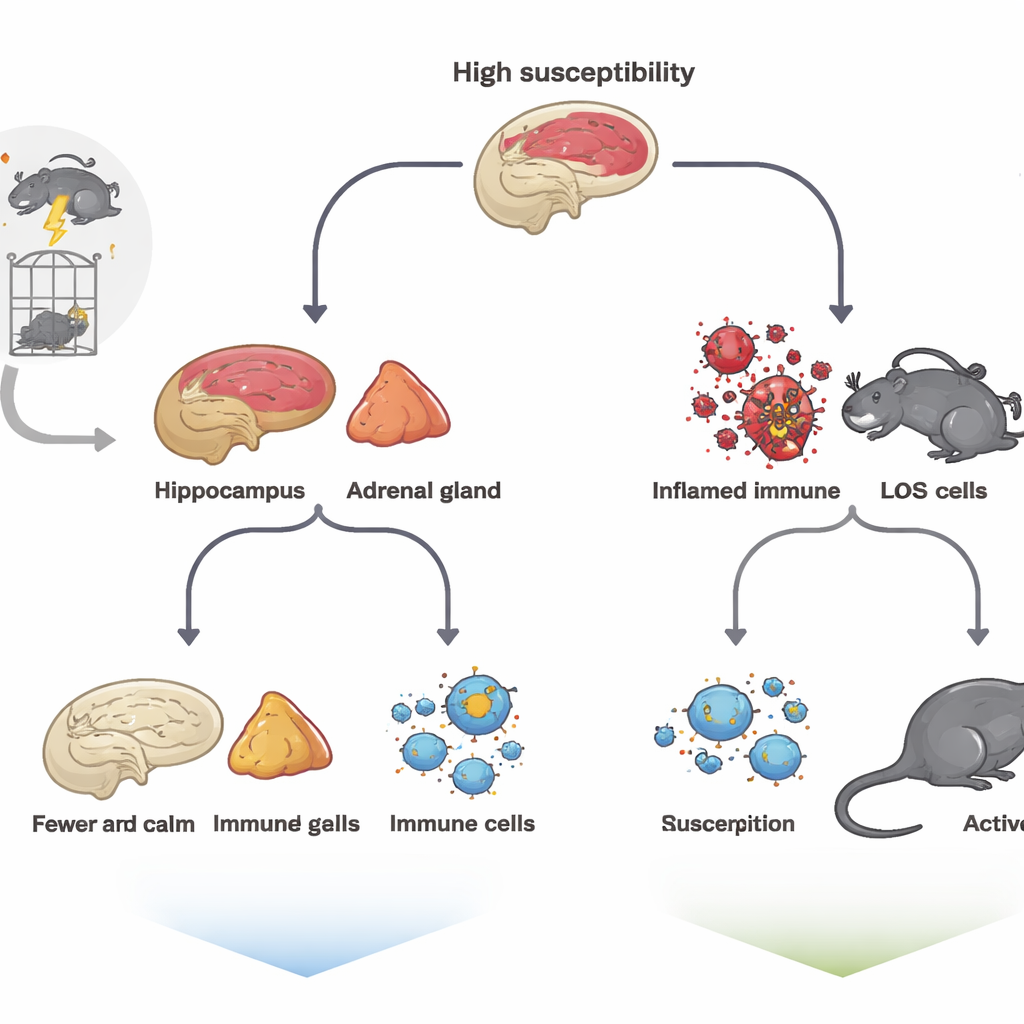
Ein chemischer Dimmer an einem wichtigen Gehirnrezeptor
Die Forschenden konzentrierten sich auf einen Rezeptor im Gehirn namens mGluR5, der Nervenzellen hilft, ihre Verbindungen anzupassen, und an Furchtlernen sowie emotionaler Regulation beteiligt ist. Anstatt nach Mutationen im Gen des Rezeptors zu suchen, untersuchten sie die DNA-Methylierung — kleine chemische Markierungen, die wie Dimmer wirken und Gene gewöhnlich dämpfen, wenn sie an bestimmten Stellen anreichern. Im Hippokampus, einer Region, die für Gedächtnis und Stresskontrolle wichtig ist, wiesen hoch anfällige Ratten sowohl eine geringere Aktivität des mGluR5-Gens als auch eine höhere Methylierung an spezifischen Stellen in der Kontrollregion des Gens auf. Wenig anfällige Ratten zeigten dieses Muster nicht. Dieses Zusammenspiel aus stärkerer chemischer Markierung und verringerter Genaktivität legt nahe, dass das Trauma den Rezeptor, der normalerweise dem Gehirn bei der Anpassung an Stress hilft, effektiv „abgedreht“ hat.
Stresshormone, Entzündung und zellulärer Verschleiß
Veränderungen in der Gensteuerung traten nicht isoliert auf. Hoch anfällige Ratten zeigten einen Anstieg im wichtigsten Stresshormonsystem des Körpers. Zellen in einer tiefen Hirnregion, die Corticotropin-releasing Factor freisetzt — ein zentraler Auslöser der Stresskaskade —, waren aktiver, und die Blutspiegel von Corticosteron, dem Gegenstück zu Cortisol bei Nagetieren, waren erhöht. Gleichzeitig neigte ihr Immunsystem zu einem feindlicheren Zustand. Die Spiegel eines proinflammatorischen Signals, Interleukin-1β, waren höher, während die Werte des beruhigenden Signals Interleukin-10 niedriger lagen. Mikroglia, die residenten Immunzellen des Gehirns, zeigten eine stärkere Aktivierung. Diese Tiere wiesen außerdem deutliche Zeichen oxidativen Stresses auf: mehr chemische Abbauprodukte von Schäden an Fetten in Zellmembranen und reduzierte Mengen natürlicher Antioxidantien wie Glutathion und Superoxiddismutase. Im Gegensatz dazu bewahrten wenig anfällige Ratten ausgeglichenere Profile von Hormonen, Immunreaktion und Antioxidantien.
Verknüpfung von Schaltern im Gehirn mit Stressreaktionen des gesamten Körpers
Durch die Kombination von Verhaltenstests, Analyse von Hirngewebe und Blutmessungen zeichnet die Studie ein koordiniertes Bild. Tiere, die PTBS-ähnlichen Symptomen erlagen, waren diejenigen, bei denen DNA-Methylierung mGluR5 im Hippokampus unterdrückte, während Stresshormone anstiegen, Entzündungen aufflammten und die zellulären Abwehrmechanismen gegen oxidative Schäden versagten. Diejenigen, die trotz desselben Erlebnisses resilient blieben, entgingen dieser vollständigen Kaskade von Veränderungen. Obwohl die Arbeit an Ratten durchgeführt wurde und sich auf eine Hirnregion sowie eine Form der epigenetischen Kontrolle konzentrierte, macht sie deutlich, wie eine kleine chemische Änderung an der DNA sich nach außen ausbreiten und Stressnetzwerke im Gehirn und Körper umgestalten kann. 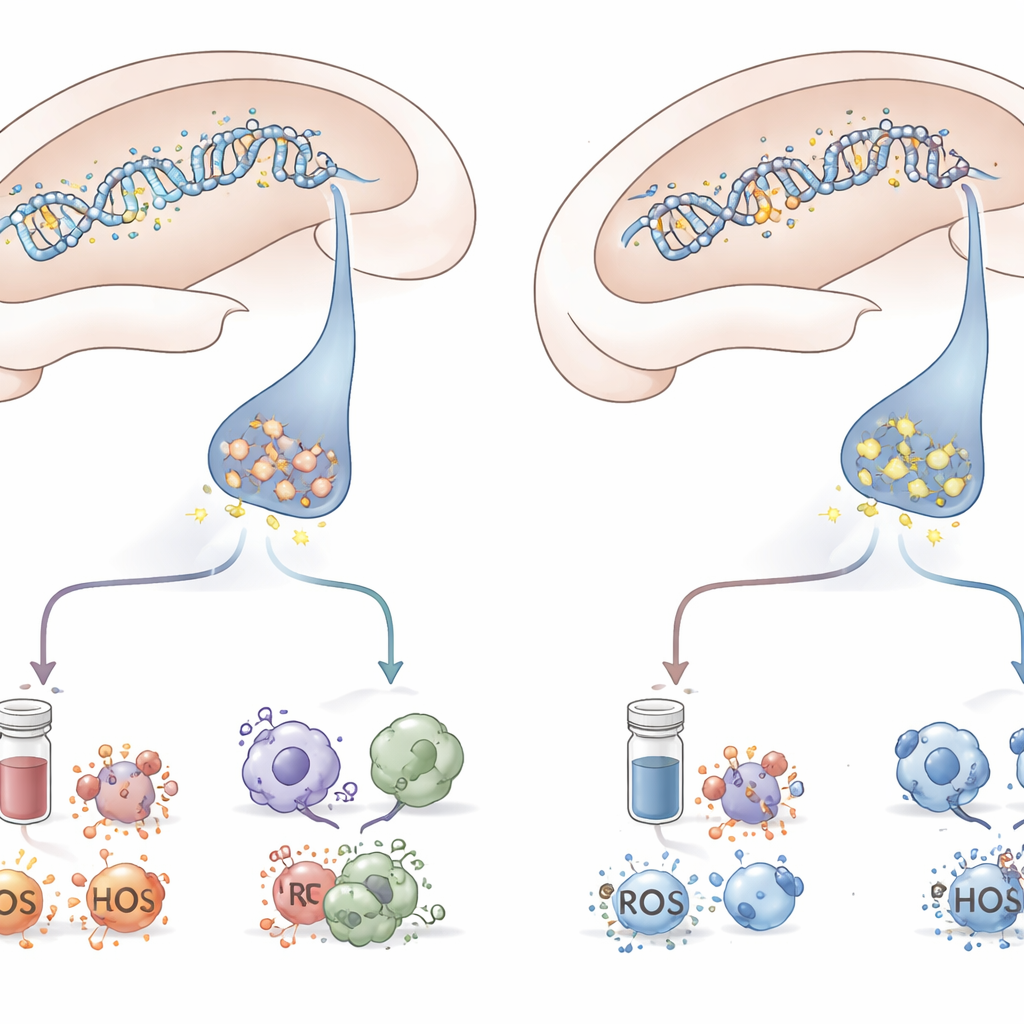
Was das für Menschen mit Traumata bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft, dass die Verwundbarkeit gegenüber PTBS möglicherweise nicht nur von Lebensereignissen abhängt, sondern auch davon, wie unsere Gene nach einem Trauma chemisch eingestellt werden. In dieser Studie wirkte stärkere Methylierung am mGluR5-Gen wie eine Bremse an einem hilfreichen Gehirnrezeptor und ging einher mit überaktiven Stresshormonen, schwelender Entzündung und größerer zellulärer Belastung. Die Ergebnisse legen nahe, dass ähnliche epigenetische Markierungen beim Menschen eines Tages helfen könnten, diejenigen zu identifizieren, die nach einem Trauma am stärksten gefährdet sind, und so frühe Unterstützung und Behandlung zu leiten. Sie deuten auch darauf hin, dass Therapien, die darauf abzielen, diese molekularen Schalter behutsam zurückzusetzen — sei es durch Medikamente, Lebensstiländerungen oder künftige epigenetische Werkzeuge — eines Tages dazu beitragen könnten, das Gleichgewicht von Anfälligkeit hin zu Resilienz zu verschieben.
Zitation: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Schlüsselwörter: posttraumatische Belastungsstörung, Epigenetik, DNA-Methylierung, Stressresilienz, Hippokampus