Clear Sky Science · it
La regolazione epigenetica del gene del recettore dei glucocorticoidi tramite metilazione è legata al disturbo da stress post-traumatico
Perché alcune menti si piegano ma non si spezzano
Non tutti coloro che attraversano guerra, aggressione o disastro sviluppano il disturbo da stress post-traumatico (PTSD). Questa distribuzione disomogenea delle conseguenze del trauma solleva una domanda fondamentale: cosa rende un cervello vulnerabile mentre un altro si dimostra resiliente? In questo studio sui ratti, i ricercatori hanno guardato al di sotto della superficie del comportamento, al livello dei tag chimici sul DNA, esplorando come piccoli interruttori nel circuito cerebrale dello stress possano inclinare alcuni individui verso paura, ansia e umore depresso di lunga durata dopo un trauma.
Dallo stesso evento traumatico a esiti molto diversi
Per imitare il trauma, il gruppo ha esposto i ratti a una sequenza intensa di stress—contenimento, nuoto forzato, esposizione a fumi anestetici e scosse elettriche lievi—nota come modello di stress prolungato singolo. Successivamente, gli animali sono stati lasciati indisturbati per una settimana e poi valutati con una batteria di test standard che misurano comportamenti simili alla disperazione, ansia e perdita di piacere. Nonostante tutti avessero affrontato lo stesso ordeal, le loro risposte sono divergenti. Alcuni mostravano marcata immobilità nel test del nuoto forzato, esplorazione ridotta di spazi aperti e minore interesse per acqua zuccherata; questi sono stati etichettati come animali ad alta suscettibilità. Altri si comportavano molto come i ratti non stressati e sono stati considerati a bassa suscettibilità, un proxy per la resilienza. 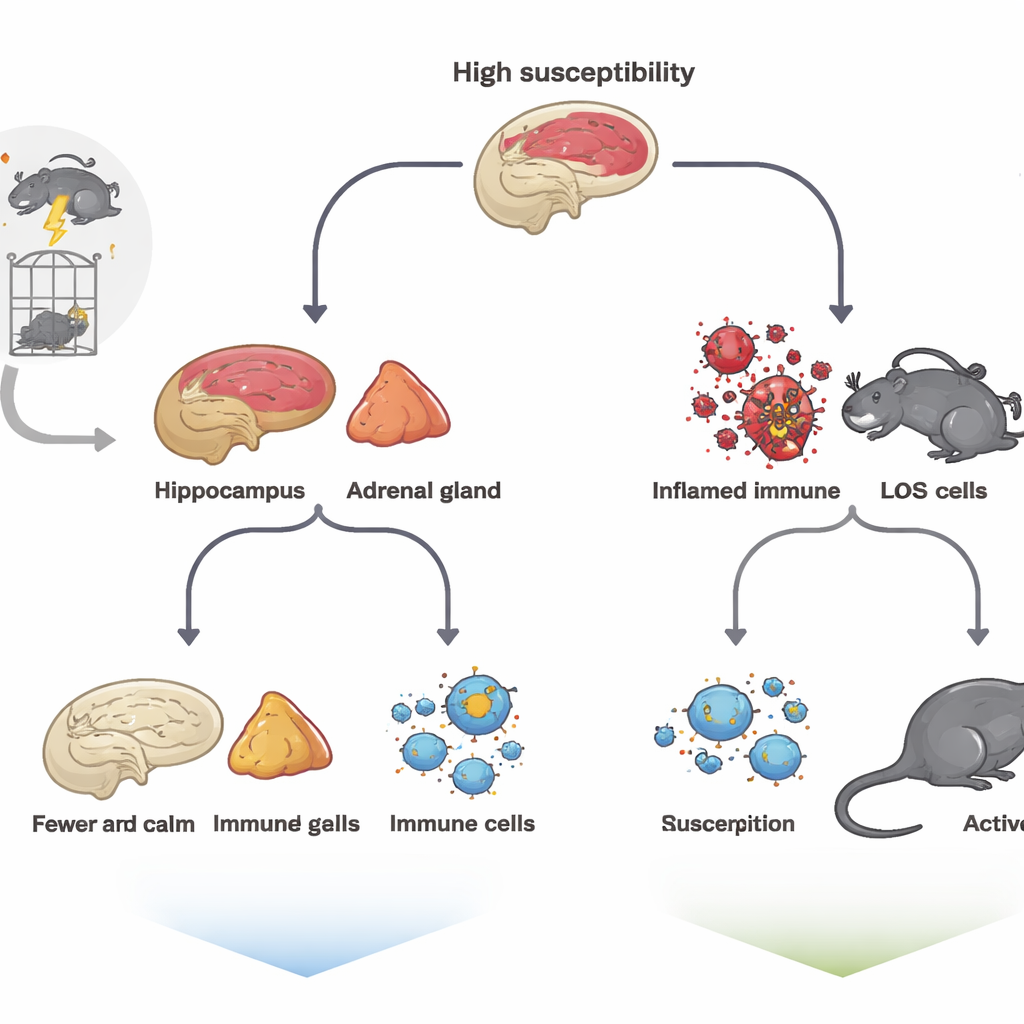
Un dimmer chimico su un recettore cerebrale chiave
I ricercatori si sono concentrati su un recettore nel cervello chiamato mGluR5, che aiuta le cellule nervose ad adattare le loro connessioni ed è coinvolto nell’apprendimento della paura e nella regolazione emotiva. Piuttosto che cercare mutazioni nel gene del recettore, hanno esaminato la metilazione del DNA—piccoli tag chimici che agiscono come dimmer, solitamente attenuando l’espressione genica quando si accumulano in punti specifici. Nell’ippocampo, una regione critica per la memoria e il controllo dello stress, i ratti ad alta suscettibilità avevano sia una minore attività del gene mGluR5 sia una maggiore metilazione in siti specifici della regione di controllo del gene. I ratti a bassa suscettibilità non mostravano questo schema. Questa associazione tra marcata etichettatura chimica e ridotta attività genica suggerisce che l’esperienza traumatica abbia effettivamente “abbassato” un recettore che normalmente aiuta il cervello ad adattarsi allo stress.
Ormoni dello stress, infiammazione e logoramento cellulare
I cambiamenti nel controllo genico non sono avvenuti in isolamento. I ratti ad alta suscettibilità mostravano un picco nel principale sistema ormonale dello stress dell’organismo. Le cellule in una regione profonda del cervello che rilasciano il fattore di rilascio della corticotropina—un trigger chiave della cascata dello stress—erano più attive, e i livelli ematici di corticosterone, l’equivalente rodentico del cortisolo, erano elevati. Allo stesso tempo, i loro sistemi immunitari tendevano verso uno stato più ostile. I livelli di un segnale pro-infiammatorio, l’interleuchina-1β, erano più alti, mentre quelli del segnale calmante interleuchina-10 erano più bassi. Le microglia, le cellule immunitarie residenti nel cervello, risultavano più attivate. Questi animali mostravano anche chiari segni di stress ossidativo: più sottoprodotti chimici del danno ai lipidi delle membrane cellulari e livelli ridotti di antiossidanti naturali come il glutatione e la superossido dismutasi. I ratti a bassa suscettibilità, al contrario, mantenevano profili più equilibrati di ormoni, immunità e antiossidanti.
Collegare gli interruttori cerebrali alle risposte di stress dell’intero organismo
Combinando comportamento, analisi del tessuto cerebrale e misurazioni del sangue, lo studio dipinge un quadro coordinato. Gli animali che sono ceduti a sintomi simili al PTSD erano quelli in cui la metilazione del DNA aveva soppresso mGluR5 nell’ippocampo, mentre gli ormoni dello stress aumentavano, l’infiammazione si accendeva e le difese cellulari contro il danno ossidativo vacillavano. Coloro che sono rimasti resilienti, nonostante avessero affrontato lo stesso ordeal, hanno evitato questa cascata completa di cambiamenti. Sebbene il lavoro sia stato condotto su ratti e si sia concentrato su una regione cerebrale e su una forma di controllo epigenetico, mette in luce come una piccola modifica chimica sul DNA possa riverberare fino a rimodellare le reti dello stress attraverso cervello e corpo. 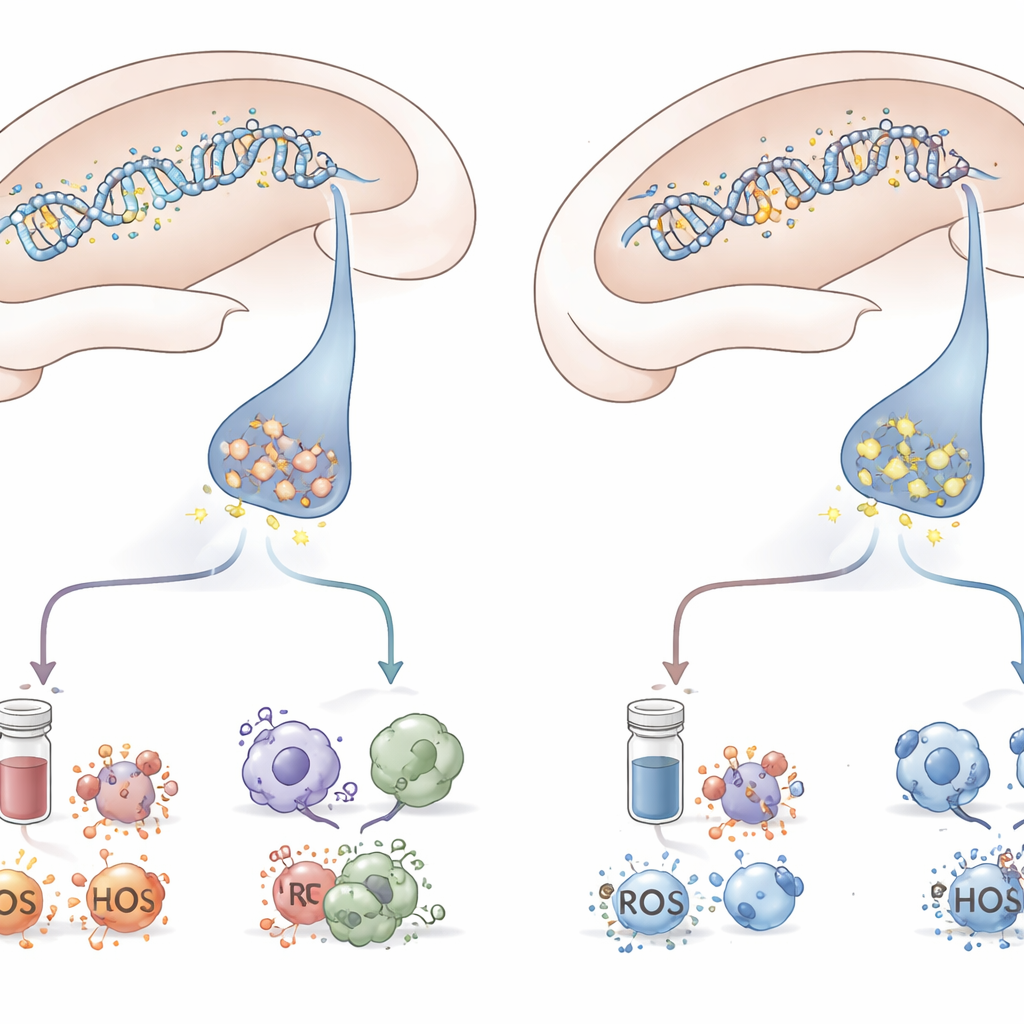
Che cosa significa per le persone che vivono il trauma
Per il lettore non specialista, il messaggio centrale è che la vulnerabilità al PTSD potrebbe dipendere non solo dagli eventi di vita ma anche da come i nostri geni vengono chimicamente regolati dopo un trauma. In questo studio, una metilazione più marcata sul gene mGluR5 ha agito come un freno su un recettore cerebrale utile e si è accompagnata a ormoni dello stress iperattivi, infiammazione latente e maggiore stress cellulare. Questi risultati suggeriscono che marchi epigenetici simili negli esseri umani potrebbero un giorno aiutare a identificare chi è a maggior rischio dopo un trauma, indirizzando interventi e trattamenti precoci. Suggeriscono inoltre che terapie volte a ripristinare delicatamente questi interruttori molecolari—sia tramite farmaci, cambiamenti dello stile di vita o futuri strumenti epigenetici—potrebbero un giorno aiutare a spostare l’equilibrio dalla suscettibilità verso la resilienza.
Citazione: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Parole chiave: disturbo da stress post-traumatico, epigenetica, metilazione del DNA, resilienza allo stress, ippocampo