Clear Sky Science · ru
Эпигенетическая регуляция гена глюкокортикоидного рецептора через метилирование связана с посттравматическим стрессовым расстройством
Почему одни умы гнутся, но не ломаются
Не все, кто пережил войну, нападение или стихийное бедствие, развивают посттравматическое стрессовое расстройство (ПТСР). Такое неравномерное влияние травмы порождает фундаментальный вопрос: что делает один мозг уязвимым, а другой — стойким? В этом исследовании на крысах учёные заглянули глубже поведения — на уровень химических меток на ДНК, изучая, как тонкие переключатели в нервной схеме стресса могут склонить одних особей к длительному страху, тревоге и низкому настроению после травмы.
От одного травматического события — к очень разным исходам
Чтобы смоделировать травму, команда подвергла крыс интенсивной последовательности стрессоров — фиксации, вынужденного плавания, воздействия анестезирующих паров и лёгкого электрического шока — известной как модель «одиночного длительного стресса». Затем животных оставляли в покое на неделю и тестировали стандартным комплексом испытаний, измеряющих поведение, похожее на отчаяние, тревожность и потерю удовольствия. Несмотря на то что все крысы пережили одно и то же испытание, их реакции разошлись. Некоторые проявляли выраженную неподвижность в тесте вынужденного плавания, уменьшенную исследовательскую активность в открытых пространствах и меньший интерес к подслащённой воде; их отнесли к группе с высокой восприимчивостью. Другие вели себя почти как нестрессированные животные и считались мало восприимчивыми — прокси‑показатель устойчивости. 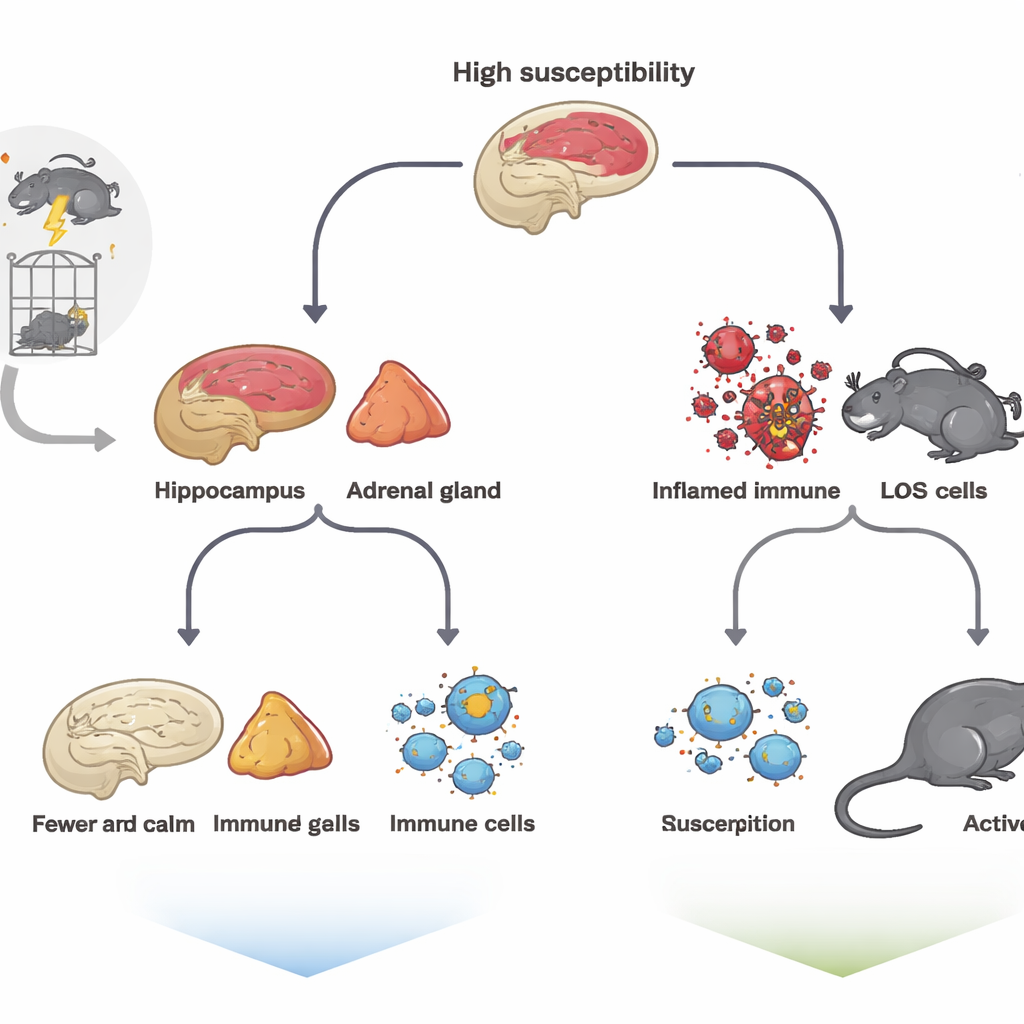
Химический регулятор на ключевом рецепторе мозга
Исследователи сосредоточились на рецепторе мозга под названием mGluR5, который помогает нейронам регулировать связи и участвует в обучении страху и эмоциональной регуляции. Вместо того чтобы искать мутации в гене рецептора, они изучали метилирование ДНК — небольшие химические метки, действующие как регуляторы яркости, обычно подавляющие экспрессию генов при накоплении в определённых участках. В гиппокампе, области, критичной для памяти и контроля стресса, крысы с высокой восприимчивостью показывали как пониженную активность гена mGluR5, так и повышенное метилирование в специфических участках регуляторной области гена. У мало восприимчивых животных такой картины не наблюдалось. Сочетание усиленной химической метки и сниженной активности гена позволяет предположить, что пережитая травма фактически «приглушила» рецептор, который обычно помогает мозгу адаптироваться к стрессу.
Гормоны стресса, воспаление и клеточный износ
Изменения в регуляции генов не происходили изолированно. У крыс с высокой восприимчивостью наблюдался всплеск активности основной гормональной системы стресса. Клетки в глубокой области мозга, выделяющие кортикотропин‑высвобождающий фактор — ключевой триггер стрессовой каскады — были более активны, а уровни кортикостерона в крови, аналогичного кортизолу у грызунов, были повышены. Одновременно их иммунная система сместилась в более про‑воспалительное состояние. Уровни провоспалительного сигнала интерлейкина‑1β были выше, тогда как противовоспалительного интерлейкина‑10 — ниже. Микроглия, собственные иммунные клетки мозга, были более активированы. Эти животные также демонстрировали явные признаки окислительного стресса: больше побочных продуктов повреждения липидов в клеточных мембранах и сниженные уровни природных антиоксидантов, таких как глутатион и супероксиддисмутаза. В отличие от них, мало восприимчивые крысы сохраняли более сбалансированные профили гормонов, иммунитета и антиоксидантов.
Связывая мозговые переключатели с реакциями всего организма на стресс
Комбинируя поведение, анализ тканей мозга и измерения в крови, исследование рисует скоординированную картину. Животные, поддавшиеся симптомам, похожим на ПТСР, были теми, у которых метилирование ДНК подавляло mGluR5 в гиппокампе, при этом усиливались гормоны стресса, разгоралось воспаление, и ослабевали клеточные защитные механизмы против окислительного повреждения. Те, кто оставался устойчивым, несмотря на одинаковое испытание, избегали этой полной цепочки изменений. Хотя работа выполнена на крысах и сфокусирована на одной области мозга и одном виде эпигенетического контроля, она подчёркивает, как небольшое химическое изменение на ДНК может распространиться и перестроить сети стресса по всему мозгу и телу. 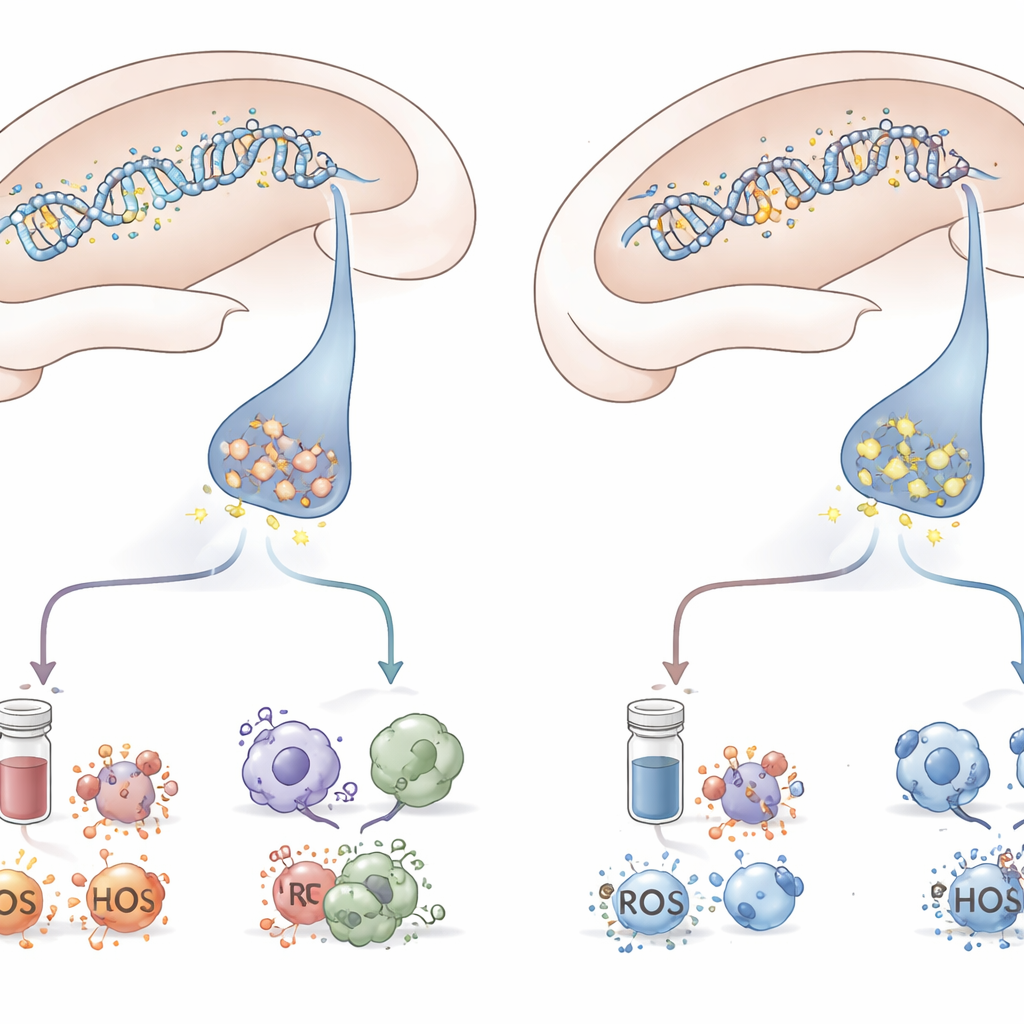
Что это означает для людей, переживших травму
Для широкого читателя главный вывод таков: восприимчивость к ПТСР может зависеть не только от жизненных событий, но и от того, как наши гены химически перенастраиваются после травмы. В этом исследовании усиленное метилирование гена mGluR5 действовало как тормоз для полезного рецептора мозга и сопровождалось гиперактивностью гормонов стресса, тлеющим воспалением и повышенным клеточным напряжением. Эти результаты позволяют предположить, что аналогичные эпигенетические метки у людей когда‑нибудь смогут помочь выявлять тех, кто находится в наибольшем риске после травмы, направляя раннюю поддержку и лечение. Они также намекают, что терапии, нацеленные на мягкую перенастройку этих молекулярных переключателей — будь то лекарства, изменения образа жизни или будущие эпигенетические инструменты — могут со временем помочь сдвинуть равновесие от восприимчивости к устойчивости.
Цитирование: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Ключевые слова: посттравматическое стрессовое расстройство, эпигенетика, метилирование ДНК, устойчивость к стрессу, гиппокамп