Clear Sky Science · he
ויסות אפיגנטי של גן הקולטן לגלוקוקורטיקואידים באמצעות מתילציה מקושר להפרעה פוסט‑טראומטית
מדוע מוחות מסוימים מעקמים אך אינם נשברים
לא כל מי שעובר מלחמה, מתקפה או אסון מפתח הפרעה פוסט‑טראומטית (PTSD). ההשפעה הבלתי שווה של הטראומה מעלה שאלה בסיסית: מה הופך מוח אחד לפגיע בעוד אחר עמיד? במחקר זה על חולדות חקרו החוקרים מתחת לפני השטח של ההתנהגות עד לרמה של תגים כימיים על ה‑DNA, ובחנו כיצד מתגים עדינים במעגלי הלחץ של המוח עשויים להטות חלק מהפרטים לעבר פחד, חרדה ומצב רוח ירוד מתמשכים לאחר טראומה.
מאירוע טראומטי אחד לתוצאות שונות מאוד
כדי לדמות טראומה, הצוות חשף את החולדות לרצף אינטנסיבי של גורמי לחץ — כבילה, שחייה מאולצת, חשיפה לאדים של חומרי הרדמה וחשמול קל — הידוע כמודל ה‑single prolonged stress. לאחר מכן, בעלי החיים הושארו ללא הפרעה במשך שבוע ונבדקו במערך מבחנים סטנדרטי שמודד התנהגויות של ייאוש, חרדה ואובדן הנאה. למרות שכל החולדות עברו את אותו עינוי, תגובותיהן נבדלו. חלקן הציגו חוסר תנועה בולט במבחן השחייה האילצתית, חקר נמוך של מרחבים פתוחים ופחות עניין במים ממותקים; אלו סווגו כבעלי פגיעה גבוהה. אחרות התנהגו בדומה לחולדות שלא נחשפו ללחץ ונחשבו לבעלות פגיעה נמוכה, שקול לחוסן. 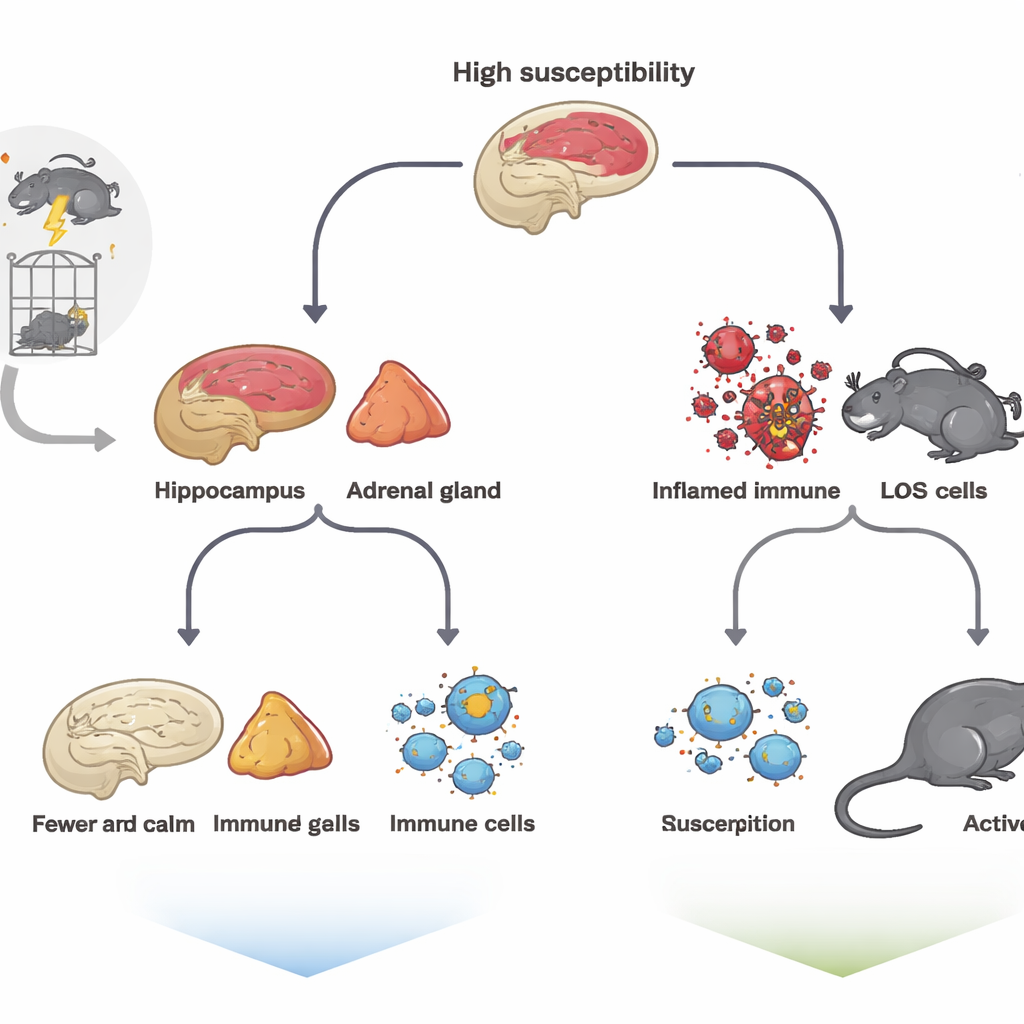
מתג דימר כימי על קולטן מרכזי במוח
החוקרים התמקדו בקולטן במוח הקרוי mGluR5, המסייע לנוירונים לכוונן את הקשרים שלהם ומשתתף בלמידת פחד ובויסות רגשי. במקום לחפש מוטציות בגן של הקולטן, בדקו את מתילציית ה‑DNA — תגים כימיים קטנים שמהתנהגותם דומים למתגי דימר, שלרוב מדכאים ביטוי גנים כשהם מצטברים במיקומים מסוימים. בהיפוקמפוס, אזור החשוב לזיכרון ולבקרת לחץ, חולדות בעלות פגיעה גבוהה הראו גם פעילות נמוכה יותר של גן ה‑mGluR5 וגם מתילציה גבוהה יותר באתרים ספציפיים באזור הבקרה של הגן. חולדות בעלות פגיעה נמוכה לא הראו דפוס זה. שילוב של תיוג כימי כבד יותר יחד עם פעילות גנטית מופחתת מרמז שהחוויה הטראומטית "הורידה" בפועל קולטן אשר בדרך כלל מסייע למוח להסתגל ללחץ.
הורמוני לחץ, דלקת ובלאי תאי
השינויים בבקרת הגנים לא התרחשו בבדידות. חולדות בעלות פגיעה גבוהה הראו זינוק במערכת ההורמונלית המרכזית של הלחץ. תאים באיזור עמוק במוח שמשחרר את החומר משחרר‑קורטיקוטרופין — טריגר מרכזי של מפל הלחץ — היו פעילים יותר, ורמות הדם של קורטיקוסטרון, המקביל הרודנטי של קורטיזול, היו מוגברות. במקביל, מערכת החיסון נטתה למצב יותר עוין. רמותו של אות פרו‑דלקתי, אינטרלוקין‑1β, היו גבוהות יותר, בעוד רמות האות המרגיע אינטרלוקין‑10 היו נמוכות יותר. המיקרוגליה, תאי החיסון התושבים של המוח, היו פעילים יותר. בעלי החיים הללו הראו גם סימנים ברורים של לחץ חמצוני: תוצרי לוואי כימיים של נזק לשומנים בממברנות התאים היו מוגברים, ורמות של נוגדי חמצון טבעיים כגון גלוטתיון וסופראוקסיד דיסמוטאז היו מופחתות. חולדות בעלות פגיעה נמוכה, לעומת זאת, שמרו על פרופילים מאוזנים יותר של הורמונים, מערכת חיסון ונוגדי חמצון.
קישור בין מתגי מוח לתגובות לחץ בכל הגוף
באמצעות שילוב של התנהגות, ניתוח רקמות מוח ומדידות דם, המחקר מצייר תמונה מתואמת. בעלי החיים שנכנעו לתסמינים דמויי PTSD היו אלה שבהם מתילציית ה‑DNA דיכאה את mGluR5 בהיפוקמפוס, בעוד הורמוני הלחץ עלו, הדלקת פרצה וההגנות התאית מפני נזק חמצוני נחלשו. אלה שנשארו חסונים, על אף שעברו את אותה חוויה, נמנעו מפלג השינויים המלא הזה. אף שהמחקר בוצע בחולדות והתמקד באזור מוח אחד ובצורת בקרה אפיגנטית אחת, הוא מדגיש כיצד שינוי כימי קטן על DNA יכול להדהד החוצה ולשנות רשתות לחץ במוח ובגוף.
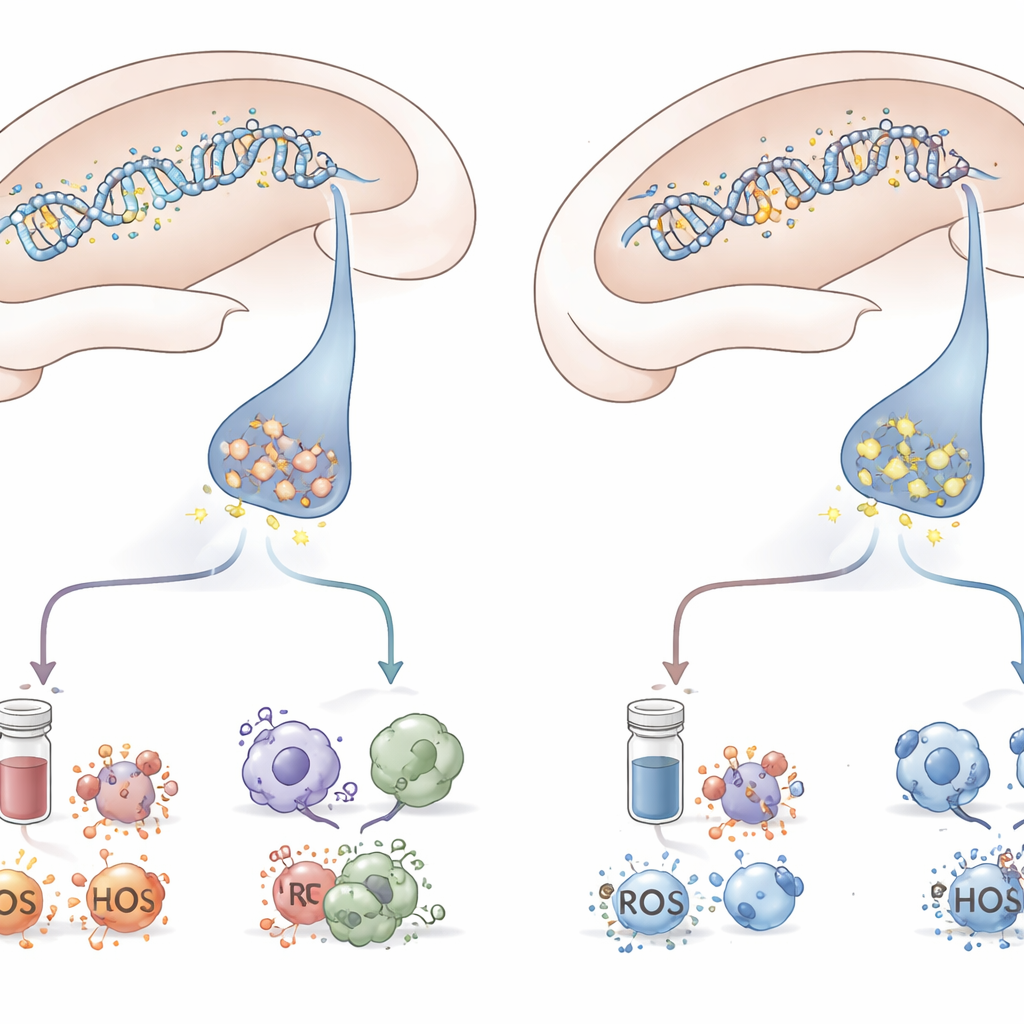
מה המשמעות עבור אנשים החיים עם טראומה
לקורא שאינו מומחה, המסר המרכזי הוא שפגיעות ל‑PTSD עשויה להימשך לא רק על רקע אירועי חיים אלא גם בהתאם לאופן שבו הגנים שלנו מכווננים כימית לאחר טראומה. במחקר זה, מתילציה כבדה יותר על גן ה‑mGluR5 פעלה כבלם על קולטן מועיל במוח והלכה יחד עם פעילות יתר של הורמוני לחץ, דלקת חבויה ומתח תאי מוגבר. ממצאים אלה מרמזים כי סימנים אפיגנטיים דומים בבני אדם עשויים בעתיד לסייע לזהות מי בסיכון הגבוה ביותר לאחר טראומה, ולהנחות תמיכה וטיפול מוקדמים. הם גם מרמזים שטיפולים שמטרתם לכוונן בעדינות את המתגים המולקולריים האלה — בין אם בתרופות, שינויי אורח חיים או כלים אפיגנטיים עתידיים — עשויים יום אחד לסייע להזיז את האיזון מפגיעות לכיוון חוסן.
ציטוט: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
מילות מפתח: הפרעה פוסט‑טראומטית, אפיגנטיקה, מתילציה של DNA, חוסן ללחץ, היפוקמפוס