Clear Sky Science · pt
Regulação epigenética do gene do receptor de glicocorticoide por metilação está ligada ao transtorno de estresse pós‑traumático
Por que algumas mentes se curvam, mas não se quebram
Nem todo indivíduo que vivencia guerra, agressão ou desastre desenvolve transtorno de estresse pós‑traumático (TEPT). Esse impacto desigual do trauma levanta uma questão básica: o que torna um cérebro vulnerável enquanto outro se mostra resiliente? Neste estudo com ratos, os pesquisadores olharam além do comportamento, para o nível das marcas químicas no DNA, explorando como interruptores sutis na rede cerebral do estresse podem inclinar alguns indivíduos para medo, ansiedade e humor baixo de longa duração após o trauma.
De um evento traumático para desfechos muito diferentes
Para mimetizar o trauma, a equipe expôs ratos a uma sequência intensa de estressores — contenção, natação forçada, exposição a vapores anestésicos e choque elétrico leve — conhecida como modelo de estresse prolongado único. Depois, os animais ficaram sem perturbações por uma semana e então foram avaliados com um conjunto de testes padrão que medem comportamento análogo ao desespero, ansiedade e perda de prazer. Embora todos os ratos tenham enfrentado o mesmo sofrimento, suas respostas divergiram. Alguns apresentaram imobilidade marcante no teste de natação forçada, exploração reduzida de espaços abertos e menor interesse por água adoçada; esses foram rotulados como animais de alta susceptibilidade. Outros comportaram‑se de forma semelhante aos ratos não estressados e foram considerados de baixa susceptibilidade, um substituto para resiliência. 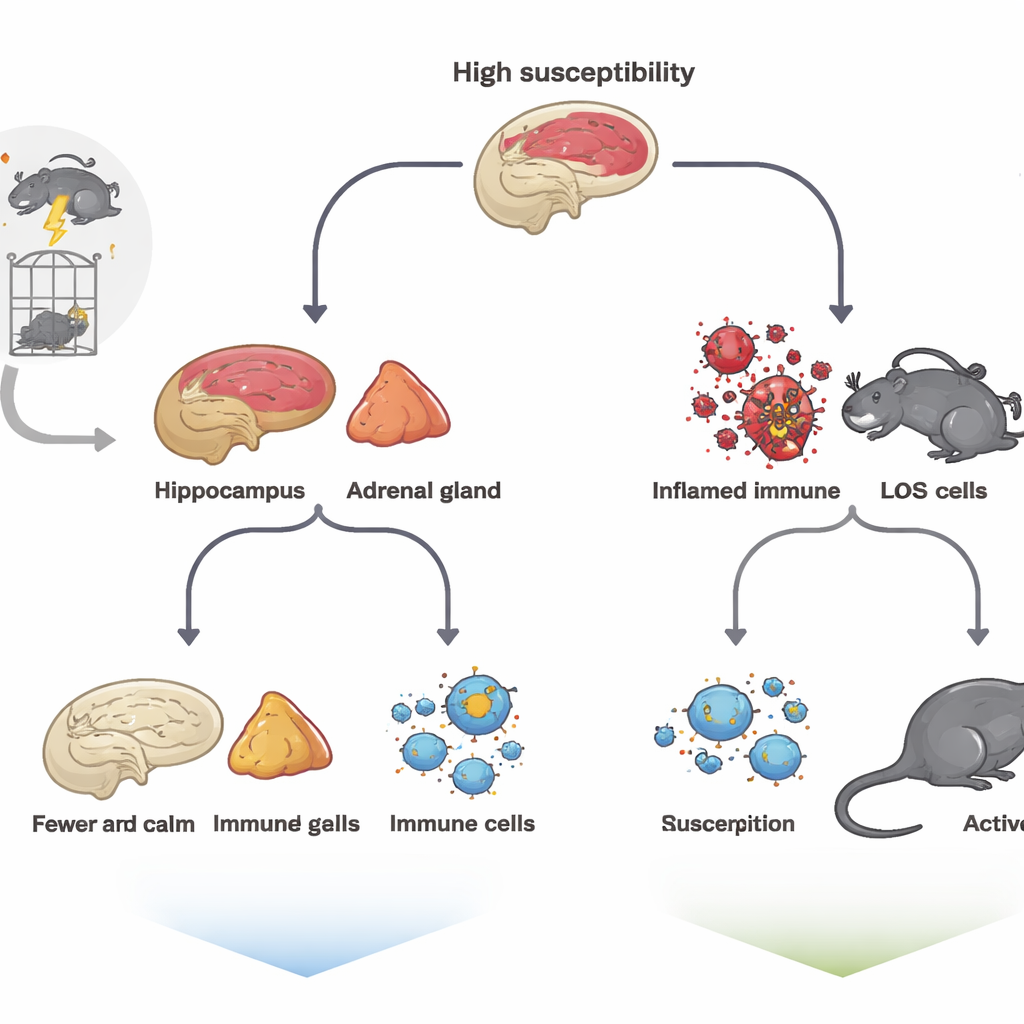
Um dimmer químico sobre um receptor cerebral chave
Os pesquisadores focaram em um receptor no cérebro chamado mGluR5, que ajuda os neurônios a ajustar suas conexões e está envolvido na aprendizagem do medo e na regulação emocional. Em vez de procurar mutações no gene do receptor, eles examinaram a metilação do DNA — pequenas marcas químicas que agem como dimmers, geralmente diminuindo a expressão gênica quando se acumulam em pontos específicos. No hipocampo, uma região crítica para memória e controle do estresse, ratos de alta susceptibilidade apresentaram tanto menor atividade do gene mGluR5 quanto maior metilação em sítios específicos da região regulatória do gene. Ratos de baixa susceptibilidade não exibiram esse padrão. Esse acoplamento de marcação química mais intensa com redução da atividade gênica sugere que a experiência traumática efetivamente “reduziu” um receptor que normalmente ajuda o cérebro a se adaptar ao estresse.
Hormônios do estresse, inflamação e desgaste celular
As mudanças no controle gênico não ocorreram isoladamente. Ratos de alta susceptibilidade mostraram um pico no principal sistema hormonal do estresse do organismo. Células em uma região profunda do cérebro que liberam o fator liberador de corticotropina — um gatilho chave da cascata do estresse — estavam mais ativas, e os níveis sanguíneos de corticosterona, o equivalente rodentil do cortisol, estavam elevados. Ao mesmo tempo, seus sistemas imunológicos inclinaram‑se para um estado mais hostil. Níveis de um sinal pró‑inflamatório, interleucina‑1β, eram maiores, enquanto os níveis do sinal calmante interleucina‑10 eram menores. As microglias, as células imunológicas residentes do cérebro, estavam mais ativadas. Esses animais também apresentaram sinais claros de estresse oxidativo: mais subprodutos químicos do dano a lipídios das membranas celulares e níveis reduzidos de antioxidantes naturais como glutationa e superóxido dismutase. Ratos de baixa susceptibilidade, em contraste, mantiveram perfis hormonais, imunes e antioxidantes mais equilibrados.
Ligando os interruptores cerebrais às respostas de estresse do corpo inteiro
Ao combinar comportamento, análise de tecido cerebral e medições sanguíneas, o estudo traça um quadro coordenado. Os animais que sucumbiram a sintomas análogos ao TEPT foram aqueles em que a metilação do DNA suprimiu mGluR5 no hipocampo, enquanto os hormônios do estresse dispararam, a inflamação irrompeu e as defesas celulares contra o dano oxidativo enfraqueceram. Aqueles que permaneceram resilientes, apesar de enfrentarem o mesmo sofrimento, evitaram essa cascata completa de mudanças. Embora o trabalho tenha sido feito em ratos e focado em uma região cerebral e em uma forma de controle epigenético, ele ressalta como uma pequena mudança química no DNA pode repercutir e remodelar redes de estresse por todo o cérebro e o corpo. 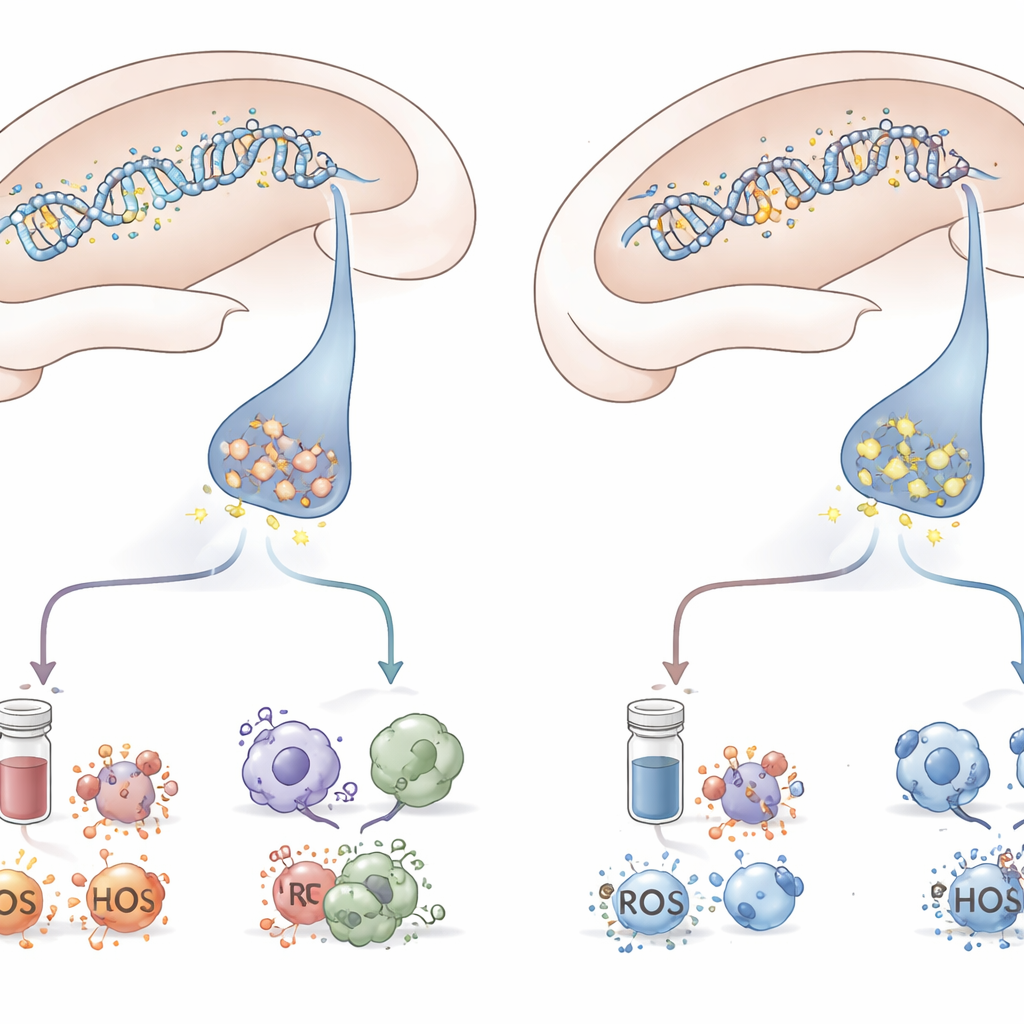
O que isso significa para pessoas que vivem com trauma
Para o leitor leigo, a mensagem central é que a vulnerabilidade ao TEPT pode depender não apenas dos eventos de vida, mas também de como nossos genes são afinados quimicamente após o trauma. Neste estudo, metilações mais intensas no gene mGluR5 agiram como um freio em um receptor cerebral útil e foram acompanhadas por hormônios do estresse hiperativos, inflamação persistente e maior tensão celular. Esses achados sugerem que marcas epigenéticas semelhantes em humanos podem, um dia, ajudar a identificar quem está em maior risco após um trauma, orientando suporte e tratamento precoces. Eles também indicam que terapias voltadas a reajustar suavemente esses interruptores moleculares — seja por fármacos, mudanças no estilo de vida ou futuras ferramentas epigenéticas — podem, no futuro, ajudar a deslocar o equilíbrio da susceptibilidade para a resiliência.
Citação: Ye, M., Lee, Hj. & Shim, I. Epigenetic regulation of the glucocorticoid receptor gene through methylation is linked to post-traumatic stress disorder. Sci Rep 16, 10635 (2026). https://doi.org/10.1038/s41598-026-43615-4
Palavras-chave: transtorno de estresse pós‑traumático, epigenética, metilação do DNA, resiliência ao estresse, hipocampo