Clear Sky Science · zh
肠道微生物群失衡和代谢异常促进特发性肺纤维化中的氧化应激和纤维化
为什么你的肠道可能与肺有关
特发性肺纤维化(IPF)是一种无情的肺部疾病,会疤痕化脆弱的肺泡,使每一次呼吸都变得更困难。长期以来,医生主要关注肺本身,但这项研究提出了一个令人意想不到的问题:我们肠道中的微生物和化学物质是否可能在悄然推动这种疤痕化进程?通过将患者样本与动物实验相结合,研究人员追踪了一条从肠道失衡到血液化学压力,最终导致肺部僵硬受损的事件链。
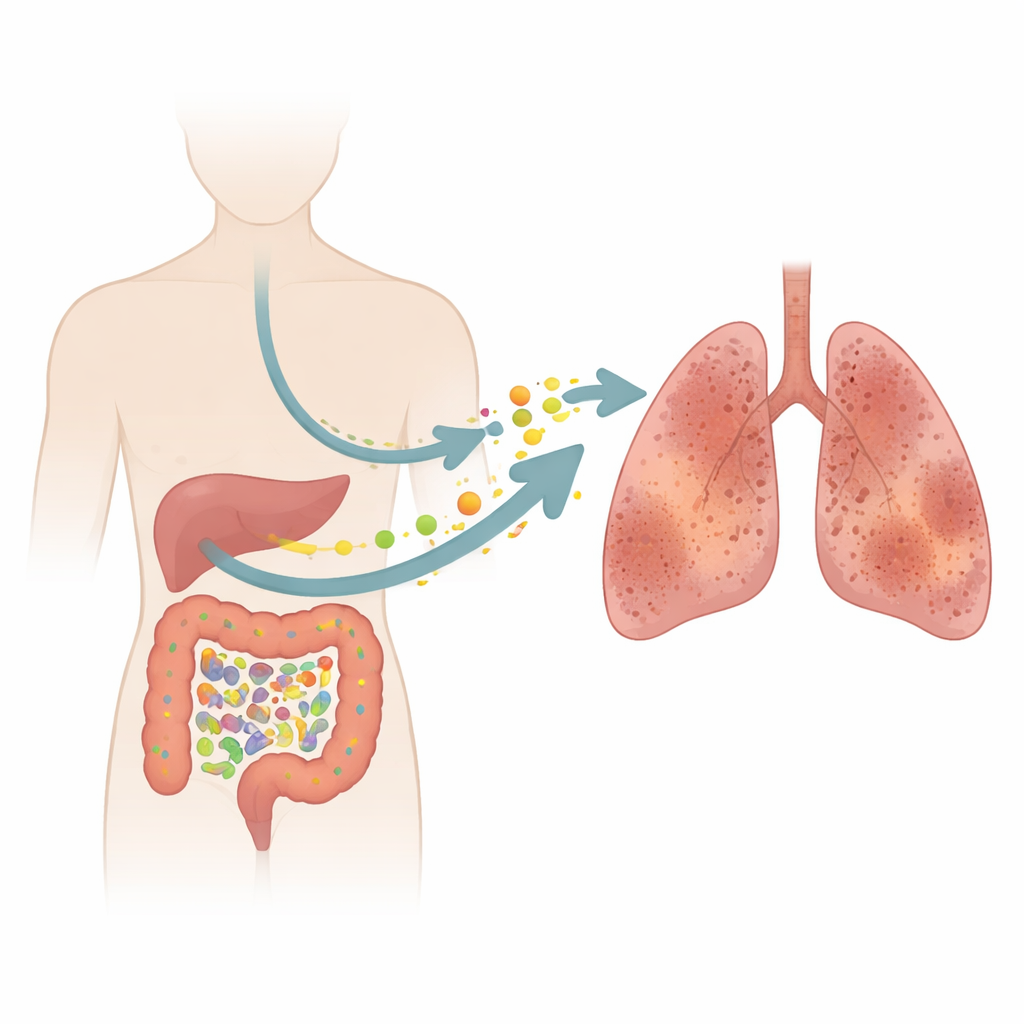
一种悄无声息夺取呼吸的疾病
IPF主要影响老年人,并逐步剥夺他们的肺功能。在这项研究中,17名IPF患者与17名年龄和性别相近的健康对照进行了比较。标准肺功能测试显示,IPF患者的肺容量明显下降,更显著的是他们从空气向血液输送氧气的能力严重受损。这些测量反映了肺泡壁增厚和瘢痕化,空气被困住而不能自由流动。即便有现代影像和检测方法,IPF仍然难以早期诊断,现有药物只能延缓而不能阻止疾病进展,这凸显了在肺外寻找新线索的必要性。
肠道群落及其化学足迹
研究组接着把目光转向肠道。参与者提供了粪便样本,以便研究人员记录其肠道微生物及这些微生物与机体产生的数千种小分子物质。总体来看,肠道群落的整体结构在患者与健康志愿者之间并没有出现极端差异。然而,更细致的分析显示某些细菌群体,尤其是拟杆菌属(Ruminococcus)家族中的一些群体以及一种名为Ruminococcus torques的物种,在IPF患者中更为丰富。与此同时,粪便的化学“指纹”明显改变,这表明即便是关键微生物的温和变化也能对肠道代谢环境产生巨大影响。
一种缺失的保护性分子与上升的化学压力
在众多改变的化学物质中,有一种特别突出:一种由色氨酸和甘氨酸组成的小二肽——色氨酸–甘氨酸(Trp‑Gly)。该分子在IPF患者中的水平显著降低,且与Ruminococcus的过度丰富密切相关。血液检测为谜题补上了另一块拼图。IPF患者的诱导型一氧化氮合酶(iNOS)水平更高,这是氧化应激的一个标志——本质上是组织的化学磨损。他们的血液中整体色氨酸和甘氨酸含量减少,但犬尿氨酸(kynurenine)——色氨酸的分解产物,与炎症和氧化损伤相关——含量增加。综合这些发现表明,失衡的肠道群落可能消耗或改变色氨酸和甘氨酸的代谢,耗竭像Trp‑Gly这样的潜在保护性分子,同时促进产生有害氧化应激的通路。
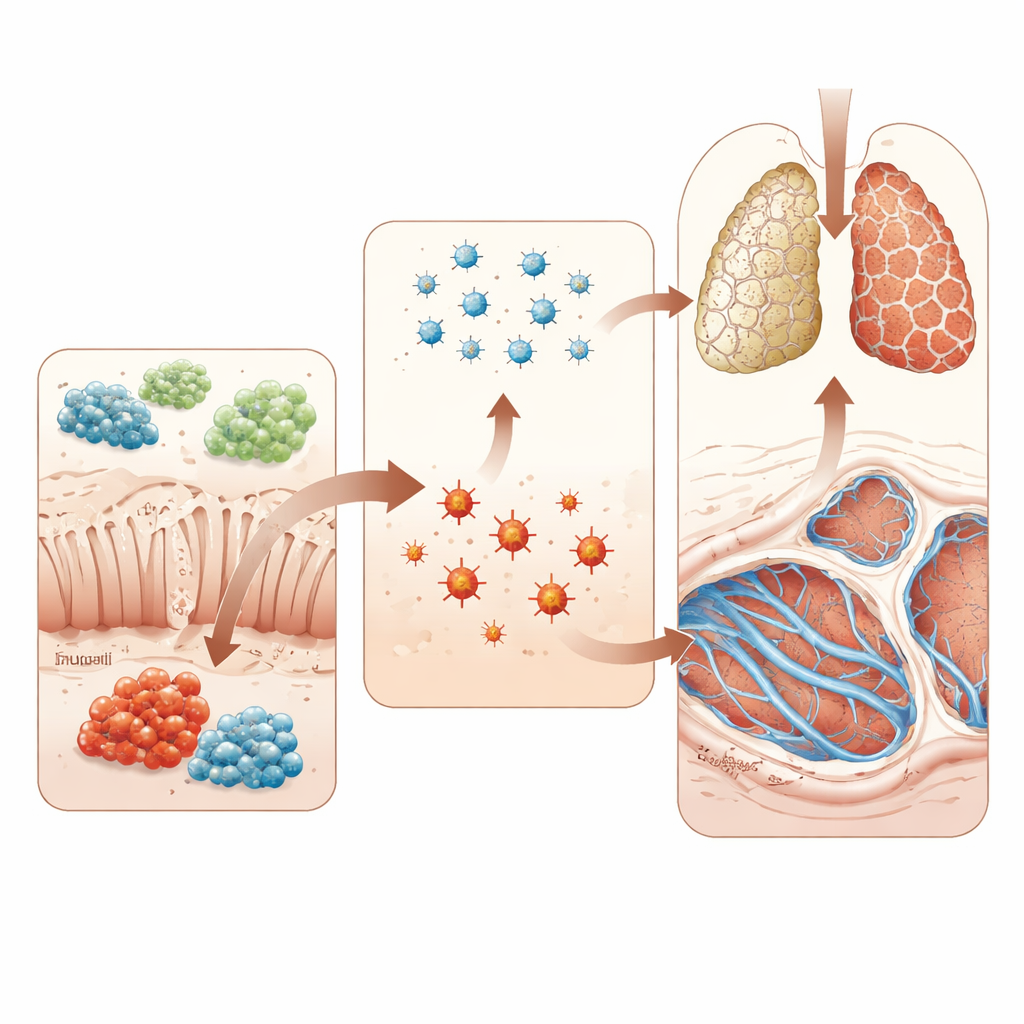
在动物模型中检验因果
为超越相关性,研究人员使用了由药物博来霉素(bleomycin)诱发的标准大鼠肺纤维化模型。部分动物口服补充Trp‑Gly,另一些则给予活的R. torques细菌。补充Trp‑Gly可降低血液中的氧化应激标志物,降低相对于体重的肺重量,并减轻在显微镜下观察到的厚实胶原带和结构畸变。它还抑制了一个关键纤维化通路——TGF‑β/Smad3的活性。相反,给予R. torques的大鼠肺纤维化更严重,氧化应激更高,同样的促纤维化信号通路激活更强。这些实验支持了这样的观点:某些肠道细菌可以推动肺向纤维化方向发展,而特定的肠源分子则可以将其拉回。
这对未来护理意味着什么
通俗地说,这项工作提出了一条连锁反应:肠道微生物的不健康转变,尤其是Ruminococcus及R. torques的增多,扰乱了像Trp‑Gly这样的保护性小分子的产生,反过来提升了血液中的化学压力,并在肺中开启了瘢痕化程序。尽管这项研究仍处于早期,且参与的志愿者和动物数量有限,但它指向了一种新的IPF思路:不仅将其视为肺部疾病,而应视为肠–肺轴失衡的最终结果。如果未来研究证实这些联系,医生或许可以通过肠道或血液标志物更早地诊断风险,并不仅用针对肺的药物治疗IPF,还可能采用定制饮食、微生物疗法或设计型代谢物来恢复这种脆弱的生化平衡。
引用: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
关键词: 特发性肺纤维化, 肠道微生物群, 氧化应激, 色氨酸代谢, 纤维化