Clear Sky Science · de
Dysbiose der Darmmikrobiota und stoffwechselbedingte Auffälligkeiten fördern oxidativen Stress und Fibrose bei idiopathischer pulmonaler Fibrose
Warum Ihr Darm für Ihre Lungen wichtig sein könnte
Die idiopathische pulmonale Fibrose (IPF) ist eine unerbittliche Lungenerkrankung, die die feinen Lungenbläschen vernarbt und jeden Atemzug erschwert. Ärztinnen und Ärzte haben lange die Lungen selbst in den Mittelpunkt gestellt, doch diese Studie stellt eine überraschende Frage: Könnten Mikroben und Chemikalien in unserem Darm stillschweigend das Fortschreiten dieser Vernarbung fördern? Durch die Kombination von Proben von Patientinnen und Patienten mit Tierversuchen verfolgen die Forschenden eine Kette von Ereignissen von einem Ungleichgewicht im Darm über chemischen Stress im Blut bis hin zu steifen, geschädigten Lungen.
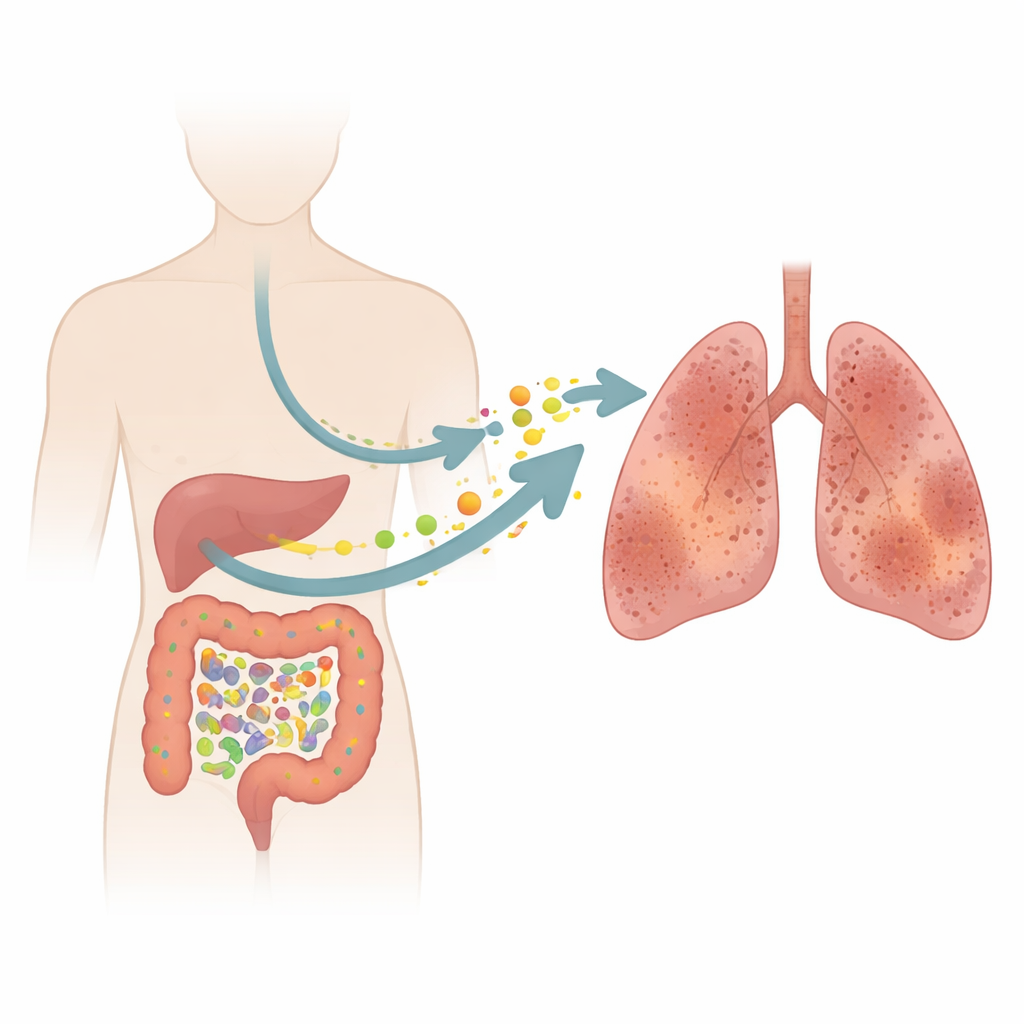
Eine stille Krankheit, die die Atmung stiehlt
IPF betrifft vor allem ältere Erwachsene und raubt ihnen nach und nach die Lungenkapazität. In dieser Studie wurden 17 Menschen mit IPF mit 17 gesunden, alters‑ und geschlechtsangepassten Kontrollpersonen verglichen. Standardisierte Lungenfunktionstests zeigten, dass Menschen mit IPF deutlich reduzierte Lungenvolumina hatten und noch ausgeprägter eine verminderte Fähigkeit, Sauerstoff aus der Luft ins Blut zu transportieren. Diese Messwerte spiegeln verdickte, vernarbte Wände in den Lungenbläschen wider, die Luft einfangen, statt sie frei zirkulieren zu lassen. Trotz moderner Bildgebung und Untersuchungen ist die IPF nach wie vor schwer früh zu diagnostizieren, und die derzeitigen Medikamente verlangsamen die Erkrankung nur, anstatt sie zu stoppen — ein Hinweis darauf, dass es sich lohnt, über die Lungen hinaus nach neuen Hinweisen zu suchen.
Die Darmgemeinschaft und ihre chemische Spur
Als Nächstes wandte sich das Team dem Darm zu. Die Teilnehmenden lieferten Stuhlproben, damit die Forschenden ihre intestinalen Mikroben und die tausenden kleinen Moleküle katalogisieren konnten, die diese Mikroben und der Körper produzieren. Insgesamt wirkte die grobe Struktur der Darmgemeinschaft zwischen Patientinnen und Patienten und gesunden Freiwilligen nicht radikal unterschiedlich. Eine detailliertere Analyse zeigte jedoch, dass bestimmte Bakteriengruppen, insbesondere Angehörige der Familie Ruminococcus und eine Art namens Ruminococcus torques, bei Menschen mit IPF häufiger vorkamen. Gleichzeitig war der chemische „Fingerabdruck“ des Stuhls deutlich verändert, was zeigt, dass selbst moderate Verschiebungen in Schlüsselmikroben überproportionale Auswirkungen auf das metabolische Umfeld des Darms haben können.
Ein fehlendes schützendes Molekül und zunehmender chemischer Stress
Unter den vielen veränderten Chemikalien fiel eines besonders auf: ein kleines Dipeptid namens Tryptophan‑Glycin (Trp‑Gly), das aus den Aminosäuren Tryptophan und Glycin gebildet wird. Die Spiegel dieses Moleküls waren bei IPF‑Patientinnen und -Patienten stark reduziert und eng mit der Überhäufigkeit von Ruminococcus verknüpft. Blutuntersuchungen lieferten ein weiteres Puzzlestück. Menschen mit IPF hatten höhere Werte der induzierbaren Stickstoffmonoxid‑Synthase (iNOS), einen Marker für oxidativen Stress — im Grunde chemischen Verschleiß des Gewebes. In ihrem Blut fanden sich insgesamt weniger Tryptophan und Glycin, aber mehr Kynurenin, ein Abbauprodukt von Tryptophan, das mit Entzündung und oxidativen Schäden assoziiert ist. Zusammengenommen deuten diese Befunde darauf hin, dass eine unausgewogene Darmgemeinschaft Tryptophan und Glycin verbrauchen oder umleiten könnte, schützend wirkende Moleküle wie Trp‑Gly dezimiert und gleichzeitig Stoffwechselwege begünstigt, die schädlichen oxidativen Stress erzeugen.
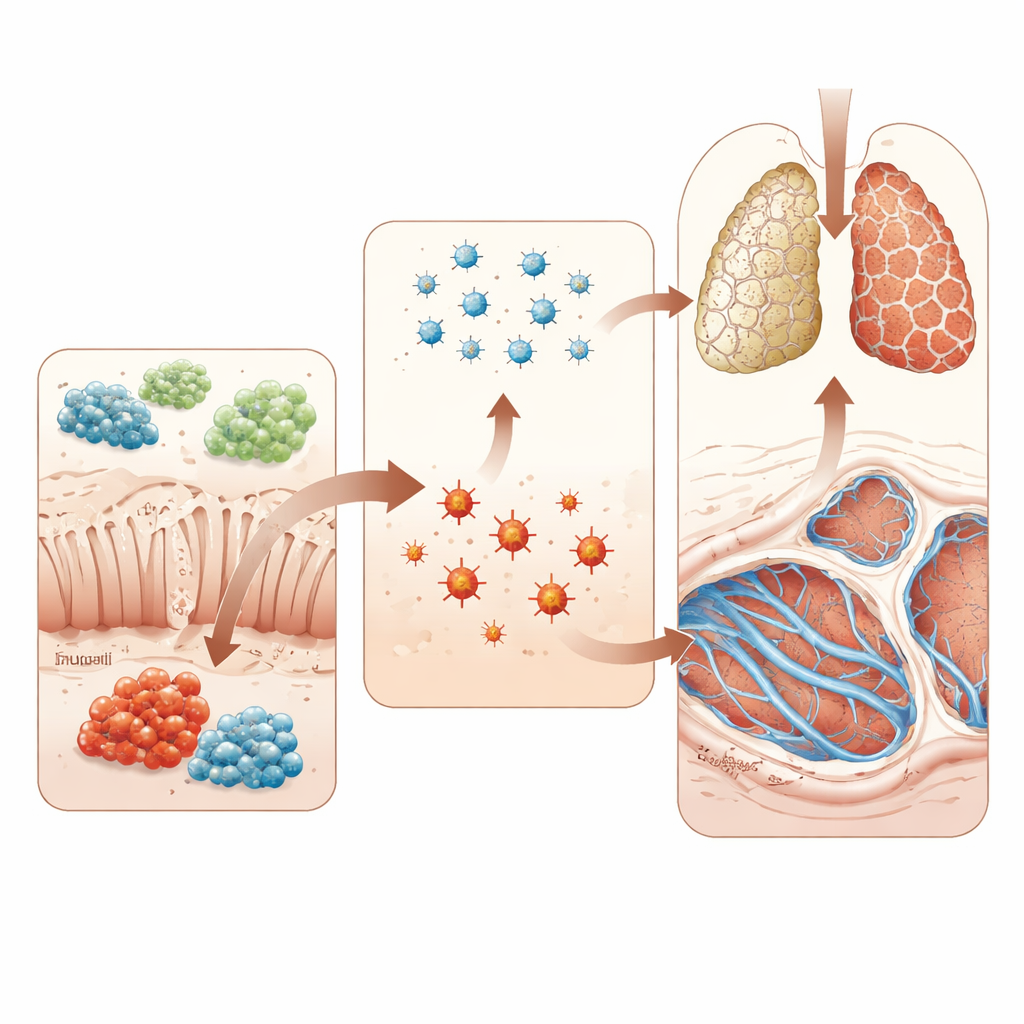
Ursache und Wirkung in Tiermodellen testen
Um über Korrelationen hinauszugehen, verwendeten die Forschenden ein standardisiertes Rattenmodell der Lungenvernarbung, ausgelöst durch das Medikament Bleomycin. Einige Tiere erhielten Trp‑Gly oral, andere wurden mit lebenden R. torques‑Bakterien besiedelt. Die Supplementierung mit Trp‑Gly senkte Marker für oxidativen Stress im Blut, verringerte das Lungengewicht relativ zur Körpergröße und minderte die dicken Kollagenbänder und die verzerrte Architektur, wie sie mikroskopisch zu sehen sind. Außerdem dämpfte sie die Aktivität eines zentralen Vernarbungswegs, bekannt als TGF‑β/Smad3. Im scharfen Gegensatz dazu zeigten Ratten, die R. torques erhielten, stärkere Lungenvernarbung, höheren oxidativen Stress und eine stärkere Aktivierung desselben fibrotischen Signalwegs. Diese Experimente stützen die Idee, dass bestimmte Darmbakterien die Lungen in Richtung Fibrose treiben können, während spezifische vom Darm stammende Moleküle dies rückgängig machen können.
Was das für die zukünftige Versorgung bedeutet
Alltäglich formuliert schlägt diese Arbeit eine Kettenreaktion vor: Eine ungünstige Verschiebung der Darmmikrobiota, insbesondere die Ausweitung von Ruminococcus und R. torques, stört die Produktion kleiner schützender Moleküle wie Trp‑Gly, was wiederum den chemischen Stress im Blut erhöht und Vernarbungsprogramme in der Lunge aktiviert. Zwar ist die Studie noch früh und umfasste nur eine begrenzte Zahl von Freiwilligen und Tieren, doch sie weist auf eine neue Denkweise zur IPF hin: nicht nur als Erkrankung der Lunge, sondern als Endpunkt einer fehlgesteuerten Darm‑Lungen‑Achse. Bestätigen künftige Forschungen diese Zusammenhänge, könnten Ärztinnen und Ärzte eines Tages Risiken früher diagnostizieren — mithilfe von Darm‑ oder Blutmarkern — und IPF nicht nur mit lungenspezifischen Medikamenten, sondern auch durch maßgeschneiderte Ernährung, mikrobielle Therapien oder gezielte Metaboliten behandeln, die dieses fragile biochemische Gleichgewicht wiederherstellen.
Zitation: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Schlüsselwörter: idiopathische pulmonale Fibrose, Darmmikrobiota, oxidativer Stress, Tryptophan‑Stoffwechsel, Fibrose