Clear Sky Science · ja
腸内細菌叢の不均衡と代謝異常は特発性肺線維症における酸化ストレスと線維化を促進する
なぜ腸が肺に影響する可能性があるのか
特発性肺線維症(IPF)は、繊細な肺胞を瘢痕化させ、呼吸を困難にする容赦ない肺疾患です。これまで医師は主に肺そのものに注目してきましたが、本研究は驚くべき疑問を投げかけます:腸内の微生物や化学物質が、この瘢痕化プロセスの一因となっている可能性はあるのか。患者試料と動物実験を組み合わせることで、研究者たちは腸の不均衡から血中の化学的ストレス、そして最終的には硬く損なわれた肺へと至る一連の流れをたどりました。
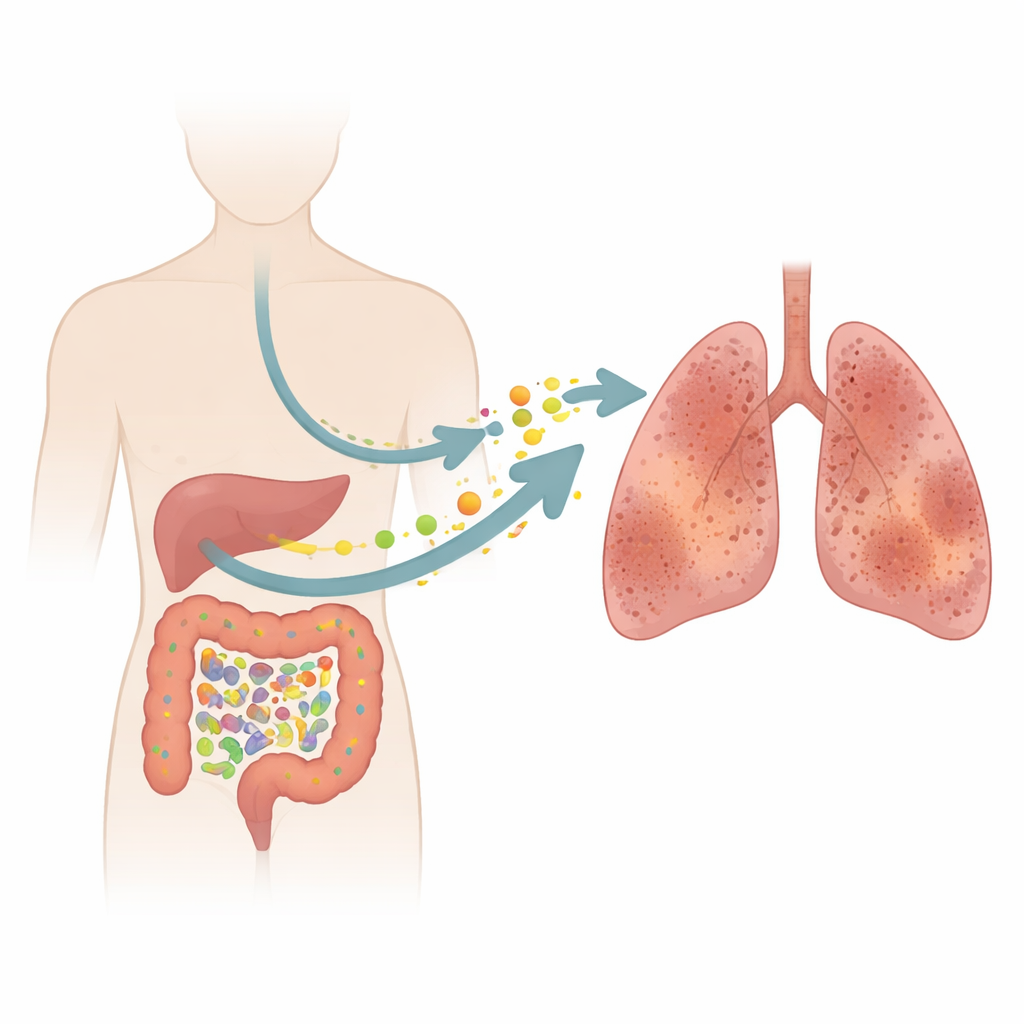
呼吸を奪う静かな病
IPFは主に高齢者に発症し、徐々に肺活量を奪います。本研究では、IPF患者17名と年齢・性別が類似する健康な対照17名を比較しました。標準的な呼吸機能検査では、IPF患者は肺容積が著しく低下していることに加え、特に空気中の酸素を血中に移す能力が大幅に低下していました。これらの測定値は、肺胞の壁が肥厚して瘢痕化し、空気が自由に流れずに閉じ込められていることを反映しています。現代の画像検査や検査にもかかわらず、IPFは早期診断が依然難しく、現行の薬は病気を止めるのではなく遅らせるにとどまるため、肺以外の新たな手がかりを探る必要性が示されています。
腸内コミュニティとその化学的足跡
研究チームは次に腸に注目しました。参加者から便検体を提供してもらい、腸内微生物とそれらの微生物や体が産生する数千の低分子化合物をカタログ化しました。全体としては、腸内コミュニティの大まかな構造は患者と健康対照で劇的に異なるようには見えませんでした。しかし詳細解析では、特にルミノコッカス(Ruminococcus)属、そしてRuminococcus torquesという種がIPF患者でより多く検出されることが明らかになりました。同時に、便の化学的「フィンガープリント」は明確に変化しており、主要な微生物がわずかに変動するだけでも腸の代謝環境に大きな影響を及ぼし得ることを示しています。
失われた保護分子と高まる化学的ストレス
多くの変動した化合物の中で、際立ったものがありました:トリプトファンとグリシンというアミノ酸から形成される小さなジペプチド、トリプトファン–グリシン(Trp‑Gly)。この分子のレベルはIPF患者で著しく低下しており、Ruminococcusの過剰存在と強く結びついていました。血液検査はさらに謎の一端を示しました。IPF患者は誘導型一酸化窒素合成酵素(iNOS)のレベルが高く、これは酸化ストレス、すなわち組織に対する化学的な摩耗の指標です。血中では総じてトリプトファンとグリシンが減少している一方、炎症や酸化的損傷と関連するトリプトファンの分解産物であるキヌレニンは増えていました。これらを総合すると、腸内コミュニティの不均衡がトリプトファンやグリシンを消費または経路転換し、Trp‑Glyのような潜在的に保護的な分子を枯渇させる一方で、有害な酸化ストレスを生む経路を助長していることが示唆されます。
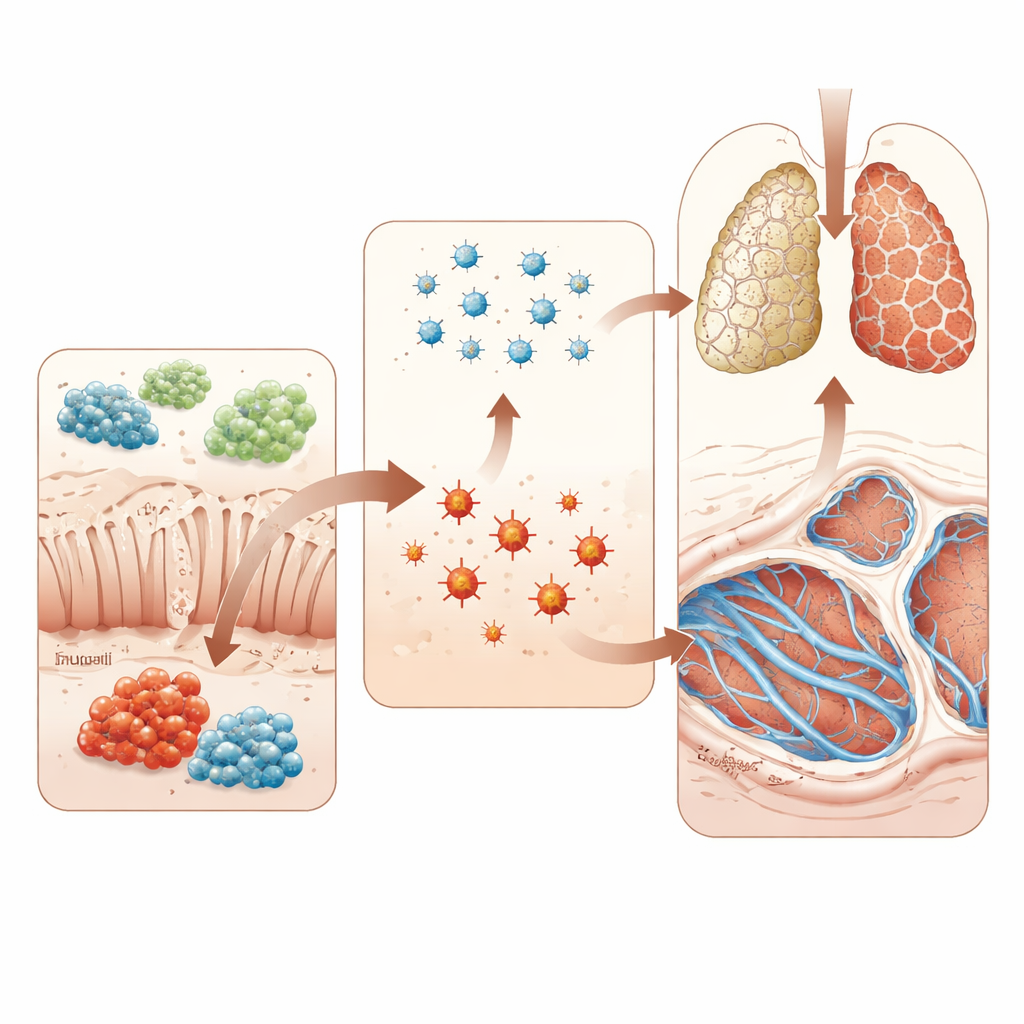
動物モデルでの因果関係の検証
相関関係を超えるために、研究者らはブレオマイシンという薬剤で誘発される標準的なラットの肺線維化モデルを用いました。一部の動物には経口でTrp‑Glyを投与し、別の群には生きたR. torques細菌を与えました。Trp‑Glyの補給は血中の酸化ストレスマーカーを低下させ、体重比での肺重量を下げ、顕微鏡で見られる厚いコラーゲン帯や乱れた構造を軽減しました。また、TGF‑β/Smad3として知られる主要な線維化経路の活動も抑制しました。対照的に、R. torquesを投与されたラットは肺の瘢痕化が悪化し、酸化ストレスが増加し、同じ線維化シグナル経路の活性化が強まりました。これらの実験は、特定の腸内細菌が肺を線維化へと押し進め得る一方で、特定の腸由来分子がそれを抑える可能性がある、という考えを支持します。
将来の医療にとっての意味
平易に言えば、本研究は次のような連鎖反応を提示します:腸内微生物の不健康な変化、特にRuminococcusおよびR. torquesの増殖が、Trp‑Glyのような小さな保護分子の産生を乱し、それが血流中の化学的ストレスを高め、肺の瘢痕化プログラムをスイッチオンしてしまうというものです。本研究はまだ初期段階であり、被験者数や動物数は限られますが、IPFを単なる肺の病気ではなく、腸–肺軸の崩壊の帰結と考える新しい視点を示しています。今後の研究でこれらの関連が確認されれば、医師はいつか腸や血中のマーカーを用いてリスクを早期に診断し、肺を標的とした薬だけでなく、食事療法、微生物治療、あるいはこの不安定な生化学的バランスを回復する設計分子といった治療法を組み合わせてIPFを治療する可能性が開けるでしょう。
引用: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
キーワード: 特発性肺線維症, 腸内細菌叢, 酸化ストレス, トリプトファン代謝, 線維化