Clear Sky Science · pt
Desequilíbrio da microbiota intestinal e anomalias metabólicas promovem estresse oxidativo e fibrose na fibrose pulmonar idiopática
Por que seu intestino pode importar para seus pulmões
A fibrose pulmonar idiopática (FPI) é uma doença pulmonar implacável que cicatriza os delicados alvéolos, tornando cada respiração mais difícil. Os médicos há muito concentram-se nos próprios pulmões, mas este estudo faz uma pergunta surpreendente: micróbios e substâncias químicas em nossos intestinos poderiam, silenciosamente, contribuir para esse processo de cicatrização? Ao combinar amostras de pacientes com experimentos em animais, os pesquisadores rastreiam uma cadeia de eventos desde o desequilíbrio intestinal até o estresse químico no sangue e, por fim, pulmões rígidos e danificados.
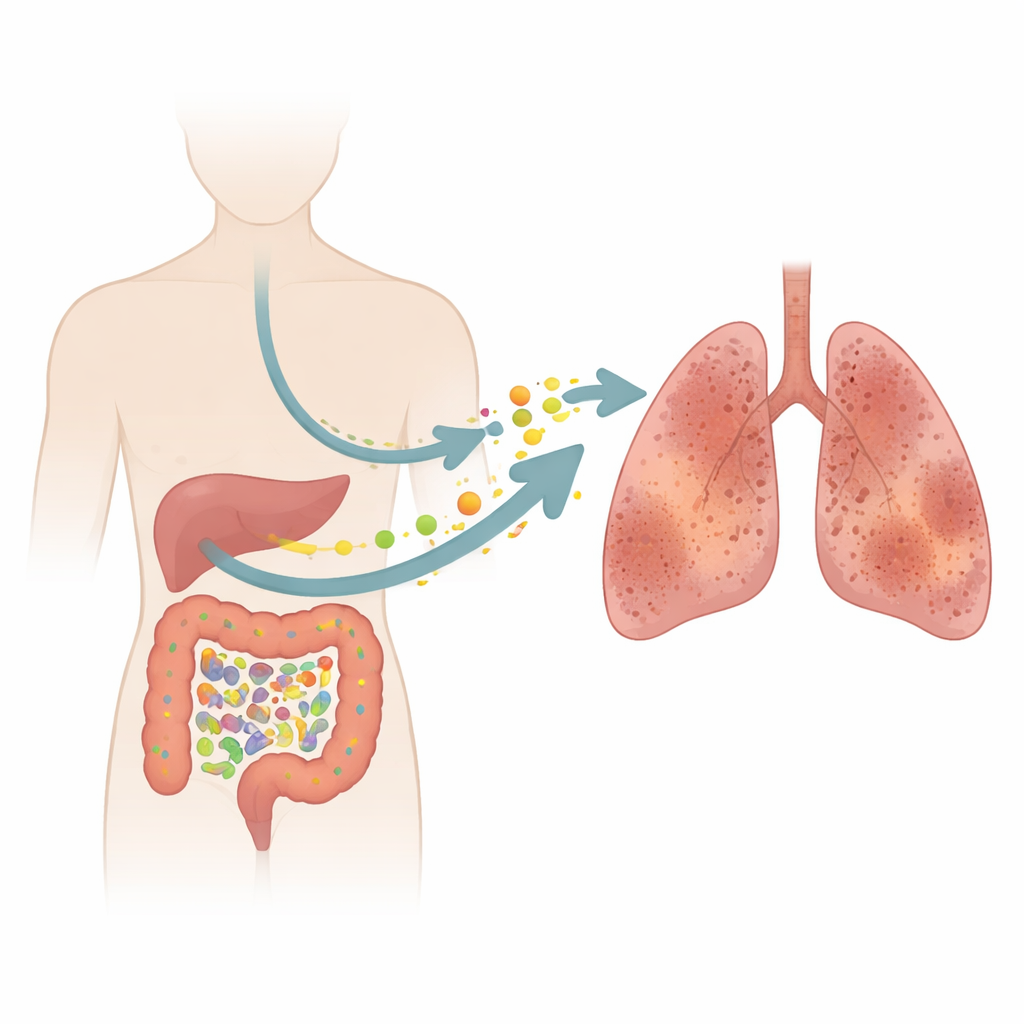
Uma doença silenciosa que rouba o fôlego
A FPI afeta principalmente adultos mais velhos e gradualmente lhes rouba a capacidade pulmonar. Neste estudo, 17 pessoas com FPI foram comparadas a 17 pares saudáveis de idade e sexo semelhantes. Testes respiratórios padrão mostraram que pessoas com FPI apresentavam volumes pulmonares marcadamente reduzidos e, de forma ainda mais dramática, uma capacidade pior de transferir oxigênio do ar para o sangue. Essas medidas refletem paredes espessadas e cicatrizadas nos alvéolos, que aprisionam ar em vez de permitir seu fluxo livre. Apesar de exames e testes modernos, a FPI ainda é difícil de diagnosticar precocemente e os medicamentos atuais apenas retardam, em vez de interromper, a doença, destacando a necessidade de buscar além dos pulmões por novas pistas.
A comunidade intestinal e sua assinatura química
A equipe, em seguida, voltou-se para o intestino. Os participantes forneceram amostras de fezes para que os pesquisadores pudessem catalogar seus micróbios intestinais e as milhares de pequenas moléculas que esses micróbios e o corpo produzem. No geral, a estrutura ampla da comunidade intestinal não parecia radicalmente diferente entre pacientes e voluntários saudáveis. No entanto, análises mais detalhadas revelaram que certos grupos bacterianos, particularmente os da família Ruminococcus e uma espécie chamada Ruminococcus torques, eram mais abundantes em pessoas com FPI. Ao mesmo tempo, a “impressão digital” química das fezes estava claramente alterada, mostrando que mesmo mudanças modestamente direcionadas em micróbios-chave podem ter efeitos desproporcionais no ambiente metabólico do intestino.
Uma molécula protetora ausente e o aumento do estresse químico
Entre muitas substâncias alteradas, uma sobressaiu: um pequeno dipeptídeo chamado triptofano–glicina (Trp‑Gly), formado pelos aminoácidos triptofano e glicina. Os níveis dessa molécula estavam fortemente reduzidos em pacientes com FPI e intimamente vinculados à superabundância de Ruminococcus. Exames de sangue acrescentaram outra peça ao quebra‑cabeça. Pessoas com FPI apresentavam níveis mais altos de óxido nítrico sintase indutível (iNOS), um marcador de estresse oxidativo—essencialmente desgaste químico nos tecidos. Seu sangue continha menos triptofano e glicina no geral, mas mais quinurenina, um produto de degradação do triptofano associado à inflamação e ao dano oxidativo. Juntos, esses achados sugerem que uma comunidade intestinal desequilibrada pode consumir ou redirecionar triptofano e glicina, esgotando moléculas potencialmente protetoras como Trp‑Gly enquanto alimenta vias que geram estresse oxidativo prejudicial.
Testando causa e efeito em modelos animais
Para ir além da correlação, os pesquisadores usaram um modelo padrão de rato para cicatrização pulmonar desencadeada pela droga bleomicina. Alguns animais receberam Trp‑Gly por via oral, enquanto outros receberam bactérias vivas de R. torques. A suplementação com Trp‑Gly reduziu marcadores de estresse oxidativo no sangue, diminuiu o peso pulmonar relativo ao tamanho corporal e atenuou as densas faixas de colágeno e a arquitetura distorcida observadas ao microscópio. Também reduziu a atividade em uma via chave de fibrose conhecida como TGF‑β/Smad3. Em nítido contraste, ratos tratados com R. torques apresentaram pior cicatrização pulmonar, maior estresse oxidativo e ativação mais forte da mesma via de sinalização fibrótica. Esses experimentos apoiam a ideia de que certas bactérias intestinais podem empurrar os pulmões em direção à fibrose, enquanto moléculas específicas derivadas do intestino podem afastá‑los desse processo.
O que isso significa para os cuidados futuros
Em termos práticos, este trabalho propõe uma reação em cadeia: uma mudança prejudicial nos micróbios intestinais, especialmente a expansão de Ruminococcus e R. torques, interrompe a produção de pequenas moléculas protetoras como Trp‑Gly, o que por sua vez eleva o estresse químico na corrente sanguínea e ativa programas de cicatrização nos pulmões. Embora o estudo ainda seja inicial e tenha envolvido um número modesto de voluntários e animais, ele aponta para uma nova forma de pensar sobre a FPI: não apenas como uma doença dos pulmões, mas como o resultado final de um eixo intestino–pulmão fora de equilíbrio. Se pesquisas futuras confirmarem essas ligações, os médicos poderão um dia diagnosticar o risco mais cedo usando marcadores fecais ou sanguíneos e tratar a FPI não apenas com drogas dirigidas aos pulmões, mas também com dietas personalizadas, terapias microbianas ou metabólitos projetados que restaurem esse frágil equilíbrio bioquímico.
Citação: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Palavras-chave: fibrose pulmonar idiopática, microbiota intestinal, estresse oxidativo, metabolismo do triptofano, fibrose