Clear Sky Science · fr
Dysbiose du microbiote intestinal et anomalies métaboliques favorisent le stress oxydatif et la fibrose dans la fibrose pulmonaire idiopathique
Pourquoi votre intestin pourrait importer pour vos poumons
La fibrose pulmonaire idiopathique (FPI) est une maladie pulmonaire impitoyable qui cicatrise les alvéoles délicates, rendant chaque respiration plus difficile. Les médecins se sont longtemps concentrés sur les poumons eux‑mêmes, mais cette étude pose une question surprenante : des microbes et des composés chimiques de nos intestins pourraient‑ils silencieusement contribuer à ce processus de cicatrisation ? En combinant des échantillons de patients et des expériences animales, les chercheurs retracent une chaîne d’événements partant d’un déséquilibre intestinal jusqu’au stress chimique dans le sang et, finalement, à des poumons raides et endommagés.
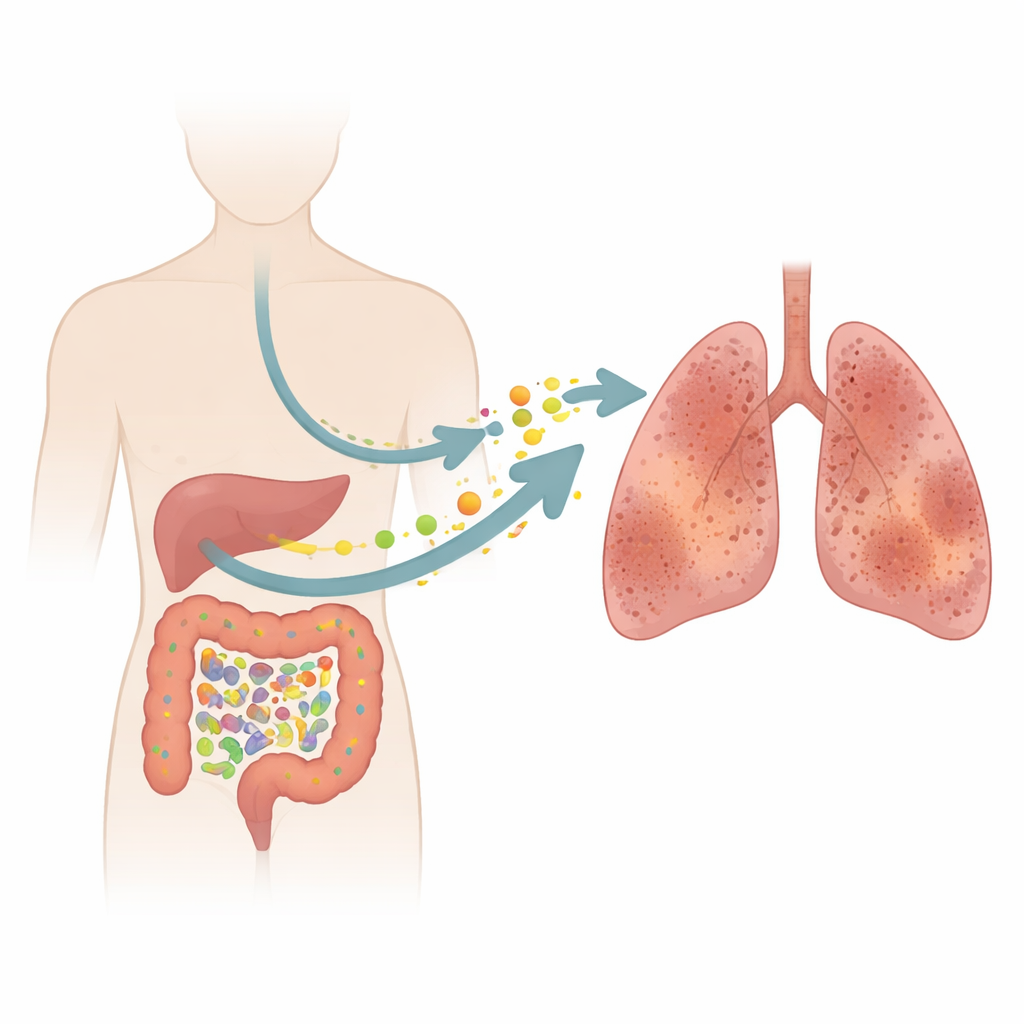
Une maladie silencieuse qui vole le souffle
La FPI touche principalement les personnes âgées et leur fait progressivement perdre de la capacité pulmonaire. Dans cette étude, 17 personnes atteintes de FPI ont été comparées à 17 témoins sains de même âge et sexe. Les tests respiratoires standards ont montré que les personnes atteintes présentaient des volumes pulmonaires nettement réduits et, de manière encore plus marquée, une capacité moindre à transférer l’oxygène de l’air vers le sang. Ces mesures reflètent l’épaississement et la cicatrisation des parois des alvéoles pulmonaires, qui piègent l’air au lieu de le laisser circuler librement. Malgré les scanners et les examens modernes, la FPI reste difficile à diagnostiquer précocement et les traitements actuels ralentissent la maladie sans l’arrêter, soulignant la nécessité d’élargir le champ de recherche au‑delà des poumons pour trouver de nouveaux indices.
La communauté intestinale et son empreinte chimique
L’équipe s’est ensuite tournée vers l’intestin. Les participants ont fourni des échantillons de selles afin que les chercheurs puissent inventorier leurs microbes intestinaux et les milliers de petites molécules produites par ces microbes et par l’organisme. Globalement, la structure générale de la communauté intestinale ne paraissait pas radicalement différente entre les patients et les volontaires sains. Cependant, une analyse plus fine a révélé que certains groupes bactériens, en particulier ceux de la famille des Ruminococcus et une espèce nommée Ruminococcus torques, étaient plus abondants chez les personnes atteintes de FPI. Parallèlement, l’« empreinte » chimique des selles était clairement modifiée, montrant que même des variations modestes de microbes clés peuvent avoir des effets disproportionnés sur l’environnement métabolique de l’intestin.
Une molécule protectrice manquante et un stress chimique croissant
Parmi les nombreux composés modifiés, un a attiré l’attention : un petit dipeptide appelé tryptophane–glycine (Trp‑Gly), formé à partir des acides aminés tryptophane et glycine. Les niveaux de cette molécule étaient fortement réduits chez les patients atteints de FPI et étroitement corrélés à la surabondance de Ruminococcus. Les analyses sanguines ajoutent une autre pièce au puzzle. Les personnes atteintes présentaient des taux plus élevés de synthase inductible de l’oxyde nitrique (iNOS), un marqueur du stress oxydatif — en d’autres termes, une usure chimique des tissus. Leur sang contenait moins de tryptophane et de glycine au total, mais davantage de kynurénine, un produit de dégradation du tryptophane associé à l’inflammation et aux dommages oxydatifs. Ensemble, ces éléments suggèrent qu’une communauté intestinale déséquilibrée peut consommer ou détourner le tryptophane et la glycine, appauvrissant des molécules potentiellement protectrices comme le Trp‑Gly tout en alimentant des voies qui génèrent un stress oxydatif nocif.
Tester la causalité dans des modèles animaux
Pour aller au‑delà de la corrélation, les chercheurs ont utilisé un modèle rat standard de cicatrisation pulmonaire déclenchée par la bléomycine. Certains animaux ont reçu du Trp‑Gly par voie orale, tandis que d’autres ont été inoculés avec la bactérie vivante R. torques. La supplémentation en Trp‑Gly a réduit les marqueurs de stress oxydatif dans le sang, diminué le poids pulmonaire relatif au poids corporel et atténué les bandes épaisses de collagène et l’architecture déformée observées au microscope. Elle a également modéré l’activité d’une voie clé de fibrose connue sous le nom de TGF‑β/Smad3. À l’inverse, les rats ayant reçu R. torques ont présenté une fibrose pulmonaire aggravée, un stress oxydatif plus élevé et une activation plus marquée de la même voie de signalisation fibrotique. Ces expériences soutiennent l’idée que certaines bactéries intestinales peuvent pousser les poumons vers la fibrose, tandis que des molécules spécifiques d’origine intestinale peuvent les en protéger.
Ce que cela signifie pour les soins futurs
Concrètement, ce travail propose une réaction en chaîne : un changement défavorable du microbiote intestinal, en particulier l’expansion des Ruminococcus et de R. torques, perturbe la production de petites molécules protectrices comme le Trp‑Gly, ce qui augmente ensuite le stress chimique dans le sang et active les programmes de cicatrisation dans les poumons. Bien que l’étude soit encore préliminaire et ait impliqué un nombre modeste de volontaires et d’animaux, elle ouvre une nouvelle manière de concevoir la FPI : non seulement comme une maladie des poumons, mais comme le résultat d’un axe intestin–poumon perturbé. Si des recherches futures confirment ces liens, les médecins pourraient un jour diagnostiquer le risque plus tôt à l’aide de marqueurs fécaux ou sanguins et traiter la FPI non seulement par des médicaments ciblant les poumons, mais aussi par des approches alimentaires personnalisées, des thérapies microbiennes ou des métabolites conçus pour rétablir cet équilibre biochimique fragile.
Citation: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Mots-clés: fibrose pulmonaire idiopathique, microbiote intestinal, stress oxydatif, métabolisme du tryptophane, fibrose