Clear Sky Science · tr
Bağırsak mikrobiyota disbiyozisi ve metabolik anormallikler idiyopatik pulmoner fibroziste oksidatif stresi ve fibrozisi teşvik ediyor
Bağırsağınızın Akciğerleriniz İçin Neden Önemli Olabileceği
İdiyopatik pulmoner fibrozis (İPF), hassas hava keseciklerini yara dokusuyla değiştiren ve her nefesi zorlaştıran amansız bir akciğer hastalığıdır. Hekimler uzun süredir doğrudan akciğerlere odaklanıyor, ancak bu çalışma sürpriz bir soruyu gündeme getiriyor: Bağırsaklarımızdaki mikroplar ve kimyasallar bu skarlaşma sürecini sessizce tetikleyebilir mi? Hasta örneklerini hayvan deneyleriyle birleştirerek araştırmacılar, bağırsaktaki dengesizlikten kanda kimyasal strese ve nihayetinde sert, hasarlı akciğerlere uzanan bir olay zincirini izliyorlar.
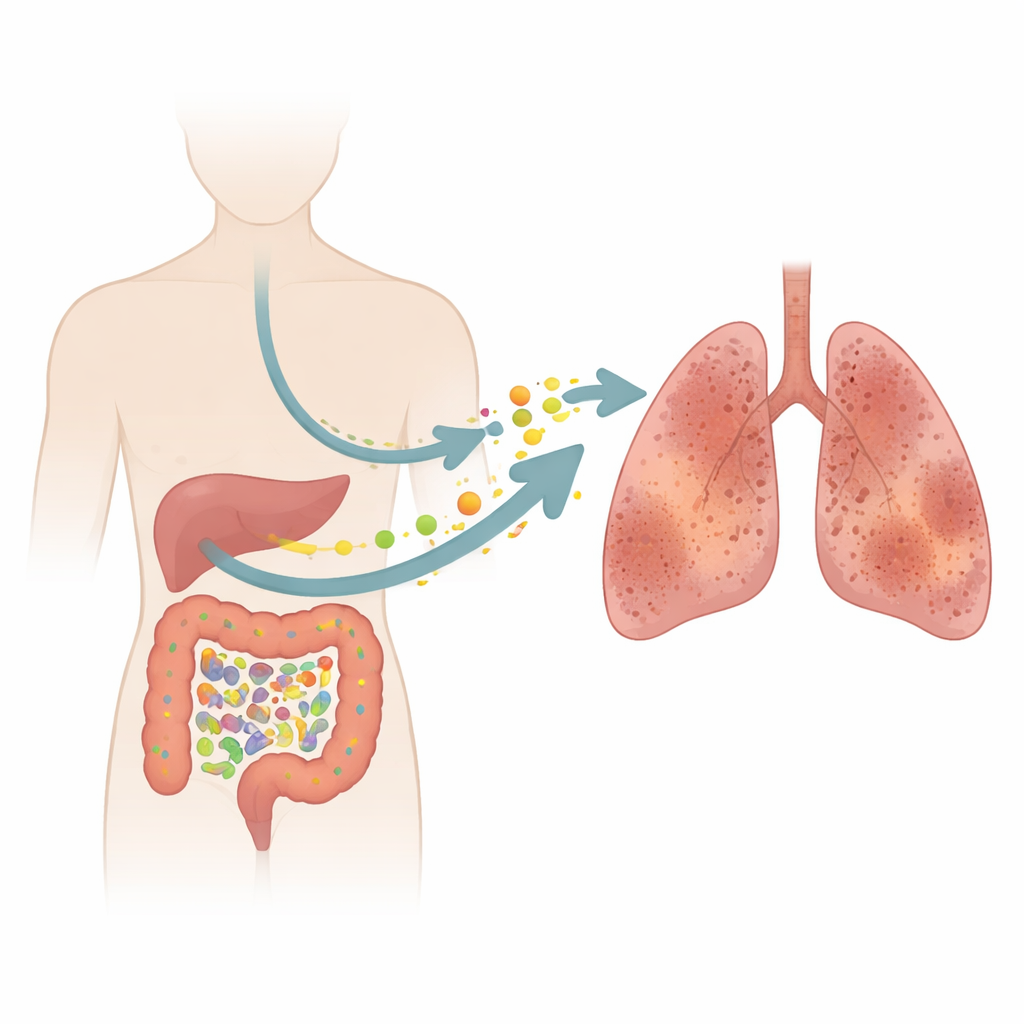
Nefesi Çalan Sessiz Bir Hastalık
İPF ağırlıklı olarak yaşlı yetişkinleri etkiler ve zamanla akciğer kapasitesini yok eder. Bu çalışmada, 17 İPF hastası benzer yaş ve cinsiyetteki 17 sağlıklı kişiyle karşılaştırıldı. Standart solunum testleri, İPF’li kişilerin belirgin şekilde azalmış akciğer hacimlerine ve daha da çarpıcı biçimde havadan kana oksijen geçişinde zayıf bir yeteneğe sahip olduğunu gösterdi. Bu ölçümler, hava keseciklerinin duvarlarının kalınlaşıp skar dokusuyla dolduğunu, havanın serbestçe akmak yerine hapsolduğunu yansıtır. Modern görüntülemelere ve testlere rağmen İPF hâlâ erken dönemde tanı koyması zor bir hastalık ve mevcut ilaçlar hastalığı durdurmak yerine yalnızca yavaşlatıyor; bu da yeni ipuçları için akciğerlerin ötesine bakılması gerektiğini vurguluyor.
Bağırsak Topluluğu ve Kimyasal Ayak İzi
Araştırmacılar sırada bağırsaklara yöneldi. Katılımcılar dışkı örnekleri verdiler; böylece ekip bağırsaktaki mikropları ve bu mikroplar ile vücudun ürettiği binlerce küçük molekülü kataloglayabildi. Genel olarak, bağırsak topluluğunun geniş yapısı hastalar ile sağlıklı gönüllüler arasında köklü şekilde farklı görünmüyordu. Ancak daha ayrıntılı analiz, özellikle Ruminococcus ailesindeki bazı bakteri grupları ve Ruminococcus torques adlı bir türün İPF’li kişilerde daha fazla bulunduğunu ortaya koydu. Aynı zamanda dışkının kimyasal “parmak izi” belirgin şekilde değişmişti; bu da anahtar mikroplardaki görece küçük kaymaların bağırsak metabolik ortamı üzerinde orantısız etkiler yaratabileceğini gösteriyor.
Eksik Bir Koruyucu Molekül ve Artan Kimyasal Stres
Çok sayıda değişen kimyasal arasında öne çıkan bir tanesi vardı: triptofan ve glisinden oluşan küçük bir dipeptid olan triptofan–glisin (Trp‑Gly). Bu molekülün düzeyleri İPF hastalarında güçlü şekilde azalmıştı ve Ruminococcus’un aşırı varlığıyla sıkı bir ilişki gösteriyordu. Kan testleri bulmacaya başka bir parça ekledi. İPF’li kişilerde indüklenebilir nitrik oksit sentaz (iNOS) seviyeleri daha yüksekti; bu, temelde dokular üzerindeki kimyasal aşınma ve yıpranmanın bir işareti olan oksidatif stres göstergesi. Kanlarında genel olarak daha az triptofan ve glisin bulunurken, triptofandan türeyen ve iltihap ile oksidatif hasarla ilişkili bir ürün olan kinurenin düzeyleri daha yüksekti. Bu bulgular birlikte, dengesiz bir bağırsak topluluğunun triptofanu ve glisini tüketebileceğini veya yönlendirebileceğini; Trp‑Gly gibi potansiyel olarak koruyucu molekülleri tüketip zararlı oksidatif stresi üreten yolakları destekleyebileceğini öneriyor.
Hayvan Modellerinde Nedensellik Testi
Korelasyonun ötesine geçmek için araştırmacılar, bleomisin adlı ilaçla tetiklenen standart bir sıçan akciğer skarlaşması modelini kullandılar. Bazı hayvanlara ağız yoluyla Trp‑Gly verildi, diğerlerine ise canlı R. torques bakterileri verildi. Trp‑Gly takviyesi kanda oksidatif stres belirteçlerini azalttı, akciğer ağırlığını vücut ağırlığına göre düşürdü ve mikroskop altında görülen kalın kolajen bantları ile bozulmuş mimariyi hafifletti. Ayrıca TGF‑β/Smad3 olarak bilinen önemli bir skarlaşma yolundaki aktiviteyi de baskıladı. Keskin bir tezat olarak, R. torques verilen sıçanlarda akciğer skarlaşması daha kötü, oksidatif stres daha yüksek ve aynı fibrotik sinyal yolunun aktivasyonu daha güçlüydü. Bu deneyler belli bağırsak bakterilerinin akciğerleri fibrozise itebileceği, oysa belirli bağırsak kaynaklı moleküllerin akciğerleri geri çekebileceği fikrini destekliyor.
Gelecekteki Bakım İçin Bunun Anlamı
Gündelik ifadeyle, bu çalışma şu zincirleme reaksiyonu öneriyor: Bağırsak mikroplarında sağlıksız bir kayma, özellikle Ruminococcus ve R. torques’in genişlemesi, Trp‑Gly gibi küçük koruyucu moleküllerin üretimini bozuyor; bu da kana kimyasal stresin yükselmesine ve akciğerlerde skarlaşma programlarının devreye girmesine yol açıyor. Çalışma hâlâ erken aşamada olup gönüllü ve hayvan sayısı sınırlı olsa da, İPF’yi yalnızca akciğer hastalığı olarak görmek yerine bağırsak–akciğer ekseninin bozulmasının nihai sonucu olarak düşünmenin yeni bir yolunu işaret ediyor. Gelecek araştırmalar bu bağlantıları doğruladıktan sonra hekimler bir gün bağırsak ya da kan belirteçleriyle riski daha erken tanıyabilir ve İPF’yi yalnızca akciğer hedefli ilaçlarla değil, aynı zamanda kişiye özel diyet, mikrobiyal tedaviler veya bu hassas biyokimyasal dengeyi geri getiren tasarlanmış metabolitlerle tedavi edebilirler.
Atıf: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Anahtar kelimeler: idiyopatik pulmoner fibrozis, bağırsak mikrobiyota, oksidatif stres, triptofan metabolizması, fibrozis