Clear Sky Science · sv
Tarmmikrobiotas dysbios och metabola avvikelser främjar oxidativ stress och fibros vid idiopatisk lungsjukdom
Varför din tarm kan ha betydelse för dina lungor
Idiopatisk lungsjukdom (IPF) är en obeveklig lungsjukdom som ärrar de känsliga luftblåsorna och gör varje andetag tyngre. Läkare har länge fokuserat på själva lungorna, men denna studie ställer en överraskande fråga: kan mikrober och kemikalier i våra tarmar i det tysta bidra till denna ärrbildningsprocess? Genom att kombinera patientprover med djurexperiment spårar forskarna en händelsekedja från tarmobalans till kemisk stress i blodet och, i slutändan, till styva, skadade lungor.
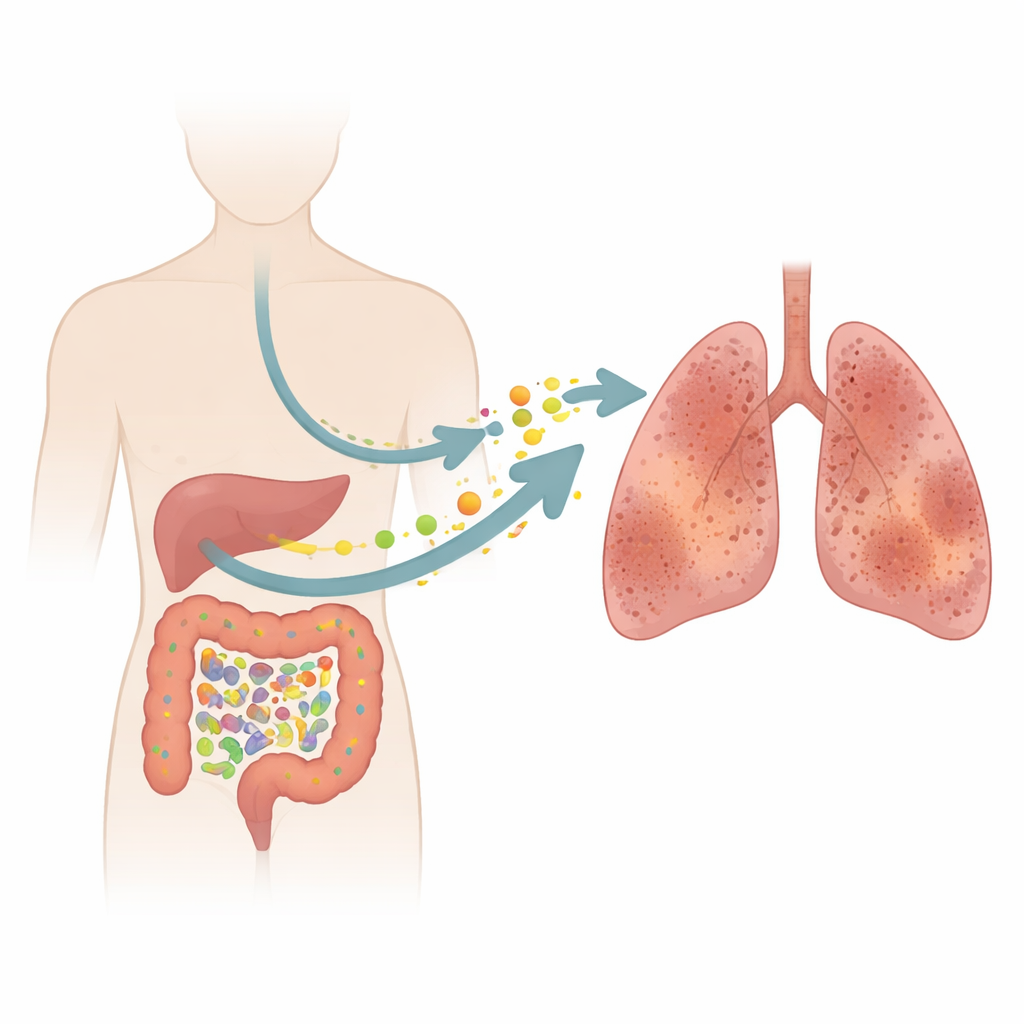
En tyst sjukdom som stjäl andningen
IPF drabbar främst äldre vuxna och berövar dem gradvis lungkapacitet. I denna studie jämfördes 17 personer med IPF med 17 friska jämnåriga med samma könsfördelning. Standardiserade andningstester visade att personer med IPF hade markant reducerade lungvolymer och, ännu tydligare, en försämrad förmåga att överföra syre från luften till blodet. Dessa mått speglar förtjockade, ärrade väggar i lungans luftblåsor som fångar luft i stället för att låta den flöda fritt. Trots moderna avbildningar och tester är IPF fortfarande svår att diagnostisera tidigt och dagens läkemedel bromsar bara sjukdomen i stället för att stoppa den, vilket understryker behovet av att söka ledtrådar bortom lungorna.
Tarmens gemenskap och dess kemiska avtryck
Teamet vände sig sedan mot tarmen. Deltagarna lämnade avföringsprover så att forskarna kunde katalogisera deras tarmmikrober och de tusentals små molekyler som dessa mikrober och kroppen producerar. Övergripande såg tarmens breda gemenskapsstruktur inte radikalt annorlunda ut mellan patienter och friska volontärer. Men mer detaljerad analys avslöjade att vissa bakteriegrupper, särskilt de i släktet Ruminococcus och en art kallad Ruminococcus torques, var mer rikliga hos personer med IPF. Samtidigt var avföringens kemiska ”fingeravtryck” tydligt förändrat, vilket visar att även måttliga skift i nyckelmikrober kan få oproportionerligt stora effekter på tarmens metabola miljö.
En saknad skyddande molekyl och ökande kemisk stress
Bland många förskjutna kemikalier stack en ut: en liten dipeptid kallad tryptofan–glycin (Trp‑Gly), bildad av aminosyrorna tryptofan och glycin. Nivåerna av denna molekyl var kraftigt reducerade hos IPF‑patienter och starkt kopplade till överflödet av Ruminococcus. Blodprover lade till en annan pusselbit. Personer med IPF hade högre nivåer av inducerbar kväveoxidsyntas (iNOS), en markör för oxidativ stress—i praktiken kemiskt slitage på vävnader. Deras blod innehöll mindre tryptofan och glycin totalt sett, men mer kynurenin, en nedbrytningsprodukt av tryptofan som förknippas med inflammation och oxidativ skada. Tillsammans tyder dessa fynd på att en obalanserad tarmgemenskap kan konsumera eller omdirigera tryptofan och glycin, tömma potentiellt skyddande molekyler som Trp‑Gly samtidigt som den driver vägar som genererar skadlig oxidativ stress.
Test av orsak och verkan i djurmodeller
För att gå bortom korrelation använde forskarna en standard råttmodell för lungsärrbildning utlösta av läkemedlet bleomycin. Vissa djur fick Trp‑Gly oralt, medan andra gavs levande R. torques‑bakterier. Tillskott av Trp‑Gly minskade markörer för oxidativ stress i blodet, sänkte lungvikten i förhållande till kroppsstorlek och reducerade de tjocka kollagenbanden och den förvrängda arkitektur som ses i mikroskopet. Det dämpade också aktiviteten i en viktig ärrbildningsväg känd som TGF‑β/Smad3. I skarp kontrast hade råttor som fått R. torques sämre lungsärrbildning, högre oxidativ stress och starkare aktivering av samma fibrotiska signalväg. Dessa experiment stödjer idén att vissa tarmbakterier kan driva lungorna mot fibros, medan specifika tarm‑härledda molekyler kan dra dem tillbaka.
Vad detta betyder för framtida vård
I vardagliga termer föreslår detta arbete en kedjereaktion: en ohälsosam förskjutning i tarmmikrober, särskilt expansion av Ruminococcus och R. torques, stör produktionen av små skyddande molekyler som Trp‑Gly, vilket i sin tur ökar kemisk stress i blodomloppet och aktiverar ärrprogram i lungorna. Studin är fortfarande tidig och omfattade ett begränsat antal frivilliga och djur, men den pekar på ett nytt sätt att betrakta IPF: inte bara som en lungsjukdom utan som slutresultatet av en tarm–lunga‑axel i obalans. Om framtida forskning bekräftar dessa kopplingar kan läkare en dag diagnostisera risk tidigare med hjälp av tarm‑ eller blodmarkörer och behandla IPF inte bara med lunginriktade läkemedel, utan också med skräddarsydd kost, mikrobiella terapier eller designade metaboliter som återställer denna sköra biokemiska balans.
Citering: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Nyckelord: idiopatisk lungsjukdom, tarmmikrobiota, oxidativ stress, tryptofanmetabolism, fibros