Clear Sky Science · it
Disbiosi del microbiota intestinale e anomalie metaboliche favoriscono stress ossidativo e fibrosi nella fibrosi polmonare idiopatica
Perché il tuo intestino potrebbe contare per i tuoi polmoni
La fibrosi polmonare idiopatica (IPF) è una malattia polmonare inesorabile che cicatrizza i delicati alveoli, rendendo ogni respiro più faticoso. I medici si sono a lungo concentrati sui polmoni stessi, ma questo studio pone una domanda sorprendente: potrebbero i microbi e le sostanze chimiche presenti nell’intestino contribuire silenziosamente a guidare questo processo di cicatrizzazione? Combinando campioni di pazienti con esperimenti su animali, i ricercatori tracciano una catena di eventi dalla disbiosi intestinale allo stress chimico nel sangue e, infine, a polmoni irrigiditi e danneggiati.
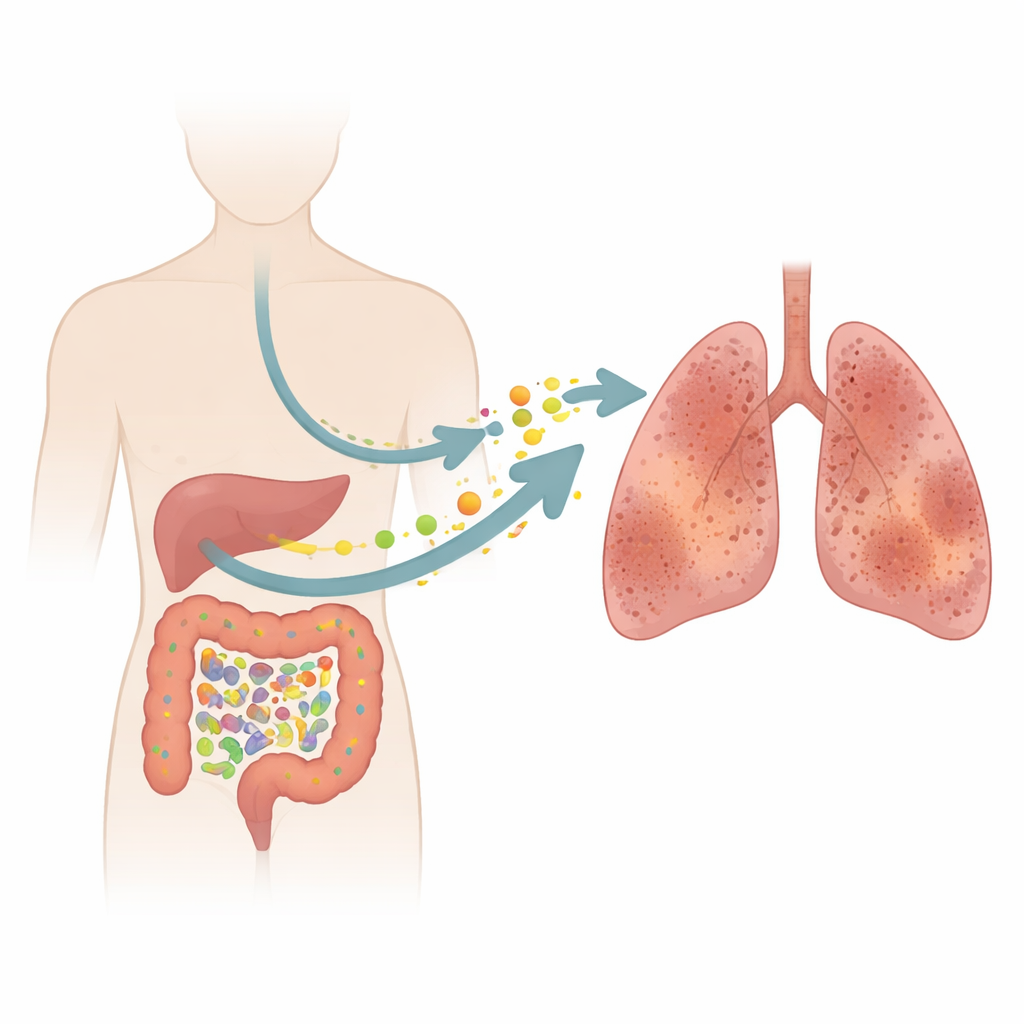
Una malattia silenziosa che ruba il respiro
L’IPF colpisce principalmente gli adulti più anziani e progressivamente li priva della capacità polmonare. In questo studio, 17 persone con IPF sono state confrontate con 17 soggetti sani di pari età e sesso. I test standard di funzionalità respiratoria hanno mostrato che i pazienti con IPF avevano volumi polmonari marcatamente ridotti e, in modo ancora più pronunciato, una minore capacità di trasferire ossigeno dall’aria al sangue. Queste misure riflettono l’ispessimento e la cicatrizzazione delle pareti degli alveoli, che intrappolano l’aria invece di permetterne il libero flusso. Nonostante esami e immagini moderne, l’IPF è ancora difficile da diagnosticare precocemente e i farmaci attuali rallentano solo, anziché arrestare, la malattia, sottolineando la necessità di cercare oltre i polmoni nuovi indizi.
La comunità intestinale e la sua impronta chimica
Il gruppo si è poi concentrato sull’intestino. I partecipanti hanno fornito campioni di feci affinché i ricercatori potessero catalogare i loro microbi intestinali e le migliaia di piccole molecole prodotte da questi microbi e dall’organismo. Complessivamente, la struttura ampia della comunità intestinale non appariva radicalmente diversa tra i pazienti e i volontari sani. Tuttavia, analisi più dettagliate hanno rivelato che alcuni gruppi batterici, in particolare quelli della famiglia Ruminococcus e una specie chiamata Ruminococcus torques, erano più abbondanti nelle persone con IPF. Allo stesso tempo, l’“impronta” chimica delle feci risultava chiaramente alterata, mostrando che anche spostamenti modesti in microbi chiave possono avere effetti sproporzionati sull’ambiente metabolico intestinale.
Una molecola protettiva mancante e l’aumento dello stress chimico
Tra le molte sostanze chimiche alterate, una è emersa in modo evidente: un piccolo dipeptide chiamato triptofano–glicina (Trp‑Gly), formato dagli amminoacidi triptofano e glicina. I livelli di questa molecola erano fortemente ridotti nei pazienti con IPF e strettamente correlati alla sovraabbondanza di Ruminococcus. Gli esami del sangue hanno aggiunto un altro pezzo al puzzle. Le persone con IPF presentavano livelli più elevati di ossido nitrico sintetasi inducibile (iNOS), un marcatore di stress ossidativo — essenzialmente l’usura chimica dei tessuti. Il loro sangue conteneva meno triptofano e glicina nel complesso, ma più chinurenina, un prodotto di degradazione del triptofano associato a infiammazione e danno ossidativo. Nel complesso, questi risultati suggeriscono che una comunità intestinale squilibrata possa consumare o deviare triptofano e glicina, esaurendo molecole potenzialmente protettive come Trp‑Gly e alimentando al tempo stesso percorsi che generano dannoso stress ossidativo.
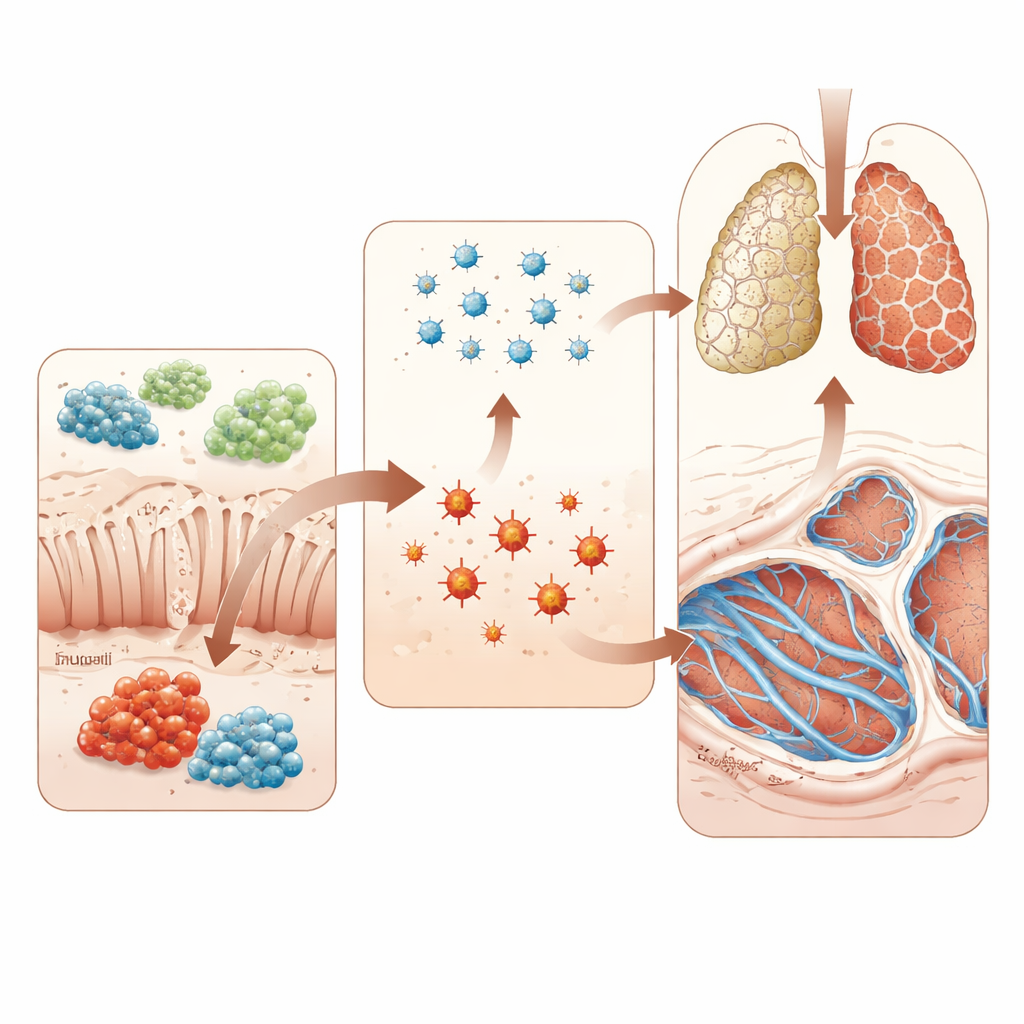
Testare la causa e l’effetto nei modelli animali
Per andare oltre la correlazione, i ricercatori hanno utilizzato un modello standard di ratto per la fibrosi polmonare indotta dal farmaco bleomicina. Alcuni animali hanno ricevuto Trp‑Gly per via orale, mentre ad altri è stato somministrato il batterio vivo R. torques. L’integrazione con Trp‑Gly ha ridotto i marker di stress ossidativo nel sangue, abbassato il peso polmonare relativo al corpo e attenuato le spesse bande di collagene e l’architettura distorta osservate al microscopio. Ha inoltre smorzato l’attività in una via chiave della fibrosi nota come TGF‑β/Smad3. In netto contrasto, i ratti trattati con R. torques mostravano una fibrosi polmonare peggiore, uno stress ossidativo più elevato e una maggiore attivazione della stessa via di segnalazione fibrotica. Questi esperimenti supportano l’idea che certi batteri intestinali possano spingere i polmoni verso la fibrosi, mentre specifiche molecole di origine intestinale possano invece contrastarla.
Cosa significa per le cure future
In termini pratici, questo lavoro propone una reazione a catena: uno spostamento malsano del microbiota intestinale, in particolare l’espansione di Ruminococcus e R. torques, interrompe la produzione di piccole molecole protettive come Trp‑Gly, che a sua volta aumenta lo stress chimico nel circolo sanguigno e attiva i programmi di cicatrizzazione nei polmoni. Sebbene lo studio sia ancora preliminare e abbia coinvolto un numero modesto di volontari e animali, indica un nuovo modo di pensare all’IPF: non solo come una malattia dei polmoni, ma come il risultato di un asse intestino‑polmone che è andato storto. Se ricerche future confermeranno questi collegamenti, un giorno i medici potrebbero diagnosticare il rischio più precocemente usando marker fecali o ematici e trattare l’IPF non solo con farmaci mirati ai polmoni, ma anche con diete personalizzate, terapie microbiche o metaboliti progettati per ripristinare questo fragile equilibrio biochimico.
Citazione: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Parole chiave: fibrosi polmonare idiopatica, microbiota intestinale, stress ossidativo, metabolismo del triptofano, fibrosi