Clear Sky Science · es
Desequilibrio de la microbiota intestinal y anomalías metabólicas promueven estrés oxidativo y fibrosis en la fibrosis pulmonar idiopática
Por qué tu intestino podría importar para tus pulmones
La fibrosis pulmonar idiopática (FPI) es una enfermedad pulmonar implacable que cicatriza los delicados sacos de aire, haciendo que cada respiración sea más difícil. Los médicos se han centrado durante mucho tiempo en los propios pulmones, pero este estudio plantea una pregunta sorprendente: ¿podrían los microbios y los compuestos químicos en nuestros intestinos contribuir silenciosamente a este proceso de cicatrización? Combinando muestras de pacientes con experimentos en animales, los investigadores trazan una cadena de acontecimientos desde el desequilibrio intestinal hasta el estrés químico en la sangre y, en última instancia, los pulmones rígidos y dañados.
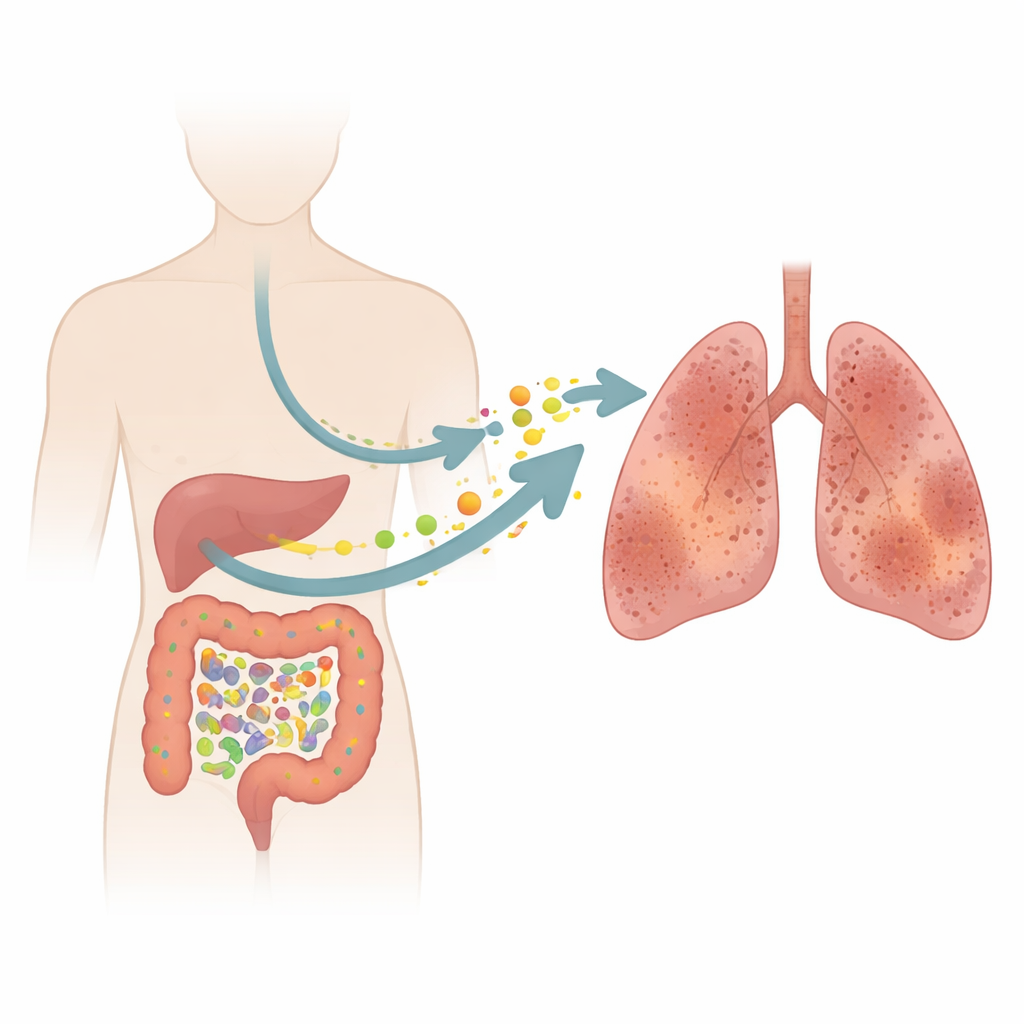
Una enfermedad silenciosa que te quita el aliento
La FPI afecta sobre todo a adultos mayores y les roba gradualmente capacidad pulmonar. En este estudio, se comparó a 17 personas con FPI con 17 sanos de edad y sexo similares. Las pruebas estándar de función respiratoria mostraron que las personas con FPI tenían volúmenes pulmonares notablemente reducidos y, de manera aún más llamativa, una menor capacidad para transferir oxígeno del aire a la sangre. Estas mediciones reflejan paredes engrosadas y cicatrizadas en los sacos de aire del pulmón, que atrapan el aire en lugar de permitir su libre circulación. A pesar de los avances en exploraciones y pruebas, la FPI sigue siendo difícil de diagnosticar de forma temprana y los fármacos actuales solo ralentizan, en lugar de detener, la enfermedad, lo que subraya la necesidad de buscar nuevas pistas más allá de los pulmones.
La comunidad intestinal y su huella química
El equipo pasó luego al intestino. Los participantes proporcionaron muestras de heces para que los investigadores pudieran catalogar sus microbios intestinales y las miles de pequeñas moléculas que esos microbios y el organismo producen. En conjunto, la estructura general de la comunidad intestinal no parecía radicalmente diferente entre pacientes y voluntarios sanos. Sin embargo, un análisis más detallado reveló que ciertos grupos bacterianos, en particular los de la familia Ruminococcus y una especie llamada Ruminococcus torques, eran más abundantes en personas con FPI. Al mismo tiempo, la “huella” química de las heces estaba claramente alterada, lo que muestra que incluso cambios modestos en microbios clave pueden tener efectos desproporcionados en el entorno metabólico del intestino.
Una molécula protectora ausente y aumento del estrés químico
Entre las muchas moléculas alteradas, destacó una: un pequeño dipéptido llamado triptófano–glicina (Trp‑Gly), formado por los aminoácidos triptófano y glicina. Los niveles de esta molécula estaban fuertemente reducidos en los pacientes con FPI y se relacionaban estrechamente con la sobreabundancia de Ruminococcus. Las pruebas de sangre añadieron otra pieza al rompecabezas. Las personas con FPI presentaban niveles más altos de óxido nítrico sintasa inducible (iNOS), un marcador de estrés oxidativo—esencialmente desgaste químico en los tejidos. Su sangre contenía menos triptófano y glicina en general, pero más quinurenina, un producto de degradación del triptófano asociado con inflamación y daño oxidativo. En conjunto, estos hallazgos sugieren que una comunidad intestinal desequilibrada puede consumir o desviar triptófano y glicina, agotando moléculas potencialmente protectoras como Trp‑Gly mientras alimenta vías que generan un estrés oxidativo dañino.
Comprobando causa y efecto en modelos animales
Para ir más allá de la correlación, los investigadores utilizaron un modelo estándar de ratas con cicatrización pulmonar inducida por el fármaco bleomicina. A algunos animales se les administró Trp‑Gly por vía oral, mientras que a otros se les dio la bacteria viva R. torques. La suplementación con Trp‑Gly redujo los marcadores de estrés oxidativo en la sangre, disminuyó el peso del pulmón en relación con el tamaño corporal y atenuó las gruesas bandas de colágeno y la arquitectura distorsionada observadas al microscopio. También amortiguó la actividad en una vía clave de fibrosis conocida como TGF‑β/Smad3. En marcado contraste, las ratas a las que se administró R. torques mostraron una fibrosis pulmonar peor, mayor estrés oxidativo y una activación más fuerte de la misma vía de señalización fibrótica. Estos experimentos apoyan la idea de que ciertas bacterias intestinales pueden empujar a los pulmones hacia la fibrosis, mientras que moléculas específicas procedentes del intestino pueden frenarla.
Qué significa esto para la atención futura
En términos prácticos, este trabajo propone una reacción en cadena: un cambio adverso en los microbios intestinales, especialmente la expansión de Ruminococcus y R. torques, altera la producción de pequeñas moléculas protectoras como Trp‑Gly, lo que a su vez eleva el estrés químico en el torrente sanguíneo y activa los programas de cicatrización en los pulmones. Aunque el estudio aún es preliminar y contó con un número modesto de voluntarios y animales, apunta a una nueva forma de entender la FPI: no solo como una enfermedad de los pulmones, sino como el resultado final de un eje intestino‑pulmón desajustado. Si investigaciones futuras confirman estos vínculos, los médicos podrían algún día diagnosticar el riesgo antes mediante marcadores intestinales o sanguíneos y tratar la FPI no solo con fármacos dirigidos a los pulmones, sino también con dietas personalizadas, terapias microbianas o metabolitos diseñados que restauren este frágil equilibrio bioquímico.
Cita: Bai, B., Li, F., Zheng, P. et al. Gut microbiota dysbiosis and metabolic abnormalities promote oxidative stress and fibrosis in idiopathic pulmonary fibrosis. Sci Rep 16, 12305 (2026). https://doi.org/10.1038/s41598-026-43366-2
Palabras clave: fibrosis pulmonar idiopática, microbiota intestinal, estrés oxidativo, metabolismo del triptófano, fibrosis