Clear Sky Science · zh
利用双特异性 αGD2×αCD3 蛋白接合器靶向GD2高表达的肺肿瘤
为何动员免疫系统对抗肺癌很重要
肺癌仍然是全球最致命的癌症之一,部分原因在于常常晚期才被诊断出且能抵抗手术、化疗和放疗等标准疗法。近年来,科学家们开始教免疫系统更精确地识别并摧毁癌细胞。本研究探索了一种新途径:设计一种定制蛋白,将免疫细胞物理性地连接到带有特定表面标志的肺癌细胞上,可能为更靶向且毒性更低的治疗开辟道路。
肺癌细胞上的特殊“旗帜”
癌细胞常在表面呈现异常分子,可作为靶向治疗的标志。其中一种是 GD2,一种脂糖分子,在某些肿瘤上高表达,但在大多数正常组织上仅稀少分布。作者首先调查了 GD2 在肺癌细胞中的普遍程度。使用标准的实验室细胞系,他们发现一种称为 A549 的腺癌细胞系携带的 GD2 量远高于另一种非小细胞肺癌细胞系 NCI-H460。这证实至少部分肺癌能强烈表达 GD2,因此可以基于该标志被识别出来。
构建分子“红娘”
为利用这一差异,团队设计了一种“双特异性蛋白接合器”,这是一种紧凑的融合蛋白,旨在同时抓住两种不同的细胞。一端识别肿瘤细胞表面的 GD2;另一端识别 T 细胞上的关键分子 CD3,T 细胞是免疫系统的主要攻击力量。该 55 千道尔顿的蛋白在来源于人类细胞的生产体系中表达并从培养液中纯化,结构稳定且可用常规生化方法检测到。结合研究显示它能强烈结合含有丰富 GD2 的细胞,比如 A549 和一个高 GD2 的骨癌细胞系,并能通过 CD3 结合 T 细胞,但对 GD2 或 CD3 含量很少的细胞几乎不结合。换句话说,它充当了 GD2 丰富的癌细胞与 T 细胞之间的选择性分子桥梁。
温和唤醒免疫细胞
接着,研究者检查该桥梁能否在不损伤 T 细胞的情况下激活它们。将来自健康供体的正常免疫细胞在体外暴露于该新型蛋白时,细胞死亡水平与未处理对照相近,且远低于强烈非特异性激活剂。同时,双特异性蛋白促使 T 细胞进入活跃状态:更多细胞开始分裂,并开始表达与激活相关的表面标志。与强效实验室刺激物相比,增幅适中但明显高于基线,表明该接合器可以以可控方式唤醒 T 细胞。
促成与肺肿瘤的近距离接触
最重要的测试是这种方法是否能帮助 T 细胞更有效地杀死肺癌细胞。科学家们首先通过使 T 细胞饱和结合该双特异性蛋白来“武装”它们,形成所谓的接合器武装 T 细胞。随后将这些武装细胞与未武装的 T 细胞分别与表现低或高 GD2 的肺癌细胞混合。在低 GD2 的 NCI-H460 细胞面前,差别不大:两类 T 细胞仅能杀死有限数量的靶细胞。但在高 GD2 的 A549 细胞面前,武装的 T 细胞更为高效,共培养两天后存活的癌细胞显著更少。显微镜观察确认武装 T 细胞簇集并破坏这些 GD2 丰富的靶细胞,与分子桥将两类细胞拉拢在一起的设想一致。
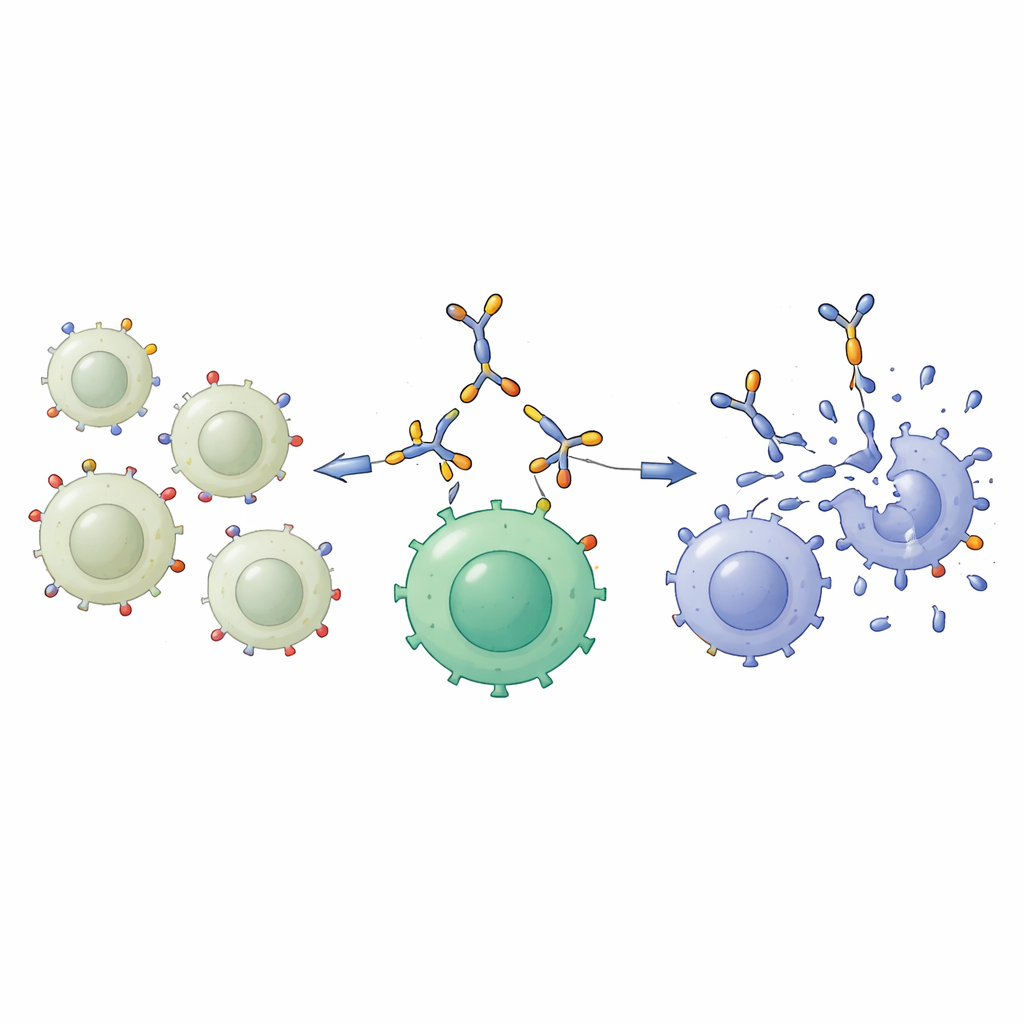
这对患者可能意味着什么
总体来看,该研究表明精心设计的双特异性蛋白可以安全地将 T 细胞与 GD2 丰富的肺癌细胞连接起来,适度增强 T 细胞活性,并显著提高它们在体外杀死这些肿瘤细胞的能力,尤其是在 GD2 标志丰富时。尽管这项工作仍处于临床前阶段,且在细胞培养中完成而非患者体内,但它提出了一种针对 GD2 高表达肺癌的潜在新策略。未来,对肿瘤 GD2 水平的检测可能有助于识别最有可能从此类靶向免疫“红娘”中受益的患者,且还需要进一步的动物和临床研究来验证这种潜力是否能转化为现实世界的获益。
引用: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
关键词: 肺癌免疫疗法, GD2 靶向, 双特异性接合器, T 细胞再定向, 非小细胞肺癌