Clear Sky Science · he
שימוש במחבר חלבוני דואל-ספציפי αGD2 × αCD3 למיקוד גידולים ריאתיים בעלי הבעה יתר של GD2
מדוע חשוב להפעיל את מערכת החיסון נגד סרטן הריאה
סרטן הריאה נשאר בין הסרטן הקטלניים ביותר בעולם, בחלקו מכיוון שהוא מאובחן לעתים קרובות בשלבים מתקדמים ויכול לעמוד בפני טיפולים סטנדרטיים כמו ניתוח, כימותרפיה וקרינה. בשנים האחרונות מדענים החלו ללמד את מערכת החיסון לזהות ולהשמיד תאי סרטן בדיוק רב יותר. מחקר זה בוחן דרך חדשה לעשות זאת על ידי עיצוב חלבון מיוחד שמקשר פיזית בין תאי החיסון לתאי סרטן הריאה הנושאים סימן פני שטח מסוים, ובכך עשוי לפתוח נתיב לטיפולים ממוקדים ופחות רעילים.
דגל מיוחד על תאי סרטן הריאה
תאי סרטן לעתים מציגים מולקולות בלתי רגילות על פני שטחם שיכולות לשמש כדגלים לטיפולים ממוקדים. דגל כזה הוא GD2, מולקולת שומן-סוכר הנשענת על ממברנה ונמצאת ברמות גבוהות בגידולים מסוימים אך מועטה ברוב הרקמות התקינות. החוקרים שאלו ראשית עד כמה GD2 שכיח בתאי סרטן הריאה. באמצעות קווי תאים מעבדתיים סטנדרטיים הם מצאו כי קו אדנוקרצינומה בשם A549 נושא כמויות גבוהות בהרבה של GD2 בהשוואה לקו אחר של סרטן ריאה לא-תאי קטן, NCI-H460. ממצא זה אישר שלפחות חלק ממקרי סרטן הריאה מציגים GD2 בעוז ויכולים לפיכך להיות מזוהים על פי סממן זה.
בניית "מגרש שידוכים" מולקולרי
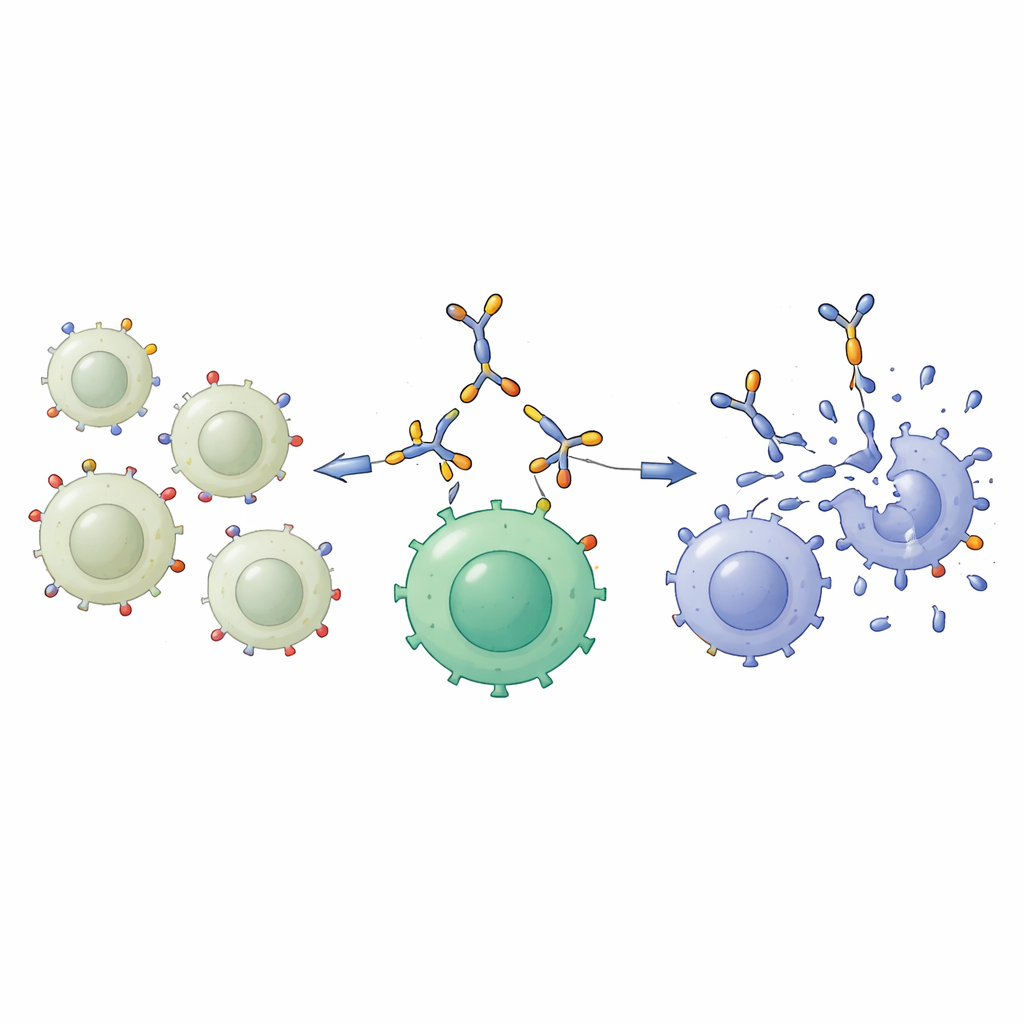
כדי לנצל הבדל זה, הצוות מהנדס "מחבר חלבוני דו-ספציפי", חלבון פיוז'ן קומפקטי שתוכנן לתפוס שני סוגי תאים בו-זמנית. קצה אחד מזהה את GD2 על פני התא הסרטני; הקצה השני מזהה את CD3, מולקולה מרכזית על תאי T, כוחות ההתקפה העיקריים של מערכת החיסון. החלבון, שיוצר בתאים שמקורם אנושי ונוקה מנוזל התרבית, שקול במשקל של כ-55 קילודלטון ושמר על מבנה יציב שניתן היה לזהותו בשיטות ביוכימיות סטנדרטיות. ניסויי קשירה הראו שהוא היתפס בחוזקה לתאים בעלי GD2 בשפע, כמו A549 וקו סרטן עצם בעל GD2 גבוה, וכן לתאי T דרך CD3, בעוד שהיתה קשירה מזערית לתאים עם מעט או ללא GD2 או CD3. במילים אחרות, הוא התנהג כגשר מולקולרי סלקטיבי בין תאים סרטניים עשירים ב-GD2 לבין תאי T.
התעוררות מתונה של תאי החיסון
בהמשך חקרו החוקרים האם הגשר הזה יכול להפעיל תאי T בלי להזיק להם. כאשר תאי חיסון נורמליים מתורמים בריאים נחשפו לחלבון החדש במעבדה, שיעור המוות התאי נשאר דומה לקבוצות הביקורת שלא טופלו והרבה מתחת לאלו שטופלו במפעיל לא-ספציפי חזק. במקביל, החלבון הדו-ספציפי דחף את תאי T לפעולה: יותר מהם החלו להתחלק והחלו לבטא סמני פני שטח המשויכים להפעלה. העלייה הייתה צנומה ביחס למעורר מעבדתי עוצמתי, אך לעומת הקו הבסיסי היתה ברורה, מה שמראה שהמחבר יכול לעורר תאי T באופן מבוקר.
אילוץ מפגש קרוב עם הגידולים הריאתיים
הבדיקה החשובה ביותר היתה האם גישה זו יכולה לסייע לתאי T להרוג תאי סרטן ריאה ביעילות רבה יותר. המדענים קודם כל "חמשו" תאי T על ידי רוויה שלהם בחלבון הדו-ספציפי, ויצרו את מה שמכונים תאי T חמושים במחבר. תאים חמושים אלה ותאי T לא חמושים עורבבו אז עם תאי סרטן ריאה שהציגו רמות GD2 נמוכות או גבוהות. מול תאי NCI-H460 בעלי GD2 נמוך לא נצפה הבדל משמעותי: שני סוגי תאי T הרגו מספר מוגבל של מטרות. אך מול תאי A549 בעלי GD2 גבוה, תאי T החמושים היו יעילים בהרבה, והשאירו הרבה פחות תאים סרטניים חיים לאחר יומיים של תרבית משותפת. מיקרוסקופיה אישרה כי תאי T החמושים התקבצו סביב והשמידו מטרות עשירות ב-GD2, בהתנהגות התואמת לרעיון שהגשר המולקולרי משך את שני סוגי התאים זה אל זה.
מה זה עלול להצביע עבור מטופלים
בסך הכול, המחקר מראה כי חלבון דו-ספציפי שעוצב בקפידה יכול לחבר בבטחה תאי T לתאי סרטן ריאה עשירים ב-GD2, להגביר במידה מתונה את פעילות תאי ה-T ולהגביר באופן בולט את יכולתם להרוג את התאים הסרטניים במעבדה, במיוחד כאשר דגל ה-GD2 שופע. בעוד שהעבודה עדיין נמצאת בשלב טרום-קליני ובוצעה בתרביות תאיות ולא בחולים, היא מציעה אסטרטגיה חדשה לטיפול בגידולי ריאה שמביעים GD2 ביתר. בעתיד, מדידת רמת GD2 בגידול עשויה לסייע לזהות את המטופלים שסביר שיעילו מה"מגרשי שידוכים" החיסוניים הממוקדים האלה, וידרשו מחקרים נוספים בבעלי חיים ובניסויים קליניים כדי לברר האם ההבטחה הזו תתורגם לתועלת בעולם האמיתי.
ציטוט: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
מילות מפתח: אימונותרפיה לסרטן הריאה, מיקוד ב-GD2, מחבר דו-ספציפי, הכוונת תאי T, סרטן ריאה שאינו תאי קטן