Clear Sky Science · ru
Использование биспецифического связывающего белка αGD2 × αCD3 для нацеливания на опухоли легкого с гиперэкспрессией GD2
Почему важно направить иммунную систему против рака легких
Рак легкого по‑прежнему остается одним из самых смертоносных видов рака в мире, отчасти потому, что часто выявляется на поздних стадиях и может сопротивляться стандартным методам лечения — хирургии, химио- и радиотерапии. В последние годы ученые научились точнее обучать иммунную систему распознавать и уничтожать раковые клетки. В этом исследовании изучается новый подход: создание специально сконструированного белка, который физически связывает иммунные клетки с клетками рака легкого, несущими специфический поверхностный маркер, что потенциально открывает путь к более целенаправленным и менее токсичным терапиям.
Особенный флаг на клетках рака легких
Раковые клетки часто демонстрируют на поверхности необычные молекулы, которые могут служить «флагами» для таргетной терапии. Одним из таких флагов является GD2 — липосахаридный компонент, встречающийся в высоких концентрациях на некоторых опухолях и лишь в небольших количествах на большинстве нормальных тканей. Авторы сначала выяснили, насколько широко распространен GD2 на клетках рака легких. На стандартных лабораторных линиях клеток они обнаружили, что аденокарцинома A549 несет гораздо больше GD2, чем другая линия немелкоклеточного рака легкого NCI‑H460. Это подтвердило, что по крайней мере некоторые раки легких сильно экспрессируют GD2 и поэтому могут быть выделены на основе этого маркера.
Построение молекулярного свахина
Чтобы использовать это различие, команда создала «биспецифический связывающий белок» — компактный белковый фьюжн, спроектированный так, чтобы захватывать два разных типа клеток одновременно. Один конец распознает GD2 на поверхности опухолевой клетки; другой — CD3, ключевой компонент на Т‑клетках, главной ударной силе иммунной системы. Белок, полученный в клетках человеческого происхождения и очищенный из культуральной жидкости, имел массу около 55 килодальтон и сохранял свою структуру, что подтверждалось стандартными биохимическими методами. Исследования связывания показали, что он прочно присоединяется к клеткам с высоким содержанием GD2, таким как A549 и линия костной опухоли с высокой экспрессией GD2, а также к Т‑клеткам через CD3, но практически не связывается с клетками, имеющими мало или совсем не имеющими GD2 или CD3. Иными словами, он выступал как селективный молекулярный мост между клетками, богатые GD2, и Т‑клетками.
Мягкое пробуждение иммунных клеток
Далее исследователи проверили, может ли этот мост активировать Т‑клетки, не повреждая их. При воздействии нормальных иммунных клеток от здоровых доноров новым белком в лаборатории уровни гибели клеток оставались сопоставимыми с необработанными контролями и значительно ниже, чем при применении сильного неспецифического активатора. В то же время биспецифический белок стимулировал Т‑клетки: большее число клеток стало делиться и начало экспрессировать поверхностные маркеры, связанные с активацией. Прирост был умеренным по сравнению с мощным лабораторным стимулятором, но явно превышал исходный уровень, показывая, что энгагер может аккуратно пробуждать Т‑клетки.
Принуждение к близкой встрече с опухолями легкого
Ключевым тестом была проверка, поможет ли этот подход Т‑клеткам эффективнее убивать клетки рака легкого. Сначала ученые «вооружили» Т‑клетки, насыщая их биспецифическим белком, создав так называемые энгагер‑вооруженные Т‑клетки. Эти вооруженные и невооруженные Т‑клетки затем смешивали с клетками рака легкого, демонстрировавшими либо низкий, либо высокий уровень GD2. Против клеток NCI‑H460 с низким содержанием GD2 различий было мало: оба типа Т‑клеток уничтожили лишь ограниченное число мишеней. Но против клеток A549 с высоким уровнем GD2 вооруженные Т‑клетки были значительно эффективнее, оставляя намного меньше живых раковых клеток после двух дней совместной культуры. Микроскопия подтвердила, что вооруженные Т‑клетки образуют скопления вокруг и разрушают эти GD2‑богатые мишени, что согласуется с идеей, что молекулярный мост способствует сближению двух типов клеток.
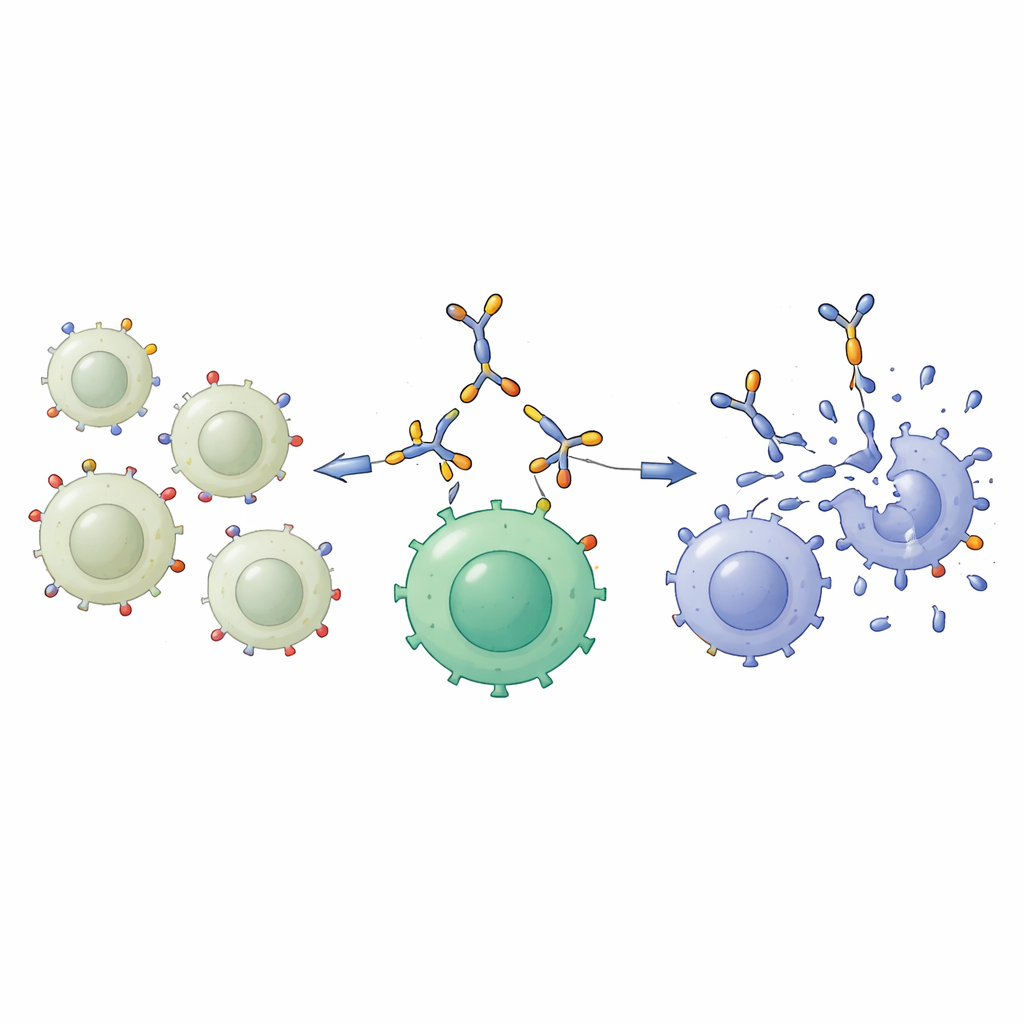
Что это может значить для пациентов
В целом исследование показывает, что тщательно спроектированный биспецифический белок может безопасно соединять Т‑клетки с GD2‑богатыми клетками рака легкого, умеренно усиливать активность Т‑клеток и резко повышать их способность убивать эти опухолевые клетки в лабораторных условиях, особенно при высокой экспрессии GD2. Хотя работа пока находится на доклинической стадии и проведена в культурах клеток, а не у пациентов, она предлагает новую стратегию лечения раков легкого с гиперэкспрессией GD2. В будущем измерение уровня GD2 в опухоли может помочь выявить пациентов, которые с наибольшей вероятностью получат пользу от таких целевых иммунных «свах», а дополнительные исследования на животных и клинические испытания потребуются, чтобы понять, реализуется ли этот потенциал в реальной клинической пользе.
Цитирование: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
Ключевые слова: иммунотерапия рака легких, таргетирование GD2, биспецифический энгагер, перенаправление Т-клеток, немелкоклеточный рак легкого