Clear Sky Science · de
Ausnutzung eines bispezifischen αGD2 × αCD3 Protein-Engagers zur gezielten Bekämpfung von GD2-überexprimierenden Lungentumoren
Warum es wichtig ist, das Immunsystem gegen Lungenkrebs zu richten
Lungenkrebs bleibt eine der tödlichsten Krebsarten weltweit, teilweise weil er oft spät erkannt wird und gegen Standardbehandlungen wie Operation, Chemotherapie und Strahlentherapie resistent sein kann. In den letzten Jahren haben Forschende begonnen, dem Immunsystem beizubringen, Krebszellen präziser zu erkennen und zu zerstören. Diese Studie untersucht einen neuen Ansatz, indem ein maßgeschneidertes Protein entwickelt wird, das Immunzellen physisch mit Lungenkrebszellen verbindet, die einen bestimmten Oberflächenmarker tragen, und damit möglicherweise einen Weg zu gezielteren und weniger toxischen Therapien eröffnet.
Ein besonderes Erkennungszeichen auf Lungenkrebszellen
Krebszellen zeigen oft ungewöhnliche Moleküle auf ihrer Oberfläche, die als Markierungen für gezielte Therapien dienen können. Eine solche Markierung ist GD2, ein Lipid‑Zucker‑Molekül, das auf bestimmten Tumoren in hohen Mengen vorkommt, aber in den meisten normalen Geweben nur selten vorhanden ist. Die Autorinnen und Autoren fragten zunächst, wie verbreitet GD2 auf Lungenkrebszellen ist. Anhand gängiger Zelllinien im Labor stellten sie fest, dass eine Adenokarzinom‑Linie namens A549 deutlich höhere Mengen an GD2 aufwies als eine andere nicht‑kleinzellige Lungenkrebs‑Linie, NCI‑H460. Das bestätigt, dass zumindest einige Lungenkrebse GD2 stark exprimieren und somit anhand dieses Markers identifiziert werden könnten.
Ein molekularer Kuppler wird gebaut
Um diesen Unterschied zu nutzen, entwickelte das Team einen „bispezifischen Protein‑Engager“, ein kompaktes Fusionsprotein, das dafür ausgelegt ist, zwei verschiedene Zelltypen gleichzeitig zu greifen. Ein Ende erkennt GD2 auf der Tumorzelloberfläche; das andere Ende erkennt CD3, ein Schlüsselmolekül auf T‑Zellen, der Hauptangriffskraft des Immunsystems. Hergestellt in menschlichen Zellen und aus dem Kulturüberstand gereinigt, behielt dieses 55‑Kilodalton‑Protein zuverlässig seine Struktur und war mit gängigen biochemischen Methoden nachweisbar. Bindungsstudien zeigten, dass es stark an Zellen mit hohem GD2‑Gehalt wie A549 und an einer Knochenkrebs‑Linie mit hoher GD2‑Expression sowie an T‑Zellen über CD3 band, aber kaum an Zellen mit wenig oder keinem GD2 bzw. CD3. Mit anderen Worten: Es fungierte als selektive molekulare Brücke zwischen GD2‑reichen Krebszellen und T‑Zellen.
Das behutsame Wecken von Immunzellen
Als Nächstes prüften die Forschenden, ob diese Brücke T‑Zellen aktivieren kann, ohne ihnen zu schaden. Wenn normale Immunzellen von gesunden Spendern im Labor dem neuen Protein ausgesetzt wurden, blieben die Sterblichkeitsraten ähnlich wie bei unbehandelten Kontrollen und deutlich niedriger als bei einem starken, unspezifischen Aktivator. Gleichzeitig brachte das bispezifische Protein T‑Zellen in Stellung: Mehr Zellen begannen sich zu teilen und zeigten Oberflächenmarker, die mit Aktivierung assoziiert sind. Der Anstieg war im Vergleich zu einem starken Laborstimulator moderat, aber deutlich über dem Ausgangsniveau, was zeigt, dass der Engager T‑Zellen kontrolliert stimulieren kann.
Erzwingen einer engen Begegnung mit Lungentumoren
Der wichtigste Test war, ob dieser Ansatz T‑Zellen dabei helfen kann, Lungenkrebszellen effizienter zu töten. Die Wissenschaftler bewaffneten zunächst T‑Zellen, indem sie diese mit dem bispezifischen Protein sättigten und so sogenannte engager‑bewaffnete T‑Zellen erzeugten. Diese bewaffneten und unbewaffneten T‑Zellen wurden dann mit Lungenkrebszellen mit entweder niedrigen oder hohen GD2‑Werten zusammengebracht. Gegen die GD2‑armen NCI‑H460‑Zellen gab es kaum Unterschiede: Beide T‑Zelltypen töteten nur eine begrenzte Anzahl von Zielzellen. Dagegen waren die bewaffneten T‑Zellen gegen die GD2‑reichen A549‑Zellen deutlich wirksamer und ließen nach zwei Tagen Kokkultur viel weniger Krebszellen am Leben. Mikroskopie bestätigte, dass sich die bewaffneten T‑Zellen um diese GD2‑reichen Ziele sammelten und sie zerstörten, was zur Idee passt, dass die molekulare Brücke die beiden Zelltypen zusammenführt.
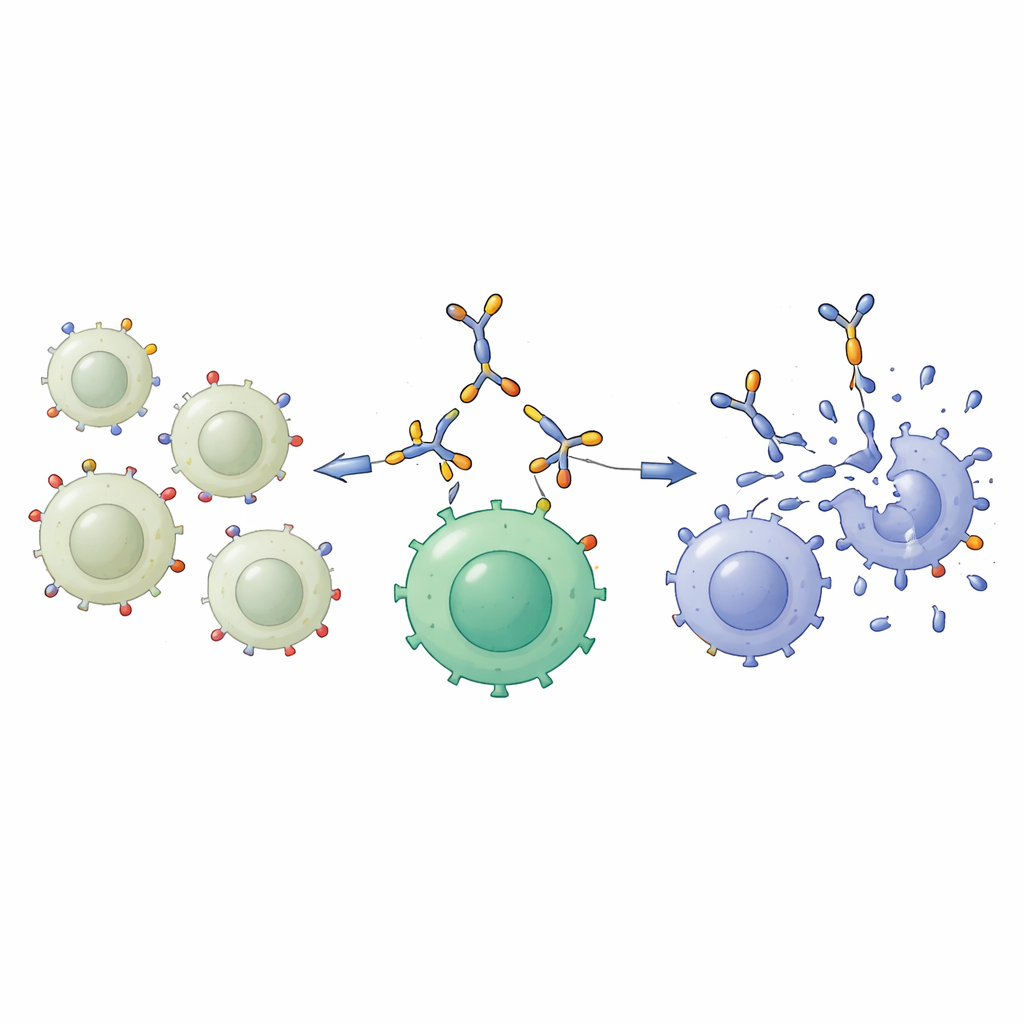
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt zeigt die Studie, dass ein sorgfältig entworfener bispezifischer Protein‑Engager T‑Zellen sicher mit GD2‑reichen Lungenkrebszellen verbinden, die T‑Zellaktivität moderat steigern und ihre Fähigkeit, diese Tumorzellen im Labor zu töten, deutlich erhöhen kann — insbesondere wenn die GD2‑Markierung reichlich vorhanden ist. Obwohl diese Arbeit noch präklinisch ist und in Zellkulturen statt in Patientinnen und Patienten durchgeführt wurde, deutet sie auf eine neue Strategie zur Behandlung von Lungenkrebserkrankungen hin, die GD2 überexprimieren. In Zukunft könnte die Messung des GD2‑Spiegels eines Tumors helfen, die Patientinnen und Patienten zu identifizieren, die am ehesten von solchen gezielten immunologischen „Kupplern“ profitieren, und weitere Tier‑ und klinische Studien werden erforderlich sein, um zu prüfen, ob dieses Versprechen in der Praxis ankommt.
Zitation: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
Schlüsselwörter: Immuntherapie bei Lungenkrebs, GD2-Zielerkennung, bispezifischer Engager, Umlenkung von T‑Zellen, nicht‑kleinzelliger Lungenkrebs