Clear Sky Science · nl
Het inzetten van een bispecifieke αGD2 × αCD3 proteïne-engager om GD2-overexpresserende longtumoren te richten
Waarom het belangrijk is het immuunsysteem tegen longkanker te keren
Longkanker blijft een van de dodelijkste kankers wereldwijd, deels omdat het vaak laat wordt ontdekt en resistent kan zijn tegen standaardbehandelingen zoals chirurgie, chemotherapie en bestraling. In de afgelopen jaren zijn wetenschappers begonnen het immuunsysteem te leren kankercellen preciezer te herkennen en te vernietigen. Deze studie onderzoekt een nieuwe benadering daarvoor door een op maat gemaakt eiwit te ontwerpen dat immuuncellen fysiek aan longkankercellen met een bepaald oppervlaktemarker koppelt, wat mogelijk een route opent naar meer gerichte en minder toxische therapieën.
Een speciaal vaantje op longkankercellen
Kankercellen tonen vaak ongebruikelijke moleculen op hun oppervlak die als herkenningsvlaggen voor gerichte therapieën kunnen dienen. Een zo’n vlag is GD2, een vet-suikermolecuul dat in hoge concentraties voorkomt op bepaalde tumoren maar slechts schaars op de meeste normale weefsels. De auteurs vroegen zich eerst af hoe algemeen GD2 op longkankercellen voorkomt. Met behulp van standaard laboratoriumcelijnen vonden ze dat een adenocarcinoomlijn genaamd A549 veel hogere hoeveelheden GD2 droeg dan een andere niet-kleincellige longkankerlijn, NCI-H460. Dit bevestigde dat ten minste sommige longkankers GD2 sterk tot expressie brengen en daarom op basis van deze marker kunnen worden onderscheiden.
Een moleculaire koppelaar bouwen
Om van dit verschil te profiteren, ontwierp het team een “bispecifiek eiwit-engager”, een compact fusie-eiwit dat is ontworpen om twee verschillende celtypen tegelijk te grijpen. Het ene uiteinde herkent GD2 op het tumorceloppervlak; het andere uiteinde herkent CD3, een sleutelmolecuul op T-cellen, de belangrijkste aanvalseenheid van het immuunsysteem. Geproduceerd in mensafgeleide cellen en gezuiverd uit het kweekmedium, behield dit 55-kilodalton-eiwit betrouwbaar zijn structuur en kon het met standaard biochemische methoden worden aangetoond. Bindingsstudies toonden aan dat het sterk aan cellen met veel GD2 hechtte, zoals A549 en een botkankerlijn met hoge GD2-expressie, en aan T-cellen via CD3, maar nauwelijks aan cellen met weinig of geen GD2 of CD3. Met andere woorden, het functioneerde als een selectieve moleculaire brug tussen GD2-rijke kankercellen en T-cellen.
Het immuunsysteem voorzichtig wekken
Vervolgens onderzochten de onderzoekers of deze brug T-cellen kon activeren zonder ze te beschadigen. Wanneer normale immuuncellen van gezonde donors in het laboratorium aan het nieuwe eiwit werden blootgesteld, bleven de niveaus van celdood vergelijkbaar met onbehandelde controles en veel lager dan bij een sterke niet-specifieke activator. Tegelijkertijd zette het bispecifieke eiwit T-cellen aan tot activiteit: meer van hen begonnen zich te delen en ze gingen oppervlaktemarkers tot expressie brengen die met activatie geassocieerd zijn. De toename was bescheiden vergeleken met een krachtige laboratoriumstimulator, maar duidelijk boven de basislijn, wat laat zien dat de engager T-cellen op een gecontroleerde manier kon wakker maken.
Een nauwe ontmoeting met longtumoren afdwingen
De belangrijkste test was of deze benadering T-cellen efficiënter kon laten doden van longkankercellen. De wetenschappers “bewapenden” eerst T-cellen door ze te verzadigen met het bispecifieke eiwit, waardoor zogeheten engager-bewapende T-cellen ontstonden. Deze bewapende cellen en onbewapende T-cellen werden vervolgens gemengd met longkankercellen die ofwel lage ofwel hoge GD2-niveaus vertoonden. Tegen de laag-GD2 NCI-H460-cellen was er weinig verschil: beide typen T-cellen doodden slechts een beperkt aantal doelcellen. Maar tegen de hoog-GD2 A549-cellen waren de bewapende T-cellen veel effectiever, met veel minder overlevende kankercellen na twee dagen co-cultuur. Microscopie bevestigde dat de bewapende T-cellen zich rondom deze GD2-rijke doelwitten concentreerden en ze vernietigden, in overeenstemming met het idee dat de moleculaire brug de twee celtypen naar elkaar toe trok.
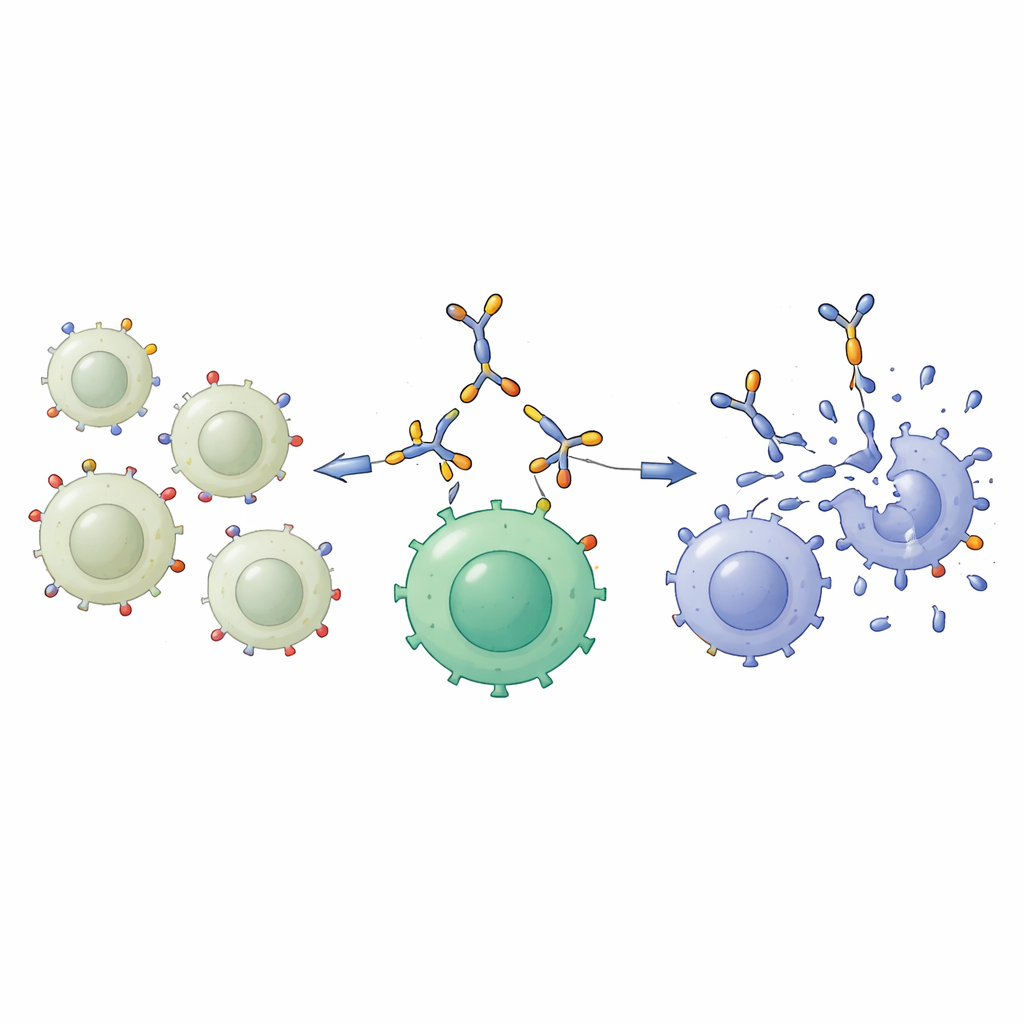
Wat dit voor patiënten zou kunnen betekenen
Al met al toont de studie aan dat een zorgvuldig ontworpen bispecifiek eiwit T-cellen veilig kan verbinden met GD2-rijke longkankercellen, de T-celactiviteit bescheiden kan verhogen en hun vermogen om die tumorcellen in het lab te doden sterk kan vergroten, vooral wanneer de GD2-vlag overvloedig aanwezig is. Hoewel dit werk nog in de preklinische fase is en in kweekcellen in plaats van bij patiënten is uitgevoerd, suggereert het een nieuwe strategie voor de behandeling van longkankers die GD2 overexpresseren. In de toekomst zou het meten van het GD2-niveau van een tumor kunnen helpen de patiënten te identificeren die het meeste baat hebben bij dergelijke gerichte immuun-“koppelaars”, en zullen verdere dier- en klinische studies nodig zijn om te bepalen of deze belofte zich vertaalt naar reële voordelen.
Bronvermelding: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
Trefwoorden: immunotherapie bij longkanker, GD2-targeting, bispecifieke engager, heroriëntatie van T-cellen, niet-kleincellige longkanker