Clear Sky Science · tr
GD2 fazlasıyla ifade edilen akciğer tümörlerini hedeflemek için bispesifik αGD2 × αCD3 protein aracısını kullanmak
İmmün sistemi akciğer kanserine karşı çevirmek neden önemli
Akciğer kanseri, sıklıkla geç evrede tanı konması ve cerrahi, kemoterapi ve radyasyon gibi standart tedavilere direnç gösterebilmesi nedeniyle dünya çapında en ölümcül kanserlerden biridir. Son yıllarda bilim insanları, immün sistemi kanser hücrelerini daha hassas biçimde tanıyıp yok etmeye öğretecek yaklaşımlar geliştirmeye başladı. Bu çalışma, bağışıklık hücrelerini belirli bir yüzey işaretini taşıyan akciğer kanseri hücrelerine fiziksel olarak bağlayan, özel tasarlanmış bir protein aracısı geliştirerek bu hedefe ulaşmanın yeni bir yolunu araştırıyor; bu da daha hedefli ve daha az toksik tedavilere kapı açabilir.
Akciğer kanseri hücrelerindeki özel bir işaret
Kanser hücreleri sıklıkla yüzeylerinde hedefe yönelik tedaviler için işaret görevi görebilecek alışılmadık moleküller gösterir. Bu işaretlerden biri GD2’dir; belirli tümörlerde yüksek düzeyde bulunan, çoğu normal dokuda ise nadiren bulunan yağlı-şeker yapısında bir moleküldür. Yazarlar önce GD2’nin akciğer kanseri hücrelerinde ne kadar yaygın olduğunu sordular. Standart laboratuvar hücre hatlarını kullanarak, A549 adındaki bir adenokarsinom hattının NCI-H460 adlı başka bir küçük hücre dışı akciğer kanseri hattına göre çok daha yüksek miktarda GD2 taşıdığını buldular. Bu, en azından bazı akciğer kanserlerinin güçlü biçimde GD2 gösterdiğini ve bu belirtece göre seçilebileceğini doğruladı.
Moleküler bir çöpçatan inşa etmek
Bu farktan yararlanmak için ekip ‘‘bispesifik protein aracısı’’ olarak adlandırılan, aynı anda iki farklı hücre tipini yakalayacak şekilde tasarlanmış kompakt bir füzyon protein mühendisliği yaptı. Bir ucu tümör hücre yüzeyindeki GD2’yi tanırken diğer ucu T hücrelerinin ana saldırı molekülü olan CD3’ü tanıyor. İnsan kökenli hücrelerde üretilip kültür sıvısından saflaştırılan bu 55 kilodaltonluk protein yapısını korudu ve standart biyokimyasal yöntemlerle tespit edilebildi. Bağlanma çalışmaları, proteinin A549 gibi bol GD2’ye sahip hücrelere ve yüksek-GD2 kemik kanseri hattına güçlü biçimde bağlandığını; ve T hücrelerine CD3 üzerinden bağlandığını, ancak çok az veya hiç GD2 ya da CD3 içeren hücrelere neredeyse bağlanmadığını gösterdi. Başka bir deyişle, GD2 açısından zengin kanser hücreleri ile T hücreleri arasında seçici bir moleküler köprü görevi gördü.
İmmün hücreleri nazikçe uyandırmak
Ardından araştırmacılar bu köprünün T hücrelerini zarar vermeden aktive edip edemeyeceğini kontrol ettiler. Sağlıklı bağışçılardan alınan normal immün hücreler laboratuvarda yeni proteinle muamele edildiğinde, hücre ölümü düzeyleri tedavi edilmemiş kontrolere benzer kaldı ve güçlü, özgül olmayan bir aktivatörden çok daha düşüktü. Aynı zamanda bispesifik protein, T hücrelerini harekete geçirmeye itti: daha fazlası bölünmeye başladı ve aktivasyonla ilişkili yüzey belirteçlerini göstermeye başladı. Artış güçlü bir laboratuvar uyarıcısına kıyasla ılımlı olsa da, başlangıç seviyesinin üzerinde olup aracının T hücrelerini kontrollü bir şekilde uyandırabildiğini gösteriyordu.
Akciğer tümörleriyle yakın karşılaşmayı zorlamak
En önemli test, bu yaklaşımın T hücrelerinin akciğer kanseri hücrelerini daha verimli öldürmesine yardımcı olup olmayacağıydı. Bilim insanları önce T hücrelerini bispesifik proteinle doygun hale getirip ‘‘aracılı T hücreler’’ oluşturdu. Bu silahlanmış hücreler ile silahsız T hücreler daha sonra düşük veya yüksek GD2 seviyelerine sahip akciğer kanseri hücreleriyle karıştırıldı. Düşük GD2 taşıyan NCI-H460 hücrelerine karşı pek fark yoktu: her iki T hücresi tipi de yalnızca sınırlı sayıda hedefi öldürdü. Ancak yüksek GD2 taşıyan A549 hücrelerine karşı, aracılı T hücreler çok daha etkiliydi ve iki günlük ortak kültürün ardından çok daha az kanser hücresi canlı kaldı. Mikroskopi, aracılı T hücrelerin bu GD2 zengin hedeflerin etrafında kümelendiğini ve onları yok ettiğini doğruladı; bu da moleküler köprünün iki hücre tipini birbirine çektiği fikriyle uyumluydu.
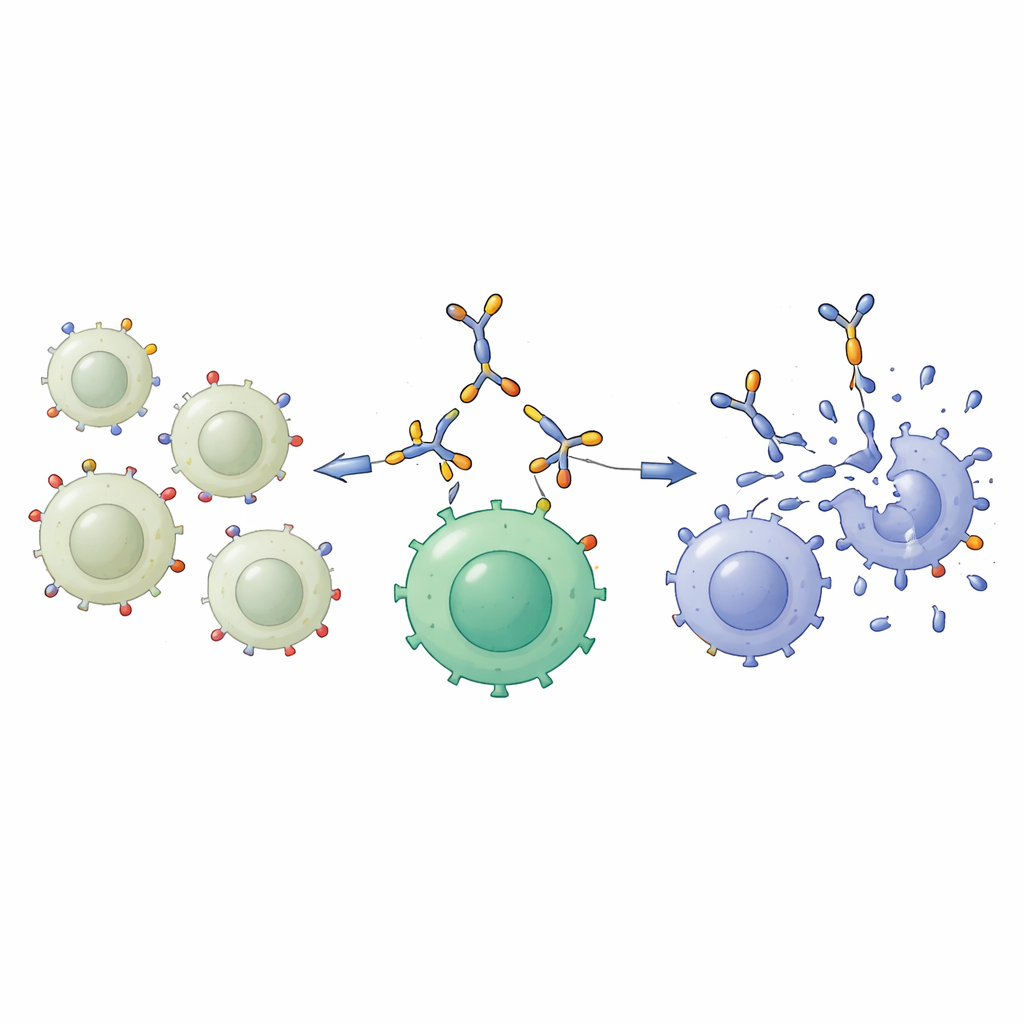
Bu hastalar için ne anlama gelebilir
Genel olarak çalışma, dikkatle tasarlanmış bir bispesifik proteinin T hücrelerini GD2 zengini akciğer kanseri hücrelerine güvenli biçimde bağlayabileceğini, T hücresi aktivitesini ılımlı şekilde artırabileceğini ve özellikle GD2 işareti bol olduğunda bu tümör hücrelerini laboratuvarda öldürme yeteneklerini keskin biçimde yükseltebileceğini gösteriyor. Bu çalışma hâlâ klinik öncesi aşamada ve hastalar yerine hücre kültürlerinde yapılmış olsa da, GD2’yi aşırı ifade eden akciğer kanserlerini tedavi etmek için yeni bir strateji öneriyor. Gelecekte bir tümörün GD2 düzeyinin ölçülmesi, böyle hedefe yönelik immün ‘‘çöpçatanlardan’’ fayda görme olasılığı en yüksek hastaları belirlemeye yardımcı olabilir; bu vaatlerin gerçek dünyada işe yarayıp yaramadığını görmek için daha fazla hayvan ve klinik çalışma gerekecektir.
Atıf: Sawasdee, N., Panya, A., Sujjitjoon, J. et al. Harnessing a bispecific αGD2 × αCD3 protein engager to target GD2-overexpressing lung tumors. Sci Rep 16, 12920 (2026). https://doi.org/10.1038/s41598-026-42885-2
Anahtar kelimeler: akciğer kanseri immünoterapisi, GD2 hedefleme, bispesifik aracılı, T hücresi yönlendirme, küçük hücre dışı akciğer kanseri