Clear Sky Science · zh
用于3D结肠癌靶向药物递送的近红外敏感姜黄素-明胶纳米颗粒的合成与表征
把一种香料变成智能抗癌武器
许多人知道姜黄素是常见厨房香料姜黄中那种鲜黄色的成分。除了烹饪上的名声外,姜黄素在实验室中能减缓癌细胞生长。但问题是人体对它的吸收不佳且易分解。本研究展示了科学家如何将姜黄素包装进微小的明胶颗粒中,变成一种“智能”结肠癌治疗剂——这些颗粒在受到近红外光温和加热时释放药物负载。
为什么结肠肿瘤难以治疗
结肠癌仍然是全球最常见且致死率较高的癌症之一。传统治疗如手术、化疗和放疗虽能挽救生命,但常常损伤健康组织,且在肿瘤产生耐药时可能失败。因此,研究者在寻找能够将作用集中在肿瘤内部同时尽量保护机体其它部位的疗法。本文团队致力于构建一种对外部触发(光)响应的药物系统,使大部分治疗作用仅在需要的位置发生,即结肠内或肿瘤附近。
设计微小的明胶载体
研究者以明胶为基础构建递药系统——明胶是一种熟悉的食品与医用材料,能被机体安全降解。他们将溶解的明胶与姜黄素混合,然后用短促的超声处理形成纳米颗粒——这些球状颗粒比一粒沙子小数千倍。通过仔细调节混合时间和姜黄素与明胶的比例,他们获得了约20–40纳米的稳定颗粒,能捕获大约三分之二的可用姜黄素。多项物理测试证实了颗粒的尺寸、结构和稳定性,并表明姜黄素主要由较弱的物理作用力而非永久性化学键束缚,从而更容易按需释放。 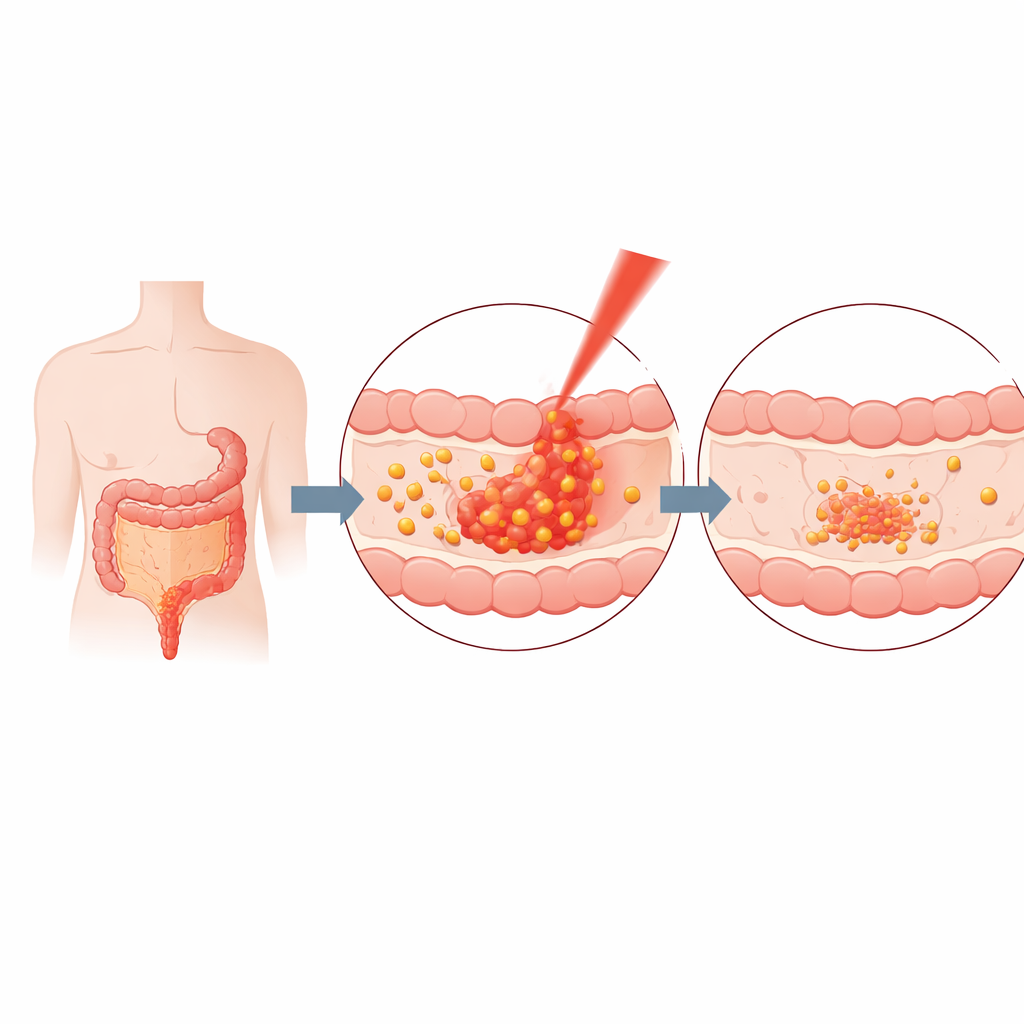
用温和加热作为开关
接着,团队探讨了近红外(NIR)光如何作为药物释放的远程控制。近红外光对肉眼不可见,但比可见光能更深地穿透组织,且已在一些医疗设备中应用。当姜黄素—明胶颗粒被近红外灯照射并被温和加热到约38°C——仅略高于正常体温时,颗粒体积膨胀并开始更快地泄漏姜黄素。在这一温和温度下,大约一半的被俘获药物被释放,且随时间的总体释放速度比未受光照时快约三分之一。重要的是,这种效应可在仅30秒的照射内实现,显示出一种快速的、对温度敏感的药物释放开关。 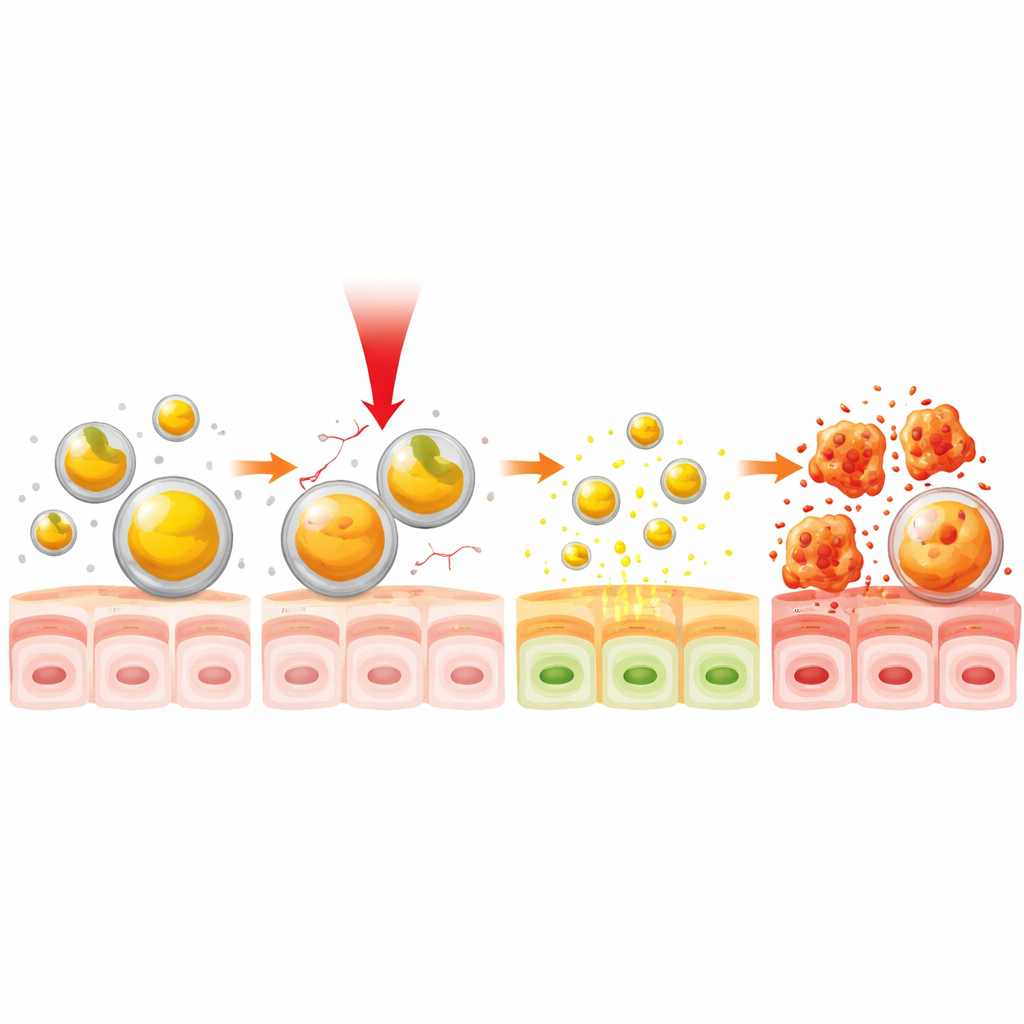
在2D和3D肿瘤模型中检验系统
为验证这种光激活系统是否确实损伤癌细胞,研究者在两种人结肠癌细胞系和培养皿中的健康血管内皮细胞上进行了测试。他们还构建了更真实的三维模型,让结肠癌细胞与内皮细胞共同生长,模拟带有支撑血管的微型肿瘤。由于姜黄素在特定光照下会自然发光,团队可以观察纳米颗粒进入细胞并在胞质中积累。在相当于25微克/毫升姜黄素剂量下,这些颗粒显著降低了癌细胞的存活、迁移和侵袭能力,尤其是在结合近红外加热时。相比之下,健康细胞在相同或更低剂量下受影响明显较小,提示对肿瘤组织具有一定选择性。
这些颗粒如何推动癌细胞走向死亡
除了简单计数存活细胞外,研究者还检查了治疗如何改变细胞行为。暴露于NIR激活姜黄素颗粒的癌细胞表现出典型的程序性细胞死亡(凋亡)特征:DNA浓缩、细胞核片段化,以及产能线粒体丧失正常电位并缩小。在测量细胞扩散和侵袭速度的伤口愈合和Transwell实验中,接受NIR处理的颗粒比未照光的颗粒更明显地减慢了癌细胞的迁移和侵袭。这些变化与姜黄素已知的降低有害活性氧分子和抑制炎性信号通路的作用一致,而这些通路有助于肿瘤生长和扩散。
对未来癌症治疗的潜在意义
简言之,这项工作将姜黄的活性成分转化为一种靶向的“远程控制”抗癌治疗。通过将姜黄素隐藏在可生物降解的明胶球中,并使用温和的近红外加热作为开—关开关,研究者在逼真的实验室模型中实现了快速、可控的药物释放和强效抗肿瘤作用,同时在很大程度上保护了健康细胞。尽管仍需更多动物与人体测试,这项研究为更精准、毒性更小且可能更易生产的结肠癌疗法指明了方向,并为基于安全天然化合物的光控智能治疗打开了门路。
引用: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
关键词: 结肠癌, 姜黄素, 纳米颗粒, 近红外光, 靶向药物递送